高一化学上学期9月份月考试题
化 学
测试范围:必修(1)第一章 从实验学化学
测试时间:2006年9月27
第I卷(选择部分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 P-31 S-32 Cl-35.5
Cu-64 Ba-137
一、选择题(每小题有1-2个选项符合题意,共45分)
1.进行化学实验必须注意实验安全。下列说法正确的是 ( )
A.不慎将酸溅到眼中,应立即水洗,边洗边眨眼睛
B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
C.不慎将酒精洒到桌面上着火时,可用水将其扑灭
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
2.下列混合物的分离和提纯方法中,主要是从溶解性的角度考虑的是 ( )
A.蒸发 B.蒸馏 C.过滤 D.萃取
3.下列说法正确的是
A.摩尔质量就等于物质的式量 B.摩尔质量就是物质式量的6.02×1023倍
C.HNO3的摩尔质量是63g D.硫酸和磷酸的摩尔质量相等
4.2molCl2和2molCO2相比较,下列叙述中正确的是 ( )
A.分子数相等 B.原子数相等 C.体积相等 D.质量相等
5.能够用来鉴别BaCl2 、 NaCl 、 Na2CO3三种物质的试剂是 ( )
A.AgNO3溶液 B.稀硫酸 C.稀盐酸 D.稀硝酸
6.现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ⑧氯化钠和单质溴的水
溶液,分离以上各混合液的正确方法依次是 ( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
7.下列有关阿佛加德罗常数(NA)的说法错误的是 ( )
A.32克O2所含的原子数目为NA
B.0.5molH2O含有的原子数目为1.5NA
C.1molH2O含有的H2O分子数目为NA
D.0.5NA个氯气分子的物质的量是0.5mol
8.下列提纯物质的实验方法不正确的是 ( )
①用Na2CO3溶液除去混在NaCl溶液中的MgCl2杂质
②用蒸馏法除去混在水中的氧气
③用酒精萃取溶解在水中的溴
④将KMnO4溶液减压低温蒸发,以获得晶体KMnO4
A.② B.③④ C.①②③ D.①②③④
9.有一种气体的质量是14.2g,体积是4.48升(STP),该气体的摩尔质量是 ( )
A.28.4 B.28.4g・mol-1 C.71 D.71g・mol-1
10.下列说法正确的是 ( )
A.1molO2和1molN2所占体积都为22.4L
B.H2的气体摩尔体积为22.4L
C.在标准状况下,1molH2和1molH2O所占的体积都为22.4L
D.在标准状况下,22.4L由N2、N2O组成的混合气体中所含有的N的物质的量为2mol
11.设NA为阿伏加德罗常数的值,下列关于0.2mol/L的Ba(NO3)2溶液不正确的说法是
( )
A.2L溶液中的阴、阳离子总数为0.8NA
B.500mL溶液中NO3-浓度为0.2mol/L
C.500mL溶液中Ba2+浓度为0.2mol/L
D.500mL溶液中NO3-总数为0.2 NA
12.已知丙酮(C3H6O)通常是无色液体,不溶于水,密度小于1g/mL,沸点约为55℃。要从水与丙酮的混合液里将丙酮分离出来,下列方法最合理的是 ( )
A.蒸馏 B.分液 C.过滤 D.蒸发
13.在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高
( )B
A.所用NaOH已经潮解 B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里 D.称量时误用“左码右物”
14.20mLCaCl2溶液加水稀释至100mL,稀释后的溶液中Cl-离子的物质的量浓度为1mol/L,则稀释前CaCl2的物质的量浓度为 ( )
A.2.5mol/L B.5mol/L C.1.25 mol/L D.2mol/L
15.20℃时,NaCl的溶解度36g,此时NaCl饱和溶液的密度为1.12g/cm3,在此温度下NaCl饱和溶液的物质的量浓度为 ( )
A.0.15mol/L B.1.36mol/L C.5.07mol/L D.6.15mol/L
第Ⅱ卷(非选择题部分)
二、填空题(本题包括3小题,共25分)
 16.(4分)有A、B两种有机液体的混合物,如果A、B互溶,且相互不发生化学反应,在常压下,A的沸点为35℃,B的沸点为200℃。回答以下问题:
16.(4分)有A、B两种有机液体的混合物,如果A、B互溶,且相互不发生化学反应,在常压下,A的沸点为35℃,B的沸点为200℃。回答以下问题:
(1)用蒸馏方法分离和提纯该混合物,必不可少的玻璃仪器和用品
是________________。
(2)如果加热升温后,3 min~10 min收集第一个馏分,15 min~
25 min收集第二个馏分。请在右图的格纸中画出蒸馏法分离
提纯该混合液的温度与时间关系示意图。
17.(11分)粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥砂
等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯 ;②固定铁
圈位置 ;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌; ⑤停止加热。其正确的操作顺序为 。
(2)如何运用最简方法检验溶液中有无SO42-离子? 。如
果有,应该如何除去SO42-离子? 。
(3)在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为
止。请问这步操作的目的是 。
(4)将经过操作(3)后的溶液过滤。请问这一操作能除掉哪些杂质?
。
(5)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要
用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;
溶解时: 、过滤时: 、蒸发时: 。
18.(10分)实验室配制0.1mol/L的BaCl2溶液分成两个阶段:第一阶段:用托盘天平称取5.2g无水BaCl2晶体。第二阶段:溶解配制成0.1mol/L的BaCl2溶液。第一阶段操作有如下几步:
A.将游码拨至0.2g处;
B.将游码拨至“0”处;
C.在天平的两边托盘上各放一张干净等质量的滤纸,调节天平两边螺丝使天平平衡;D.取走药品,将砝码放回砝码盒内;
E.往左盘内逐步添加晶体至天平平衡;
F.在右盘放置5g砝码。
(1)其正确的操作顺序是(填序号):___________________
(2)当E操作时,只缺少量晶体时,其操作是_____________________________
(3)第二阶段操作,应先将5.2gBaCl2加适量蒸馏水溶解,溶解过程中使用的主要仪器有_______________________,然后将溶液转入_________中,再_________、___________、___________后即可得到0.1mol/LBaCl2溶液。
(4)下列操作使配制的BaCl2溶液浓度偏低的有__________
A.如果将砝码放在左盘上,BaCl2放在右盘上进行称量
B.如果选用的容量瓶内有少量蒸馏水
C.如果定容摇匀后,液面下降,又加水到刻度线
D.如果整个配制过程中,容量瓶不振荡
三、填空题(本题包括2小题,共18分)
19.(10分)mg某气体,它由双原子分子构成,它的摩尔质量为Mg・mol-1。若阿伏加
德罗常数用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为_______ _个。
(3)该气体在标准状况下的体积为____________L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为______ _。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____ g・mol-1。
20.(8分)2003年3月日本筑波材料科学国家实验室一个研究小组发现首例带结晶水的
晶体在5K下呈现超导性。据报道,该晶体的化学式为 Na0.35CoO2 • 1.3H2O。试计算:该晶体的摩尔质量是 ;钴原子与氧原子的物质的量之比是 ;钴原子与氧原子的个数之比是 ;1mol该晶体中含有的氧原子数目是 。(比值可以用小数表示)
四、计算题(本题包括2小题,共12分)
21.(6分)在标准状况下,将224L HCl气体溶于635mL水中,所得盐酸的密度为1.18g/cm3。试计算:
(1)所得盐酸的质量分数和物质的量浓度。
(2)取出这种盐酸100mL,稀释至1.18L,所得稀盐酸的物质的量浓度。
22.(6分)常温下,在27.5g水中溶解12.5gCuSO4.5H2O,恰好达到饱和,该溶液密度为1.21g/cm3。求
(1)该溶液中阴阳离子的总物质的量
(2)该溶液中CuSO4的物质的量浓度
参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | AB | CD | D | A | B | C | A | C |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | |
| 答案 | D | D | AB | B | B | A | C |
 16.
16.
(1)蒸馏烧瓶(或圆底烧瓶、平底烧瓶)、温度计、冷凝管、
锥形瓶;沸石(或碎瓷片)
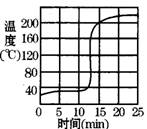
(2)见图 (每小题2分)
17.
(1)①②③④⑤(2分)
(2)静止片刻在上层清液处,滴加一滴BaCl2溶液,如果出
现白色浑浊或者沉淀,则溶液中有SO42-,不出现浑浊就说明SO42-已经除尽。(2分)
除去SO42-的方法是在溶液中加入过量的BaCl2溶液。(1分)
(3)除去Ca2+、Mg2+以及加入过量Ba2+ (1分)
(4)BaSO4、CaCO3、MgCO3、BaCO3等杂质 (2分)
(5)搅拌,加速溶解 ;使待滤液体沿玻璃棒流入漏斗,防止外洒;搅拌,防止因局
部过热液滴或晶体飞溅。(各1分)
18.
(1)DFEDB;(2分)
(2)左手拿药匙,用右手轻拍左手手腕,小心振动药题加足药品,
使天平平衡;(1分)
(3)烧杯、玻璃棒、250mL容量瓶;洗涤、定容、摇匀;(每空1分)
(4)AC(2分)
19.
(1)m/9M;
(2)2mNA/M;
(3)22.4m/M;
(4)m/(m+1000);
(5)m/MV (每空2分)
20.122 g・mol-1 ;1:3.3 ;1:3.3 ;1.99×1024 个(每空2分)
21.(1)36.5% ;11.8mol・L-1
(2)1mol・L-1 (每个答案2分)
22.(1)阴阳离子总物质的量为0.1mol
(2) 1.51mol/L (每小题3分)