��һ��ѧ�����п��Ի�ѧ����
ʱ�䣺90���ӡ����֣�100��
�༶�������������� ���� ������������ �÷� ��������������
һ��ѡ����(ÿС��ֻ��һ����ȷѡ�ÿ��3�֣���60��)
1�������ꡱʹɭ�������������ữ���ż��ٻ��ȣ������ꡱ�����������Σ��Խ��Խ�����������������ǰ����ɡ����ꡱ����Ҫԭ���ǡ������������������������������� ����������(����)
(A)����ȼ�պ���ȼ�ϣ�ұ���������ȡ���(B)������ɳ����ֲ�����ƻ�
(C)�����ŷų�����ˮ������������������ (D)��������������
2�����з�Ӧ����������ԭ��Ӧ���ǡ��������������������������������������� ����(����)
(A)3CuO + 2NH3 = 3Cu + N2��+ 3H2O������(B)NaOH + HCl ==NaCl +H2O
( C ) SO3 + H2O== H2SO4�������������� ��D��CaO + H2O = Ca(OH)2
3������ȼ���У������ڻ�ʯȼ�ϵ��ǡ������������������������������������� ���� (����)
(A)���͡����� (B)ú���������� (C)��ȼ���������������� (D)����
4�����з�Ӧ�������û���Ӧ���ǡ����������������������������������������� ���� (����)
(A)3Fe + 4H2O![]() Fe3O4 + 4H2��������
(B)4NH3 +3O2(��)
Fe3O4 + 4H2��������
(B)4NH3 +3O2(��) ![]() 2N2 +
6 H2O
2N2 +
6 H2O
(C)2Al +2NaOH+2H2O==2NaAlO2+3H2����(D)CuO +CO ![]() Cu + CO2
Cu + CO2
5������ʵ������У�����ȷ���ǡ����������������������������������������� ������ (����)
(A)�� ʹ�þƾ���ǰ��������������ƾ�
(B)�� ���Թ����Һ����ȣ�Һ������������Թ��ݻ���1/3
(C)�� ϡ��Ũ����ʱ����Ũ��������������ע��ʢˮ���ձ���
(D) ��©������ʱ��Һ�������ֽ�ı�Ե
6��ij�ǽ���Ԫ��X������ϼ�Ϊ+m�����������������Ӧˮ����ķ�������b����ԭ��,��
����������������Ӧˮ����ķ���ʽΪ�������������������������������������� (����)
��A��Hm+2bXOb�������� ��B��Hm-2bXOb����(C)H2m+bXOb��(D)H2b-mXOb
7������һ������������ϡ���ᣬ��Ͳ��ƽ������Կ̶��ߡ���ȡŨ����ʱ�������ӣ���ˮʱ���߸��ӣ��������Ƶ�ϡ����ʵ�ʵ������������������������������� ������������������(����)
(A)ƫ�͡������� (B) ƫ�ߡ��������� (C) ����Ӱ�졡���� (D) ���ж�
8��������������ȷ���ǡ��������������������������������������� ����������������(����)
(A)�� �����Ԫ�صĻ����һ������ǿ������
(B)�� ������ֻ�������ԣ�������ֻ�л�ԭ��
(C)�� ʧ����Խ�࣬��ԭ��Խǿ
(D) ǿ��������ǿ��ԭ����һ���ܷ���������ԭ��Ӧ
9��������������ԭ��Ӧ��
�١��� Fe + CuSO4== Cu + FeSO4
�ڡ��� Cu +2FeCl3== CuCl2 +2FeCl2
�ۡ��� 2KMnO4 +16HCl ==2KCl +2MnCl2 +5Cl2��+ 8H2O
�ܡ��� 2FeCl2 + Cl2 ==2FeCl3
�� ����������Ӧ���жϸ����ӵ���������ǿ������˳����ȷ���ǡ������������� (����)
(A)�� MnO4-��Cl2��Fe3+��Cu2+��Fe2+
(B)�� Cl2��MnO4-��Cu2+��Fe2+��Fe3+
(C)�� MnO4-��Fe3+��Cu2+��Cl2��Fe2+
(D) Fe3+��MnO4-��Cl2��Cu2+��Fe2+
10��20g�����С�մ�Ļ������ȵ�����ʱ������4.4gCO2�����ڻ�����У���������������ǡ������������������������������������������������������������� ������������ (����)
(A)84������������ (B) 8.4������������ (C) 16�������������� (D) 1.6��
11���ƺͼ���ɵĺϽ�4.6g����������ˮ��ַ�Ӧ���õ�H2�����������ǡ����������� (����)
(A)0.29g�������� (B) 0.18g���������� (C) 2g�������������� (D)1 g
12���������ʼ���ˮ���������ȵ��ǡ��������������������������������������� ���� (����)
(A)����NaCl���� (B)��ʯ�ҡ��������� (C)��ˮ�Ҵ��������� (D)����NH4NO3
13�����и�������������Һ�д���������ǡ������������������������������� ������( ��)
(A)Na+��H+��Cl-��HCO3-�������������� (B)Na+��Ca2+��HCO3-��OH-
(C ) Fe3+��Cl-��OH-��K +�������������� (D)Cu2+��Cl-��SO42-��K+
14���������ӷ���ʽ�д�����ǡ����������������������������������������� ������ (����)
(A)�� ����ϡ���ᷴӦ: 2Fe + 6H+==2Fe3+ +2H2��
(B)�� ��������Լ���Һ��Ӧ: CH3COOH + OH- == CH3COO- +H2O
(C)�� ̼��þ�����ᷴӦ�� MgCO3 + 2H+ == Mg2+ +H2O + CO2��
(D) ̼�������Һ�����ᷴӦ��HCO3- + H+ == CO2�� + H2O
15�������л�����������ͭ���ʣ����������۷ŵ�һ������ϡ�����У���ַ�Ӧ���������ײ���������ʣ�࣬���������Һ��Ľ��������ӡ����������������������� ���������� (����)
(A)�϶���Cu2+��Fe2+������������������ (B)�϶���Cu2+��������Fe2+
(C )�϶���Fe2+��������Cu2+ ������������(D)�϶���Fe2+��û��Cu2+
16�����¸����ʵ����ʱȽ��У���ȷ���ǡ��������������������������������� ��������(����)
(A)���ȶ��ԣ�Na2CO3��NaHCO3��H2CO3������(B)�ܽ��Na2CO3�� NaHCO3��H2CO3
(C)���� RbOH��KOH��LiOH�������������� (D)������Rb+��K+��Na+
17����һ��������NH4NO3���ȷֽ⣬�仯ѧ����ʽΪ��5 NH4NO3 ![]() 2HNO3+ 4N2 +9H2O
2HNO3+ 4N2 +9H2O
�ڷ�Ӧ�б������뱻��ԭ�ĵ�ԭ����֮��Ϊ�������������������������������� ������(����)
(A)3 ��5���� (B) 5 ��3������ (C) 1 ��1�������� (D) 5 ��4
18����һƿ�����͵�NaOH��Һ��ƽ���ֳ��ĵȷݣ����¶Ȳ���������£��ֱ�������й����е�һ�֣�ʹ��Һ�ﵽ���ͣ���������ʵ����������ǡ��������������� ��������������(����)
(A)Na��������(B) Na2O�������� (C) NaOH��������(D) Na2O2
19.Ԫ��X��һ�ּ���������й���X���仯�����˵��������ȷ���ǡ��������� ������ (����)
(A)�� ��ˮ�����εĻ�ѧʽ��X2SO4
(B)�� ������������һ��ǿ��
(C)�� �䵥����һ�����õĻ�ԭ��
(D) �䵥�ʿ����ɶ�Ӧ���������뽹̿���ȶ��Ƶ�
20����������Һ��ͨ�����CO2���й����������ǡ��������������������������� ���� (����)
��Ba(NO3)2������Na2CO3 ������Һ �������۰����ı���ʳ��ˮ���� ��CaCl2
(A)ȫ�������������� (B) �ڢۡ��������� (C) �ۢܡ��������� (D) �٢�
���������(��25��)
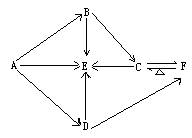
21������ͼ��ʾ�����仯�У�AΪ������BΪ����ɫ�����ĩ����ÿһ�����ʾ�����AԪ�ء�D��ˮ��Һ��AgNO3��Һ��Ӧ���ɲ�����ϡHNO3�İ�ɫ������������������⡣
(1)�ƶ�(д��ѧʽ) E ����������������F �������������� ��
(2)������з�Ӧ�ķ���ʽ�������ӷ�Ӧ����д�����ӷ���ʽ����������ԭ��Ӧ����������ת�Ƶķ������Ŀ��
![]() A������E ����������������������������������������������
A������E ����������������������������������������������
22���ش��������⣺
(1)�� ��Ϊʲô���ܱ����������У�
������������������������������������������������������������
(2)�� H+Ϊʲô����OH-�����кͷ�Ӧ��
�������� ����������������������������������������������������������
(3)�� ̼��ȼ��Ϊʲô�Ƿ��ȷ�Ӧ��
�������� ����������������������������������������������������������
(4)�� �ƾ���ˮ��ҺΪʲô�����磿
�������� ����������������������������������������������������������
23���ڽ����й�ȼ�ϳ��ȼ�յ���������ʱ�������������
��ͬѧ��Ϊ��������ã�
��ͬѧ��Ϊ������Ҫ������
����Ϊ������λͬѧ���������ȷ��������ʲô��
����������������������������������������������������������������������������
������������������������������������������
����ʵ����(��15��)
24����H2SO4��NaHCO3��BaCl2��Na2SO4������Һ���ֱ�ʢ�ڱ��ΪA��B��C��D����֧�Թ��У�����������ʾ��ʵ�飬�ݴ�������ȷ��B��C��D����ʲô���ʣ����ش��������⡣
| ʵ�� | ��Ӧ���� | ���� |
| A+B | ������ɫ���� | B�� |
| A+C | ���������� | C�� |
| A+D | ������ɫ���� | D�� |
(1)B�� ��������������C�� ������������ ��D�������������� ��
![]()
![]() (2)д��A +B���� ��A + D���� ����Ӧ�����ӷ���ʽ��
(2)д��A +B���� ��A + D���� ����Ӧ�����ӷ���ʽ��
![]() A +B���� ������������������������������������ ��
A +B���� ������������������������������������ ��
![]() A +D���� ��������������������������������������
A +D���� ��������������������������������������
25��(1)����NaCl��Һ����Na2CO3���Լ��� �������������� ������NaHCO3��Һ����Na2CO3���Լ�������������������
(2)����Na2CO3�����к���NaHCO3�ķ����� ������������������������������������������
��������������������������������������������������
����һ��ѡ����
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| A | A | D | D | A | D | B | D | A | C |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| B | B | D | A | D | A | B | C | D | B |
�������
21��(1)��E:��NaOH �� F :�� NaHCO3
(2) �� ʧ2��e-
![]()
![]() 2Na��+��2H2O��===
2Na+��+��2OH-��+
H2��
2Na��+��2H2O��===
2Na+��+��2OH-��+
H2��
��2��e-
22.(1)�������ӷ�
(2)���߷�Ӧ�����ѵ����ˮ
(3)��̼��O2������������CO2������
(4)�ƾ��Ƿǵ������ˮ�в��ܵ���������ƶ������ӡ�
23����ͬѧ�������ȷ����Ϊ��������ʱ������Ŀ��������������
24��(1)B :NaHCO3�� C;Na2SO4����D:BaCl2
�� (2)HCO3- + H+ == CO2�� + H2O��; Ba2+��+SO42- == BaSO4��
25��(1)���CaCl2��BaCl2��Һ ��(2)ȡ������������Թ��м��Ƚ�����������ͨ�����ʯ��ˮ��ʯ��ˮ����ǡ�