高一化学第一学期期末考试3
高一化学试题
本卷完成时间:100分钟 满分:100分
一、选择题(每小题只有一个正确选项,每小题2分,共20分)
1、下列叙述中,正确的是( )
A.H2SO4的摩尔质量是98
B.等质量的O2和O3中所含的氧原子个数相等
C.等质量的CO2和CO中所含的碳原子个数相等
D.将98gH2SO4溶解于500mL水中,所得溶液中H2SO4的物质的量浓度为2mol/L
2、在下列物质中,含有分子数目最多的是( )
A.22.4LH2(标准状况) B.3.01×1023个Cl2
C. 9×10-3kg H2O D.600mL2mol/L蔗糖溶液中的溶质
3、在1L溶有0.1molNaCl和0.1molMgCl2的溶液中,Cl-的物质的量浓度为( )
A.0.05mol/L B.0.1mol/L C.0.2mol/L D.0.3mol/L
4、在下列的反应中,能放出气体,但不是氧化还原反应的是( )
A.浓盐酸与二氧化锰共热 B.石灰石与稀盐酸反应
C.过氧化钠与水反应 D.铁与稀硫酸反应
5、在下列物质中,长期放置在空气中能发生氧化还原反应的是( )
A.Na2O2 B.Na2SO4 C.Na2CO3 D.NaOH
6、在下列反应中,属于离子反应,同时溶液的颜色发生变化的是( )
A.BaCl2溶液与K2SO4溶液反应 B.点燃H2与Cl2的混合气体
C.NaOH溶液与CuSO4溶液反应 D.Cu与浓硫酸反应
7、在下列物质的水溶液分别加入澄清石灰水,原溶液中的阴离子和阳离子都减少的是( )
A.CuSO4 B.Ba(NO3)2 C.Na2CO3 D.FeCl2
8、在下列物质中,溶于水后可以生成两种酸的是( )
A.SO2 B.Cl2 C.HCl D.CO2
9、下列物质属于纯净物的是( )
A.漂白粉 B.氯水 C.液氯 D.碘酒
10、为了防止溴的挥发,实验室常在盛溴的试剂瓶中加些( )
A.CCl4 B.液体石蜡 C.水 D.酒精
二、选择题(每小题可能有1-2个正确选项,多选、错选不得分,不选得1分,每小题3分,共30分)
11、在下列反应中,H2SO4不是氧化剂的是( )
A.2HBr + H2SO4 === Br2 ↑ + SO2 ↑ + 2H2O
B.BaCl2 + H2SO4 === BaSO4 ↓ + 2HCl
C.Fe + H2SO4 === FeSO4 + H2 ↑
D.2NaOH + H2SO4 === Na2SO4 + 2H2O
12、在下列反应中,其离子方程式可以用H+ + OH- === H2O表示的是( )
A.Ba(OH)2溶液与稀硫酸反应 B.Cu(OH)2与稀硝酸反应
C.Ca(OH)2溶液与盐酸反应 D.Al(OH)3与盐酸反应
13、将下列物质的量浓度相等的溶液等体积两两混合有白色沉淀生成,加入过量的稀硝酸后,沉淀消失并放出气体,再加入AgNO3溶液又有白色沉淀生成的是( )
A.Na2CO3和Ca(OH)2 B.Na2CO3和CaCl2
C.Ca(HCO3)2和NaOH D.Na2SO4和Ba(NO3)2
14、下列离子方程式书写正确的是( )
A.二氧化硫与水反应:SO2 + H2O === 2H+ +SO32-
B.碳酸钙与盐酸反应:CO32- + 2H+ === CO2 ↑ + H2O
C.硫酸铜溶液与氢氧化钡溶液反应:Ba2+ + SO42- === BaSO4↓
D.铁与稀硫酸反应:Fe + 2H+ === Fe2+ + H2 ↑
15、在化学上,常用CaH2作为制取氢气的药剂,有关反应的化学方程式为:CaH2 + 2H2O == Ca(OH)2 + 2H2↑。在这个反应中,H2O( )
A.是还原剂 B.是氧化剂
C.是溶剂 D.既不是氧化剂,也不是还原剂
16、下列各组中的离子,能够大量共存于同一溶液中的是( )
A.CO32-、H+、Na+、NO3- B.H+、Ag+、Cl-、SO42-
C.K+、H+、Cl-、OH- D.OH-、NO3-、K+、Na+
17、在标准状况下,将VLA气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为dg/cm3,则此溶液的物质的量浓度为( )
A.Vd/(MV + 2240)mol/L B.1000Vd/(MV + 2240)mol/L
C.1000VdM/(MV + 2240)mol/L D.MV/[22.4(v+0.1)d]mol/L
18、nLMgCl2溶液与nLNaCl溶液混合后,Cl-的物质的量浓度为3mol/L,则原来MgCl2溶液和NaCl溶液的物质的量浓度为( )
A.都为3mol/L B.都为6mol/L
C.都为2mol/L D.分别为1mol/L和4mol/L
19、把过量的氯气通入溴化钠和碘化钾溶液中,然后将溶液蒸干,灼烧,最后残留物是( )
A.KCl和Br2 B.KBr和NaCl C.KCl和NaBr D.KCl和NaCl
20、三种黑色粉末MnO2、炭粉、CuO,只用一种物质将它们区别开,这种物质是( )
A.稀H2SO4 B.浓HCl C.红墨水 D.NaOH溶液
三、填空题
21、(4分)已知CN-(氢氰酸根离子)和Cl-有相似之处,HCN(氰化氢)的某些性质与氯化氢相似。(SCN)2(硫氰)与Cl2的性质有相似之处,且常温常压下也是气体。写出下列反应的化学方程式。
(1)MnO2和HCN溶液加热反应:
(2)(SCN)2和KOH溶液反应:
22、(4分)将体积为V、物质的量浓度为c的K2SO4溶液与体积为V/2、物质的量浓度也为c的BaCl2溶液混合后(假设混合液的体积等于两溶液体积之和),溶液中SO42-的物质的量浓度为 ,K+的物质的量浓度为
23、(6分)将质量为m1的NaHCO3固体加热分解一段时间后,测得剩余固体的质量为m2。
(1)未分解的NaHCO3的质量为
(2)生成的Na2CO3的质量为
(3)当剩余固体的质量为 ,可以断定NaHCO3已完全分解。
四、实验题
24、(10分)现有A、B、C、D、E五种溶液中,只知道它们的溶质是NaHCO3、K2CO3、NaOH、HCl和Ca(HCO3)2。为了鉴别开来,各取少量进行如下实验:
(1)A与B混合无明显现象
(2)B与C(或D,或E)混合均有无色气体产生
(3)D与A(或E)混合均有白色沉淀产生
试根据以上现象,推断A-E各是何物质
A B C D E
25、(10分)实验室用下列所给仪器(如下图)组装实验装置制备纯净的无水CuCl2。试回答下列问题:
(1)组装氯气发生装置,应选用的仪器是 ,E的名称是
(2)按Cl2气流方向,其余装置的连接顺序(用数字1,2……填入)是:
![]()
![]()
![]()
![]() ( ) ( )( ) ( )( ) ( )( ) ( )
( ) ( )( ) ( )( ) ( )( ) ( )
(3)装置A的作用是
(4 )装置F的烧杯中盛 (填名称),其作用是 ,反应方程式是 。
(5)待充分反应后,装置D的玻璃管中剩余物呈 色,冷却后,将制得的产物配成饱和溶液,呈 色。
五、推断题(8分)
26、下图中A―G为中学化学中常见物质,它们有如图所示的反应关系:
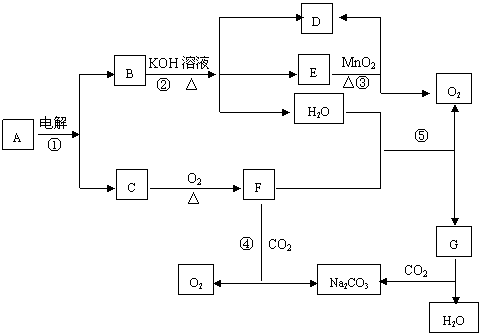
(黄绿色气体)
已知Cl2通入热NaOH溶液中发生的反应为:
3Cl2 + 6NaOH == 5NaCl + NaClO3 + 3H2O
(1)写出E的化学式
(2)反应④的化学方程式:
(3)反应⑤的化学方程式:
(4)反应②的离子方程式:
六、计算题(8分)
27、用密度为1.20g/cm3HCl的质量分数为36.5%的浓盐酸500ml与二氧化锰反应,生成的氯气在标准状况下体积为11.2L。计算:
①浓盐酸中HCl的物质的量
②在反应中被氧化的HCl的物质的量
③向反应后的溶液中加NaOH溶液使Mn2+刚好沉淀完全时,所需NaOH的物质的量。
高一化学答题纸
2004.1
一、选择题(每小题2分,共20分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
二、选择题(每小题3分,共30分)
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
三、填空题
21、(4分)
(1)
(2)
22、(4分) ,
23、(6分)
(1)
(2)
(3)
四、实验题
24、(10分)A B C D E
25、(10分)
(1) ,
![]()
![]()
![]()
![]() (2) ( ) ( )( ) ( )( ) ( )( ) ( )(3)
(2) ( ) ( )( ) ( )( ) ( )( ) ( )(3)
(4) , ,
(5) ,
五、推断题
26、(8分)
(1)
(2)
(3)
(4)
六、计算题(8分)
27、
高一化学答题纸
一、选择题(每小题2分,共20分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| B | D | D | B | A | C | A | B | C | C |
二、选择题(每小题3分,共30分)
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| BD | C | B | D | B | D | B | CD | D | B |
|
(1)MnO2 + 4HCN == Mn(CN)2 + (CN)2↑+2H2O
(2)(SCN)2 + 2KOH == KSCN + KSCNO + H2O
22、(4分)![]() C,
C, ![]() C
C
23、(6分)
(1)![]() (2)
(2)![]() (3)
(3)![]()
四、实验题
24、(10分)A 、NaOH B、 HCl C、NaHCO3 D、Ca(HCO3)2 E、Na2CO3
25、(10分)
(1) C、E, 分液漏斗
![]()
![]()
![]()
![]() (2) ( 5 ) ( 1 )( 2 ) ( 4 )( 3 ) ( 6 )( 7 ) ( 8 )(3)除去Cl2中的HCl杂质
(2) ( 5 ) ( 1 )( 2 ) ( 4 )( 3 ) ( 6 )( 7 ) ( 8 )(3)除去Cl2中的HCl杂质
(4)氢氧化钠溶液, 除去多余Cl2
Cl2 + NaOH = NaCl + NaClO + H2O
(5)棕色 , 绿色
五、推断题
26、(8分)
(1)KClO3
(2)2Na2O2 + 2CO2 = 2Na2CO3 + O2
(3)2Na2O2 + 2H2O = 4NaOH + O2 ↑
(4)3Cl2 + 6OH- = 5Cl‑ +ClO3- +3H2O
六、计算题(8分)
27、(1)12.0mol/L (2)1.00mol (3)5.00mol