高一化学上学期期末调研考试
试题
一.单项选择题(每题4分)
1.下列措施中,符合易燃,易爆物的安全要求的是
A.为了安全,存放易燃物的仓库应尽可能的封闭,不让风吹进来
B.为了节省运费,把酒精和鞭炮等物品同时装在一辆货车上
C.只要不影响工作,面粉厂的工人可以在车间内吸烟
D.生产酒精的车间里,所有的照明设备均采用隔离和封闭装置
2.下列说法正确的是
①22.4L氧气中一定含有6.02×1023个氧分子
②将80gNaOH溶于1L水中所得的溶液中NaOH的物质的量的浓度是2mol/L
③18g水在标况下的体积为22.4L
④在标况下,20mlNH3和60ml氧气所含分子数的比为1:3
A.①②③④ B.①②④ C.②③ D.④
3.有甲乙丙三种溶液,各含一种离子X(负1价)(可能为氯离子,溴离子,碘离子),向甲中加入淀粉溶液和氯水溶液
变为橙色,再加入丙溶液,颜色无明显变化,则甲乙丙依次含有
A. 溴离子,氯离子,碘离子 B. 溴离子,碘离子,氯离子
C. 碘离子,溴离子,氯离子 D. 氯离子,碘离子,溴离子
4.Na2O2和足量的NaHCO3固体混合物,在密闭容器中充分加热,排除气体物质后冷却,残留的固体物质是
A..Na2O2 ,Na2CO3 B.Na2CO3 C.Na2CO3 ,NaOH D. Na2CO3 ,NaOH, Na2O2
5.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,对砹及其化合物的叙述不正确的是
A.At-的还原性强于Br- B.NaAt属离子化合物
C.砹在常温下为白色固体 D.砹不溶于水易溶于四氯化碳
6.下列物质按强电解质,弱电解质,非电解质的顺序排列的是
①.烧碱,纯碱,苛性钠 ②硫酸氢钠,醋酸,蔗糖
③氯酸钾,硫化氢(H2S),氧气 ④硫酸,亚硫酸,氨气
A.②④ B.②③ C.①④ D.①③
7.在一定体积的容器中加入1.5mol疝气和0.75mol氟气(F2),于400℃和2633KPa下加热数小时,然后迅速冷却至25℃
容器内除得到一种无色晶体外,还余下4.5mol氟气,所得晶体中疝与氟的原子个数比为
A.1:2 B.1:3 C.1:4 D.1:6
8.重铬酸钾[(NH4)2Cr2O7]是一种受热易分解的盐,下列各组对重铬酸钾受热分解产物判断符合实际的是
A.CrO3+NH3+O2 B.Cr2O3+NH3+H2O C.Cr2O3+N2+H2O D.CrO3+N2+H2O
9.在体积为1升的干燥烧瓶中用排气法收集HCl气体后,测得烧瓶中气体的体积的密度是氧气密度的 1.082倍,以此
气体进行喷泉实验,当喷泉停止后,进入烧瓶中的液体的体积为
A.1/2L B.1/4L C.3/4L D.全满
10.体积相同的某植物营养液A,B两份,其配方:A中含氯化钾0.3mol,硫酸钾0.2mol,硫酸锌0.1molB中含氯化钾0.1mol
硫酸钾0.3mol,氯化锌0.1mol,由此推断两液的成分
A.仅c(K+)相同 B.仅c(Cl-)相同 C.完全相同 D.完全不同
11.下列离子方程式书写正确的是
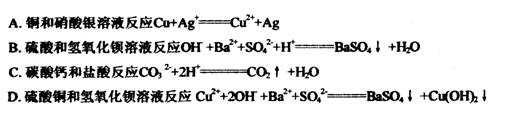
12已知X2,Y2,Z2,W2 四种物质的氧化能力W2>Z2>X2>Y2,下列氧化还原反应不能发生的是
①2NaW+Z2====2NaZ+W2 ②2NaX+Z2 ==== 2NaZ+X2
③2NaY+W2 =====2NaW+Y2 ④2NaZ+X2 ====2NaX+Z2
A.②③ B.①④ C.①② D.③④
13.向KI溶液中加入硝酸银溶液,直到反应完全为止。反应后溶液的质量恰好等于原KI溶液的质量。则所加硝酸银溶
液的质量分数是
A.50% B.38.2% C.48.8% D.72.3%
14.将Cl2 通入NaOH溶液中,反应得到NaCl,NaClO3,NaClO的混合溶液,其中ClO-,ClO3-的浓度比为3:1则Cl2 与
NaOH反应时,被还原的氯元素和被氧化的氯元素的物质的量的比是
A.21:5 B.11:3 C.3:1 D.4:1
15.工业上常用氨碱法制取碳酸钠(将NH3和CO2先后通入饱和食盐水析出小苏打:NH3+CO2+H2O=
NH4HCO3,NH4HCO3+NaCl=NaHCO3+NH4Cl然后经过滤、焙烧而得到纯碱),但却不能用氨碱法制
碳酸钾,这是因为在溶液中:
A、KHCO3的溶解度较大 B、KHCO3的溶解度较小
C、K2CO3的溶解度较大 D、K2CO3的溶解度较小
二.解答题(40分)
16.(11分)(1)“神舟四号”模拟载人飞船于2002年12月30日在酒泉载人航天发射场发射升空,按预定轨道在太空环绕地球飞行107圈,于2003年1月5日在内蒙古地区对飞船进行了成功回收。回答下列问题:
①有一种火箭推进器中盛有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合反应时生成无污染的物质并放出大量的热,从而产生巨大的推动力。写出该反应的化学方程式: .
②在宇宙气飞船中,一般要安装盛有Na2O2颗粒的装置,用来提供氧气,若用KO2(超氧化钾)代替,效果更佳。写出在飞船舱内用生成氧气的化学方程式: ,该反应中氧化剂与还原剂的物质的量之比为 ,电子转移的数目为 。
⑵在含有溴化钠和碘化钾的溶液中通入足量的氯气,最后将溶液蒸干并灼烧,剩余固体是_______反应的离子方程式
是________________________
17.(3分)用18mol/L的硫酸配制100ml 1mol/L的稀硫酸,若仪器有:A托盘天平,B50ml 容量瓶,C玻璃 棒,
D胶头滴管,E50ml烧杯,F10ml 量筒,G100ml 量筒,H100ml 容量瓶。则实验时,按仪器
使用的先后顺序写出所需仪器的编号 ______
18.(6分)已知①A,B,C,D四种物质中均含元素X,有的还可能含有元素Y,Z。元素Y,X,Z的原子序数依次
递增
②X在A,B,C,D中均不呈现它的最高价
③室温下单质A与某种常见的一元强碱溶液反应,可得到B,C
④化合物D受热催化分解,可得到元素Y的单质
⑴元素X是______Z是______
⑵写出③中的化学方程式__________________
⑶写出④中的化学方程式______________________________
19(12分)实验室用如图所示的仪器药品制取氯化铁粉末,已知氯化铁粉末很容易吸水生成结晶水化合
物FeCl3+6H2O==FeCl3・6H2O,加热时其分解如下2FeCl3・6H2O==3H3O↑+6HCl↑+Fe2O3
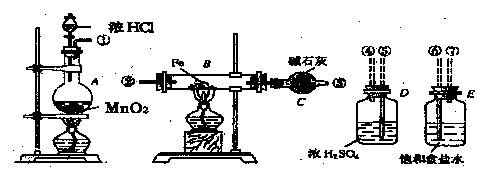
⑴按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序)
①接____,____接____,____接____
⑵烧瓶A中的反应是__________________,B中的反应是__________________
⑶干燥管C中的碱石灰的作用是________,容器D作用是__________________
容器E的作用是__________________
20. (8分)为了预防碘缺乏病,国家规定每千克食盐中应含40mg---50mg的碘酸钾。为测验某食盐是否为加碘的合格
食盐,某同学取食盐428克,设法溶解全部的碘酸钾,将溶液酸化并加入足量的碘化钾淀粉溶液,溶液呈蓝色,
再用0.030mol/L的硫代硫酸钠溶液滴定,用去18.00ml时蓝色刚好褪去。试通过计算说明该盐是否为合格产品。
上学期期末调研考试
高一化学试题
1~5DDBBC 6~10ACDCC 11~15DADDA
16.(1) N2H4+2H2O2=N2+4H2O(2分);4KO2+2CO2=2K2CO3+3O2(2分) 1:3(1分) 3e-(1分)
(2) NaCl,KCl(1分)
![]() (4分)
(4分)
17.FECHD(3分)
18.(1)Cl K
(2)Cl2+KOH==KCl+KClO+H2O
(3)![]()
19(1)①⑥⑦⑤④②
(2)MnO2+4HCl==MnCl2+Cl2+2H2O 3Cl2+2Fe==2FeCl3
(3)防止空气中的水蒸气进入装置 吸收水分
吸收氯气中的氯化氢气体
20.合格