高一化学第一学期期中统考试卷
可能用到的相对原子质量:C、12 H、1 O、16 N、14 S、32 Li、7
Na、23 K、39 Rb、86 Cs、133 Ca、40
一、选择题(每题只有一个选项符合题意2′×10 = 20′)
1、化学成为一门科学,始于( )
A、元素周期律的发现 B、分子原子学说的建立
C、结晶牛胰岛素的合成 D、《本草纲目》的编纂
2、下列操作正确的是( )
A、用10mL量简量取5.56mL稀盐酸
B、仰视量筒时读数比实际读数大
C、用托盘天平称量11.50g NaCl固体
D、在KClO3受热分解时加入CuO的作用是起催化作用
3、下列说法错误的是( )
A、Ba(OH)2・8H2O与NH4Cl的反应是吸热反应
B、高温下C 和 CO2的反应是吸热反应
C、燃料有足够的空气就能充分燃烧
D、放热反应的过程,可以看成是“贮存”在物质内部的能量转化为热能而被释放出来
4、下列说法不正确的是( ) 4、BD
A、碱金属单质的密度均小于1
B、锂不能保存在煤油中
C、碱金属的单质中,铯的熔点最低
D、碱金属元素的还原性随核电荷数增大而增强
5、在钠的焰色反应实验中,不需要的仪器或药品是( )29、C
A、铂丝棒 B、酒精灯 C、蓝色钴玻璃 D、稀盐酸
6、下列叙述中,正确的是( )
A、金属原子失电子越多,其还原性越强
B、难失去电子的物质,一定容易得到电子
C、某元素从化合态变为游离态时,该元素一定被还原
D、有单质参加或有单质生成的反应不一定是氧化还原反应
7、对Na+离子的性质叙述正确的是( )22、C
A、银白色 B、没有氧化性
C、只能被还原、不能被氧化 D、能与水反应并放出H2
8、将7.8gNa2O2投入到92.2g水中,所得溶液中溶质的质量分数( )
A.8.0% B.大于8.0% C.小于8.0% D.等于8.0%
9、下列关于氧化还原反应的叙述,正确的是( )
A.失去电子的反应是还原反应 B.失去电子的物质是还原剂
C.发生氧化反应的物质是氧化剂 D.作氧化剂的物质不能是还原剂
10、将金属钠长时间放置在空气中,最终的产物是( )23、B
A、NaOH B、Na2CO3 C、Na2CO3・10H2O D、Na2O2
二、选择题(每小题有1~2个选项符合题意 3′×10 = 30′)
11、下列电离方程式正确的是( )
A、 KOH = K+ + OH― B、H2O = H+ + OH―
C、NaHCO3 = Na+ + H+ + CO32- D、Ca(NO3)2 = Ca2+ + NO3―
12、过氧化钠和过量碳酸氢钠的混合物在密闭容器中充分加热后,容器中残留的固体物质是( ) 5、A
A、Na2CO3 B、NaHCO3和NaOH
C、Na2CO3和NaHCO3 D、Na2CO3和NaOH
13、下列关于金属钠及其化合物的叙述:①苛性钠又称纯碱 ②钠原子最外层电子只有1个电子,所以在化合物中钠只显正1价 ③过氧化钠中氧元素化合价为-1价 ④钠离子具有还原性,可以从水中还原出氢气 ⑤金属钠只有还原性,没有氧化性。上述叙述中正确的是( ) 6、C
A、①②③ B、③④⑤ C、②③⑤ D、①②⑤
14、下列叙述中正确的是 ( )
A、熔融态的Na2O能导电,因此Na2O是电解质
B、强电解质溶液的导电性不一定很强
C、SO2的水溶液能导电,因此SO2是电解质
D、强电解质在液化时都能导电
15、下列各物质能与Na、Na2O2、NaOH、NaHCO3、Na2CO3分别发生反应的是( )
A、硫酸溶液 B、CO2气体 C、盐酸 D、CaCl2溶液
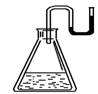 16、有下列物质:① NaOH固体;② 浓硫酸;③ 少量的Na2O2晶体;④ CaO固体。现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如右图所示状态,判断加入的物质可能是 ( )
16、有下列物质:① NaOH固体;② 浓硫酸;③ 少量的Na2O2晶体;④ CaO固体。现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如右图所示状态,判断加入的物质可能是 ( )
A、①②③④ B、①②④
C、②③④ D、①②③
17、在强酸性溶液中可发生如下反应:2Mn2++5R2O8x-+8H2O=16H++10RO42-+2MnO4-,这个反应可定性地检验Mn2+的存在.在反应中充当氧化剂的R2O8x-中x的值是( )
A、0 B、1 C、2 D、3
18、不能用离子方程式:H++OH - = H2O表示的反应是( )
A、KOH+CH3COOH=CH3COOK+H2O B、HCl+NaOH=NaCl+H2O
C、H2SO4+2NaOH=Na2SO4+2H2O D、Ba(OH)2+ H2SO4= BaSO4↓+2H2O
19、 下列各组离子,在碱性溶液中能大量共存,且溶液为无色透明的离子组是( )
A、K+、MnO4-、Cl-、SO42- B、Na+、Ba2+、NO3-、Cl-
C、Na+、H+、 NO3-、SO42- D、Ca2+、Cu2+、NO3-、Cl-
20、等质量的下列物质分别与足量的盐酸反应,放出二氧化碳气体最多的是
( )
A、Ca(HCO3)2 B、NaHCO3 B、Na2CO3 D、CaCO3
三、填空题(41′)
21(6′)、写出下列各物质的化学式:
苏打 小苏打 烧碱
22(14′)、右图中,A是单质,B的焰色反应呈黄色。判断A、B、C、D的化学式:
A B C D
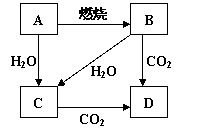 写出下列转化的化学方程式为:
写出下列转化的化学方程式为:
(1)A→B
(2)B→D
(3)A→C
该反应电子转移数目为
(4)B→C(请写出该反应的离子方程式)
5、 A:Na B:Na2O2 C:NaOH D:Na2CO3
23(12′)、为除去下列括号内的杂质,请在后面的横线上填上所需试剂的名称,并写出有关反应的离子方程式:
(1)NaHCO3 溶液(Na2CO3): , 。
(2)NaCl溶液(NaOH): , 。
(3)Na2SO4溶液(NaHCO3): , 。
24(9′)、如下图有5瓶无色溶液,按下述步骤可一一鉴别出来,请在括号内按要求填写。
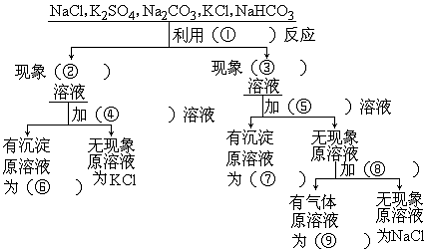
① ② ③ ④ ⑤
⑥ ⑦ ⑧ ⑨
1、(3)加热 2NaHCO3![]() Na2CO3+CO2↑H2O。 (1)H2O和CO2,CO32-+H2O+CO2===2HCO3-。 (2)HCl,H++OH-===H2O。 (4)H2SO4,HCO3-+H+===H2O+CO2↑。
Na2CO3+CO2↑H2O。 (1)H2O和CO2,CO32-+H2O+CO2===2HCO3-。 (2)HCl,H++OH-===H2O。 (4)H2SO4,HCO3-+H+===H2O+CO2↑。
四、计算题(9′)
25、3、 碱金属的氧化物和硝酸盐的化学式应该分别为R2O和RNO3,则有关反应式为:R2O+2HNO3=2RNO3+H2O,依此可以计算。
答案:相对原子质量(原子量)为132.85,应该是铯某碱金属的过氧化物11g与足量的CO2完全作用后,固体质量增加2.8g,
试判断此碱金属相对原子质量,并确定是什么金属。
高一化学第一学期期中统考
参考答案
一.选择题(每题只有一个选项符合题意,每小题2分,共20分)
| 题 号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答 案 | B | D | C | A | C | D | C | B | B | B |
二.选择题(每题有1~2个选项符合题意,每小题3分,共30分)
| 题 号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答 案 | A | A | C | AB | AC | A | C | AD | B | A |
三、填空题(41′)
21(6′)、
Na2CO3 NaHCO3 NaOH
22(14′)、
A 、Na B、Na2O2 C 、NaOH D、 Na2CO3
(1) 2Na+ O2 Na2O2
(2) 2Na2O2 +2CO2 = 2Na2CO3 + O2
(3) 2Na + 2H2O = 2NaOH + H2 ↑ ; 2e-
(4) 2Na2O2 + 2H2O =4Na++ 4OH-+O2↑ 5、 A:Na B:Na2O2 C:NaOH D:Na2CO3
化学方程式略去
23(12′)、
(1) 二氧化碳 ,CO2 + CO32- + H2O = 2HCO3-
(2) 盐酸 , OH- + H+ = H2O
(3) 硫酸 , HCO3- +H+ = CO2↑ + H2O
24(9′)
①、焰色反应 ②、紫色 ③ 、黄色 ④ 、BaCl2溶液
⑤、CaCl2溶液 ⑥ 、K2SO4溶液 ⑦、Na2CO3溶液 ⑧ 、盐酸
⑨、NaHCO3 溶液 (个别空格给其它合理答案也给分)
1、(3)加热 2NaHCO3![]() Na2CO3+CO2↑H2O。 (1)H2O和CO2,CO32-+H2O+CO2===2HCO3-。 (2)HCl,H++OH-===H2O。 (4)H2SO4,HCO3-+H+===H2O+CO2↑。
Na2CO3+CO2↑H2O。 (1)H2O和CO2,CO32-+H2O+CO2===2HCO3-。 (2)HCl,H++OH-===H2O。 (4)H2SO4,HCO3-+H+===H2O+CO2↑。
四、计算题(9′)
25、 3、 碱金属的氧化物和硝酸盐的化学式应该分别为R2O和RNO3,则有关反应式为:R2O+2HNO3=2RNO3+H2O,依此可以计算。
39 K