高一化学同步测试(8)―《物质的量浓度》
一、选择题(共10小题,每小题3分,共30分。只有1个正确答案)
1.在容量瓶上无需有标记的是 ( )
A.标线 B.温度 C.浓度 D.容量
2.某实验需要0.2 mol NaOH固体,用托盘天平称取固体时,天平读数(游码及砝码)将( )
A.等于8.0g B.等于8.00g C.大于8.0g D.等于0.2g
3.0.5L 1mol/L的FeCl3溶液与0.2L 1 mol/L的KCl溶液中,Cl-浓度比为 ( )
A.15∶2 B.1∶1 C.3∶1 D.1∶3
4.相对分子质量为M的某物质在室温下的溶解度为S g,此时测得饱和溶液的密度为
ρg・cm-3,则该饱和溶液的物质的量浓度是 ( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
5.将标准状况下的a L HCl(气)溶于1000g水中,得到的盐酸密度为b g/cm3,则该盐酸的
物质的量浓度是 ( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
6.NA为阿伏加德罗常数,下列关于0.2mol/L K2SO4溶液的正确说法是 ( )
A.500mL溶液中所含K+、SO42-总数为0.3NA
B.500mL溶液中含有0.1NA个K+离子
C.1L溶液中K+离子浓度是0.2mol/L
D.2L溶液中SO42-离子浓度是0.4mol/L
7.已知某KOH样品中含水7.62%,含K2CO3 2.23%,含KOH 90%。现将1.00g 样品加入
46.00mL 1.00mol/L的盐酸中,过量的酸用1.070mol/L KOH溶液中和。蒸发溶液,蒸发到
无水时,可得的固体的质量为 ( )
A.3.00g B.3.43g C.4.50g D.无法计算
8.取100mL 0.3mol/L和300mL 0.25mol/L的硫酸注入500mL容量瓶中,加水稀释至刻度
线,该混合溶液中H+的物质的量浓度是 ( )
A.0.21mol/L B.0.42mol/L C.0.56mol/L D.0.26mol/L
9.某Al2(SO4)3溶液V mL中含a g Al3+,取出V/4 mL溶液稀释成4V mL后,SO42-的物质
的量浓度为 ( )
A.125/54V mol・L-1 B.125a/36V mol・L-1
C.125a/18V mol・L-1 D.125a/V mol・L-1
10.将2.4mol某金属投入1.8L 2mol/L的某酸溶液中,恰好完全反应,并产生7.2g氢气,则
该金属和酸分别是 ( )
A.二价金属,二元酸 B.二价金属,三元酸
C.三价金属,二元酸 D.一价金属,一元酸
二、选择题(共5小题,每小题4分,共20分。每小题有1-2个正确答案)
11.配制一定体积、一定物质的量浓度的溶液,正确情况对实验结果产生偏低影响的是( )
A.容量瓶中原有少量蒸馏水 B.溶解所用的烧杯未洗涤
C.定容时仰视观察液面 D.定容时俯视观察液面
12.有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4mol/L,SO42-的
物质的量浓度为0.7mol/L,则此溶液中K+的物质的量浓度为 ( )
A.0.1mol/L B.0.15mol/L C.0.2mol/L D.0.25mol/L
13.在100g浓度为18mol/L、密度为ρ的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,
则加入水的体积 ( )
A.小于100mL B.等于100mL C.大于100mL D.等于![]()
14.用密度为1.32g/cm3的硫酸溶液逐滴滴入到BaCl2溶液中,直到沉淀恰好完全为止。已知
所生成的溶液的质量等于原BaCl2溶液的质量,则H2SO4溶液的浓度为 ( )
A.21.9% B.42.1% C.13.5mol/L D.5.67mol/L
15.质量为8.02g的铁片,放进1.0L 0.90mol/L的CuSO4溶液中,过一段时间取出洗净、干
燥后称量,质量变为8.66g 。若认为溶液的体积没有变化,则Cu2+的浓度变为( )
A.0.89mol/L B.0.82mol/L C.0.78mol/L D.0.6mol/L
三、填空题(35分)
16.(2分)1 mol/L的BaCl2溶液0.5L中,含有Ba2+的微粒是 个。
17.(4分)28g KOH配成250mL溶液,溶质的物质的量 ,溶液的物质的量的
浓度 。
18.(2分)配制800mL 63%的硝酸(密度1.4g/cm3)需浓度为96%的硝酸(密度1.5g/cm3)
mL。
19.(10分)100mL 1 mol・L-1Al2(SO4)3溶液中,含Al3+离子 mol, 个,
含SO42-离子 mol, 个,100mL 5 mol・L-1的蔗糖溶液中,含蔗糖分子
数与溶液中的 离子数目相同。
20.(2分)把500mL 4 mol/L H2SO4与1000mL 1 mol/L Na2SO4溶液混合,混合液总体积为
1500mL,则此混合液的物质的量的浓度 。
21.(14分)配制 1 mol/L的CuSO4溶液500m:,需胆矾 g;用 称出,把称
好的胆矾放入 里,用适量蒸馏水使它完全溶解,把制得的溶液小心地
中,用适量蒸馏水洗涤烧杯 2~3次,把每次的洗涤液都注入 中,
然后慢慢地加入蒸馏水到液面在刻度线下 ,改用 滴加蒸馏水到
刻度,使溶液的 最低点正好与刻度线 ;把瓶塞盖好,用
顶住瓶塞,另一只手 ,将瓶底倒转、摇匀。从配好的溶液中取出10mL,
此时溶液的物质的量浓度为 。
四、计算题
22.常温下,将150mL 22% NaNO3溶液加100g蒸馏水后,溶液中溶质的质量分数变为14%。
求原溶液的物质的量浓度。
23.现有200mL H2SO4和Na2SO4的混合溶液。其中,硫酸的物质的量浓度为1 mol/L,硫酸
钠的物质的量浓度为0.5mol/L。若要配制硫酸和硫酸钠的物质的量浓度分别为2mol/L
和0.2mol/L的溶液,应加入55.8%的硫酸溶液(密度为1.35g/cm3)多少毫升后再加蒸馏
水?
八、《物质的量浓度》
一、选择题:1.C 2.C 3.C 4.B 5.D 6.A 7.B 8.B 9.B 10.C
二、选择题:11.BC 12.C 13.A 14.BC 15.B
三、填空题:
16. ![]() 17.0.5mol; 2mol/L 18.490mL 19.0.2;
17.0.5mol; 2mol/L 18.490mL 19.0.2; ![]() ; 0.3mol;
; 0.3mol; ![]() ;阴阳离子总数
20.
;阴阳离子总数
20.![]()
![]()
21.125g; 天平; 烧杯; 转移至容量瓶; 玻璃棒;容量瓶; 2―3;食指;托住瓶底;1mol/L
四、计算题
22.解:设原溶液质量为x, ![]()
![]()
原来溶液的密度为:![]()
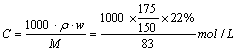 =
=![]()
23.解:加入H2SO4后,Na2SO4不变
![]()
![]()
此时H2SO4:![]() 需加入H2SO4
需加入H2SO4 ![]()
![]()
![]() 答:略。
答:略。