高一化学第一学期期中练习2
以下数据可供解题时参考:
原子量:Na—23 H—1 O—16 C—12 Cl—35.5 Ca—40
Ag—108 S—32 N—14 Cu—64 Fe—56 Ba—137
一、选择题 (每小题2分,共50分. 每小题只有一个正确选项)
1. 下列物质中只能做还原剂的是( )
A. H2S B. SO2 C. H2O D. Na
2. 下列各组溶液之间不能发生离子反应的是( )
A. NaCl和AgNO3 B. Na2CO3和硫酸
C. KNO3 和盐酸 D. Cu(OH)2和硝酸
3. 下列氧化还原反应在同一元素中进行的是
A . 2KClO3 =2K Cl+ 3O2 ↑ B. 2 H2O= H2O ↑+O2 ↑
C. 2Na 2O2 +2 H2O= 4Na OH+O2 ↑ D.2FeCl2 + Cl2 = 2FeCl3
4. 钠离子的性质是( )
A. 有强还原性 B. 无弱氧化性 C. 有碱性 D. 比钠原子稳定
5. 下列变化中需要加入还原剂才能实现的是( )
A. CaCO3 ![]() CO2
B. H+
CO2
B. H+ ![]() H2
H2
C. Fe2+ ![]() Fe3+ D.
SO4 2-
Fe3+ D.
SO4 2- ![]() Ba SO4
Ba SO4
6. 离子方程式两边应该是( )
A. 离子的个数相等 B. 正电荷与负电荷总数相等
C. 离子的正负电荷总数为零 D. 各元素原子个数相等
7. 在空气中因发生氧化还原反应而应密闭保存的( )
A. Na B. Na 2O C. Na2CO3 D. Na OH
8. 在反应2KMnO4 K2MnO4 +MnO2 +O2中 ,还原产物是( )
A. K2MnO4 B. MnO2 C. O2 D. KMnO4
9. 下列离子反应的离子方程式可以用H+ +OH- = H2O表示的( )
A. H2S+KOH
B. ![]()
C. 盐酸与氨水 D. Na H SO4 +Na OH
10.下列化合物中氮元素只具有还原性的是( )
A. KNO3 B. HNO3 C. NO D. NH3
11.在透明的酸性溶液中,能大量共存的离子组是( )
A. Mg 2+、CO3 2- 、HCO3 - 、NO3- B. Na+ 、CH3COO - 、HCO3 - 、Cl –
C.Fe3+ 、CO3 2- 、OH - 、SO4 2- D. NH4+ 、Cl –、Cu 2+ 、SO4 2-
12.依据 2 Fe2+ + Cl2 = 2Fe3+ +2Cl – 2Fe3+ +Cu = 2 Fe2+ +Cu 2+
Fe +Cu 2+ = Fe2+ +Cu
上述反应判断氧化剂的氧化性强弱顺序正确的是( )
A. Cl2 > Fe3+ > Cu 2+ B. Fe3+ > Cl2 > Cu 2+
C. Cu 2+ > Fe3+ > Cl2 D.Cl2 > Cu 2+ > Fe3+
13. 钠与水反应时的现象与下列性质无关的是( )
A. 钠的熔点低 B. 钠的密度大
C. 钠的硬度小 D. 钠有强还原性
14.下列各反应离子方程式错误的是( )
A. 金属钠与水反应 2Na+2 H2O=2 Na++2OH- +H2↑
B. 石灰水中通入二氧化碳Ca 2++2OH- + CO2 =Ca CO3 ↓+H2O
C. Na OH溶液与Cu SO4溶液反应2OH- + Cu 2+ =Cu (OH)2 ↓
D. 少量金属钠与 Cu SO4 溶液反应 2Na+ Cu 2+ =2 Na++ Cu
15. 金属钠与下列溶液反应时既有沉淀又有气体生成的是( )
A. ( NH4 )2SO4 B. NaHCO3 C. Ba Cl2 D. Cu SO4
16. 某溶液中只含有Na+ 、Al3+ 、Cl – 、SO42-四种离子,已知Na+ 、Al3+ 、
Cl –的个数比为3:2:1,则溶液中Al3+ 与SO42-个数比为( )
A. 1:2 B. 1:4 C. 3:4 D. 3:2
17. 已知aR2O72- +XM 2+ + 14H+ = bR3++ XM 3+ +c H2O反应则系数X是( )
A. 3 B. 4 C. 5 D. 6
18. 实验室中NaOH溶液应保存在( )
A.棕色瓶中 B. 带玻璃塞的玻璃试剂瓶中
C.带橡皮塞的玻璃试剂瓶中 D. 带胶头滴管的玻璃试剂瓶中
19. 在2Na 2O2+ 2CO2 = 2Na 2CO3 +O2↑反应中,有关说法正确的是( )
A. Na 2O2是 氧化剂,CO2 是还原剂
B. CO2是 氧化剂,Na 2O2是还原剂
C. Na 2O2 既是氧化剂又是还原剂
D.电子转移总数是4 e-
20. 过氧化钠7.8克溶于92.2克水中所得溶液的质量分数为( )
A. 8% B. 大于8% C. 小于 8% D. 7.8%
21. 把金属钠投入到下列溶液中溶液质量会减轻的是( )
A. HCl B. (NH4 )2SO4 C. Ca Cl2 D. Cu SO4
22. 为了除去括号中的杂质,所选用的试剂正确的是( )
A . H2( H2S) 选CuSO4 溶液 B. CO2(HCl) 选NaOH 溶液
C. Na2CO3(NaHCO3) 选CO2 D. NaOH(Na2CO3 ) 选CaCl2 溶液
23. 在反应3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O中,被还原的硝酸与未被还原的硝酸的分子个数比为( )
A. 1:2 B. 1:3 C. 3:1 D. 4:1
24.向下列饱和溶液中通入过量![]() 气体,没有析出晶体现象的是( )
气体,没有析出晶体现象的是( )
A. NaOH B. ![]() C.
C. ![]() D. Ca(OH)2
D. Ca(OH)2
25.某干燥粉末可能有Na2O、Na2O2 、Na2CO3 、Na2 SO4、NaHCO3 中的一种或几种组成。将该粉末与足量的盐酸反应有气体逸出。该气体通入足量NaOH 溶液后体积缩小(同温同压下测定)。若将原混合粉末在空气中加热,也有气体放出且剩余固体质量大于原混合粉末质量。以下判断正确的是 ( )
A. 粉末中一定含Na2O 、Na2O2 、NaHCO3
B粉末中一定不含有Na2CO3 、Na2 SO4
C. 粉末中一定不含有Na2O2 、Na2 SO4
D. 无法肯定粉末中是否含有Na2CO3 、Na2 SO4、Na2O2
二、填空题(共26分)
26. (6分) Na在空气中燃烧时是 色火焰,产生 色固体.该反应
的化学方程式为 ,
此产物可放在防毒面具中供人呼吸,其反应原理用化学方程式表示
.
27. (4分) 配平下列氧化还原方程式,用双线桥标明电子的转移方向和总数.
![]()
28.(5分) 一小块金属钠露置于空气中,可能有如下现象发生:
①生成白色粉末;②变暗;③生成白色固体;④发生潮解变成液体
(1) 这些现象的先后顺序为 ;
(2) 写出②和④现象所发生的反应的化学方程式
,
;
(3) 写出白色固体的化学式 ,
白色粉末的化学式 ;
29.(11分)已知在下列反应关系里,E为淡黄色固体,C、F为无色气体,D为无色液体,它们有如下关系:

(1)依据上述反应,分别写出下列物质的化学式:
C
D
E
(2)如果B中混有A,如何提纯 ,反应的化学方程式为
.
(3)如果B中混有G,如何用实验证明
,
反应的离子方程式为 ,
.
三、实验题(12分)
30.某同学在实验室设计钠和水反应的装置,并验证生成的气体是氢气.请回答:
(1) 金属钠为什么悬浮在水和煤油的界面上
.
(2) 关闭B处开关,当少量金属钠反应完毕后,
装置A处的现象是
,
装置B处的现象是
.
(3) 怎样验证生成的气体是氢气
.
(4) 请写出氢氧化钠溶液和二氧化碳反应的化学方程式
,
该同学要用上述装置验证此反应确能发生,你认为能否 (填写能与不能)
如果能,A处应加入 ,B处应加入 ,应如何操作
.
四、计算题(共12分)
31. (6分)向100g 4%的氢氧化钠溶液中缓缓通入二氧化碳4.4g,若反应充分发生,所得溶液的溶质是什么?求该溶液的质量分数.
32.(6分)纯碱中常含有少量氯化钠,请根据设计的实验测定纯碱的纯度.
方案一:


纯碱的质量分数为 .
方案二:
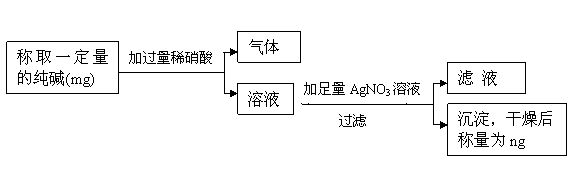

纯碱的质量分数为 .
参考答案及评分标准
一、选择题 (50分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | D | C | C | D | B | D | A | C | D |
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | D | D | A | C | D | D | A | D | C |
| 题号 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | ||
| 答案 | C | B | D | A | B | C | A |
二、 填空题 (26分)
26. (每空1分,方程式2分,共6分)
![]()
|
![]()
27. (共4分)
得到 2×3 e-
![]()
![]()
![]()
![]()
![]()
![]()
![]() 失去 3×2 e-
失去 3×2 e-
28. (每空1分,共5分)
(1) ② ④ ③ ①
(2) ![]()
(3) Na2CO3 10H2O Na2CO3
29. (每空1分,方程式2分,共11分)
|
![]() (2) 加热,
2NaHCO3 Na2CO3
+ CO2↑+ H2O
(2) 加热,
2NaHCO3 Na2CO3
+ CO2↑+ H2O
(3) 加过量 CaCl2 溶液后,过滤,向滤液中加 CuSO4 溶液
![]()
三、 实验题 (共12分)
30. (1) (1分) 钠的密度比水小,比煤油大
(2) (2分) 水面上升到球形漏斗中,液面上产生气体
(3) (2分) 打开B 处活塞点燃气体,气体燃烧呈淡蓝色火焰,生成的气体冷却后是水
(4) (5分) 2NaOH +CO2 = Na2CO3 +H2O 能, NaOH溶液,CO2气体,先向装置中加入NaOH溶液至B处充满,打开活塞通入CO2气体适量,关闭活塞,气体渐消失
四、 计算题 (共12分)
31.(6分) NaHCO3 溶液. 8.0% . 32.(6分) 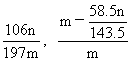
| 年级 | 高一 | 学科 | 化学 | 版本 | 期数 | ||||||||
| 内容标题 | 第一学期期中练习 高一化学 | ||||||||||||
| 分类索引号 | G.624.6 | 分类索引描述 | 考试试题与题解 | ||||||||||
| 主题词 | 北京十二中2003—2004学年度第一学期期中练习 高一化学 | 栏目名称 | 名校题库 | ||||||||||
| 供稿老师 | 审稿老师 | ||||||||||||
| 录入 | 一校 | 二校 | 审核 | ||||||||||