高一化学第二学期月考化学试卷
本试卷可能用到的数据:N:14 H:1 O:16 C:12 Cu:64 P:31
一、 选择题(每小题只有一个正确答案,每小题3分,共30分)
1. 三个容器中分别装有H2、O2、N2,当温度和密度完全相同时,三种气体压强(P)的大小关系正确的是 ( )
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
2、玻璃和水泥都要使用的原料: ( )
A、纯碱 B、石灰石 C、粘土 D、石英
3、下列保存物质的方法哪一种不对; ( )
A、少量白磷保存在水中 B、氢氟酸盛放在玻璃瓶中
C、金属钠保存在煤油中 D、氢氧化钠溶液、水玻璃盛放在带胶塞的玻瓶中
4、NO2与H2O反应时,NO2: ( )
A、只作氧化剂 B、既是氧化剂,又是还原剂
C、只作还原剂 D、既不是氧化剂,又不是还原剂
5、下列气体制取装置不相同的一组是: ( )
A、H2和CO2 B、CO2和SO2 C、NH3和O2 D、H2和H2S
6、下列各组离子中,可大量共存的是: ( )
A、Cu2+、Cl―、S2― 、H+ B、SO42― 、Na+ 、OH―、 HSO3―
C、K+ 、Cl― 、NO3― 、Cu2+ D、K+ 、ClO― 、Cl― 、S2―
7、NH4NO3和CO(NH2)2的混合物14克,含氮40%(质量分数),则该混合物中NH4NO3的质量为: ( )
A、5克 B、4克 C、2克 D、8克
8、与NH4+ 具有相同质子数和电子数的是: ( )
A、H2S B、H2O C、F― D、Na+
9、标准状况下,用一只充满NH3的烧瓶作喷泉实验,并使水充满整个烧瓶,烧瓶内氨水浓度为: ( )
A、0.045mol/L B、1mol/L C、0.45mol/L D、0.023mol/L
10、8NH3+3Cl2=6NH4Cl+N2反应中,如果有10.2克NH3被氧化,则反应用去的氯气在标准状况下的体积为: ( )
A、5.04升 B、6.72升 C、20.16升 D、40.32升
二、 择题(每小题有1-2个正确选项,每小题4分,共48分)
11、下列各组物质既不属于同素异形体,也不属于同位素的是: ( )
A、D2O、 H2O B、1H2、 2H2 C、红磷、 白磷 D、氧气 臭氧(O3)
12、有10毫升NO2和NO混合气的试管倒立于水槽中,充分作用后,试管内还有5毫升无色气体,则原混合物中NO2和NO的体积之比是: ( )
A、1:1 B、2:1 C、3:1 D、4:1
13、下列离子方程式正确的是: ( )
A、酸氢钙溶液中加盐酸:HCO3― +H+ =CO2↑+H2O
B、钠投入水中:2Na+2H2O=2Na+ +H2↑+2OH―
C、硫酸与氢氧化钡:SO42― +Ba2+ =BaSO4↓ D、硝酸与锌反应:Zn+2H+ =Zn2++H2↑
14、将1.5克Cu置于100毫升0.4mol/L的HNO3溶液中,被还原的HNO3与未被还原的HNO3的物质的量之比为; ( )
A、4:1 B、3:1 C、3:5 D、1:3
15、常温常压下等体积的4个容器中分别通入等物质的量的O2、NO、NH3、HCl、将这4个容器连通使气体充分混和后,温度和总体积不变,则各容器中的压强为原压强的: ( )
A、1倍 B、0.375倍 C、0.57倍 D、0.715倍
16、amolCu与含bmolHNO3的溶液恰好完全反应,则生成的NxOy气体的物质的量
A.一定是![]() mol
B.一定是
mol
B.一定是![]() mol
( )
mol
( )
C.一定是![]() mol
D.小于或等于
mol
D.小于或等于![]() mol
mol
17、了除去CO2中混有的少量SO2,最好选用: ( )
A、水 B、NaOH溶液 C、饱和Na2CO3溶液 D、饱和NaHCO3溶液
18、下列物质中,既能与NaOH溶液又能与盐酸反应的是: ( )
A、(NH4)2SO4 B、NH4NO3 C、NaHCO3 D、(NH4)2S
19、在标准状况下O2和CO2的混合气体共6.72L,其质量为11.4g,则混合气体中氧气的质量分数是 ( )
A、21% B、42% C、50% D、78%
20、鉴别NO2和溴蒸气的方法正确的是 ( )
A.用AgNO3溶液 B.用湿润的KI淀粉试纸 C.用NaOH溶液 D.用CCl4
21、砷是第四周期VA族元素,根据其在元素周期表中的位置推测,砷不可能具有的性质是: ( )
⑴砷原子比磷原子核外多一个电子层,共多8个电子
⑵砷酸H3AsO4是一种氧化性强酸 ⑶砷能表现出一定的金属性
⑷砷难与H2化合,砷化氢极不稳定 ⑸砷在通常状况下是固体
⑹可以有-3、+3、+5等多种化合物 ⑺As2O5对应水化物的酸性比H3PO4弱
A.⑴⑹ B.⑴⑵ C.⑷⑹⑺ D.⑶⑸
22、1.92g的Cu投入一定量的浓硝酸中,铜完全溶解,生成的气体颜色越来越浅,共收集到标准状况下672ml气体,将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积是 ( )
A.504ml B.168ml C.224ml D.336ml
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
|
|
|
|
|
|
|
|
|
|
|
|
| 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
|
|
|
|
|
|
|
|
|
|
|
|
选择题答案
第二卷(共72分)
三、填空题
23.(4分)氮族元素位于周期表的______族,其中非金属性最强的是________,其气
态氢化物的稳定性逐渐__ ___ ,其最高价氧化物的水化物的酸性逐渐
_______ ______.
24.(5分)检验NH3是否已充满试管的方法是___________________________________
欲除去NO中混有的NO2,所用的试剂是___________________ ,热的浓HNO3能使红
热的木炭燃烧是因为浓HNO3具有________ 性,其反应方程式为
25、(10分)有一白色固体A,分为等质量的甲、乙两份,甲份加热发生分解得到残余物C,同时产生能使石灰水浑浊的气体B;乙份加足量盐酸,也产生气体B,但产生气体的量是甲份的两倍,气体B跟淡黄色固体粉末D反应产生无味气体E,同时得到C,另取少量粉状A,进行焰色反应,火焰显黄色。
⑴写出B——E的化学式:B________ C_________ D_________ E__________
(2)写出A与盐酸反应的离子方程式: 。
26.(5分)以Cu和稀硝酸为主要原料制取硝酸铜,有下列两种途径
① Cu与稀硝酸反应 ② Cu先与氧气反应生成CuO,再与稀硝酸反应
试回答:选用_________途径好。因为(1)_________ ________ ____,
(2) ___________ _____
27.(10分)配平下列方程式,并填空:
(1)____P4+___KOH+____H2O — ____KH2PO2+____PH3
当有31g磷参加反应,则还原产物的质量是___________g
(2) ____HClO3+____P4+____H2O — ___ HCl+____H3PO4
当有31g磷参加反应,电子转移的个数为_____________
28.(10分)在一定条件下,某元素的氢化物x可完全分解为两种单质Y和z,若已知:
①反应前的x与反应后生成的z的物质的量之比n(x)∶n(z)=2∶3
②单质Y的分子为正四面体构型。
请填写下列空白。
⑴单质z是__________,单质Y是_________(填写名称或化学式)
⑵Y分子中共有__________个共价键,其键角为___________。
⑶x分解为Y和z的化学方程式为________ _______。
四、实验题(8分)
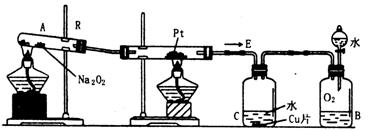 |
29.将某盐R盛在试管底部,进行如下实验,过了一段时间看到C中Cu片慢慢溶解,试回答下列问题:
⑴R的化学式可能是(填化学式)_______________;
⑵生成气体E的化学方程式________ ____________。
⑶B中的现象是___________ _______。
⑷铜片溶解的离子反应方程式_________ ______。
五、计算题
30.(8分)有一充满NO2和O2混合气体的试管倒置于水槽中一段时间后,水上升至试管容积的3/4处,求原混合气体中NO2和O2的体积比。
31.(12分)Cu、Cu2O与CuO组成的混合物加入100mL0.6mol/L的HNO3溶液,恰好使混合物完全溶解,同时收集到224mL(S.P.T)NO气体,求:
(1)写出Cu2O与稀HNO3反应的化学方程式:
(2)产物中硝酸铜的物质的量
(3)如原混合物中含0.01molCu,则Cu2O和CuO的物质的量分别为多少?
(4)若原混合物中Cu的物质的量为m,求其中Cu2O和CuO的物质的量及m的取值范围。
1C ,2B, 3B, 4B,5B,6C,7D,8D,9A,10C,
11AB,12C,13AB,14D,15B,16D,17D,18CD,19B,20AD,21B,22D。
23、VA,N,减弱,减弱。
24、潮湿的红色石蕊试纸置于试管口,若变蓝,说明已满;将混和气体通过水;氧化;
25、(1)B、CO2,C、Na2CO3 D、Na2O2 E、O2
(2)HCO3-+H+==CO2↑+H2O
26、② (1)制取等量的硝酸铜,②法所用的硝酸少
(2)②法不产生大气污染物
27、(1)1,3,3,3,1 (3分) ;8.5g(2分)
(2)3,10,18,10,12(3分);3.01*1024个
28、(1)H2,P4
(2)六,600
(3)4PH3==P4+6H2
29、(1)(NH4)2CO3或NH4HCO3
(2)4NH3+5O2==4NO+6H2O
(3)瓶子上方气体呈红棕色
(4)3Cu+8H++2NO3-==3Cu2++2NO+4H2O
30、VO2:VNO2==2:3或3:25
31、(1)略
(2)0.025
(3)Cu2O 0.005,CuO 0.005
(4) Cu2O 0.015-m CuOm-0.005 0.015>m>0