��ѧ
����2��һ��ѧ�����п����Ծ�
����ѧ��ѧ�����һ������
�����ֵ������ѡ���⣩�͵ڢ������ѡ���⣩�����֣���ֵ150�֣�ʱ��90���ӡ�
���������õ������ԭ��������H��1��O��16��S��32��P��31��Na��23��C��12��N��14
�ڢ����ѡ���� 72����
һ������ѡ���⣨ÿС��4�֣���40�֡�ÿС��ֻ��һ��ѡ��������⡣��
1��������Ne������ͬ�������͵������������ǣ� ���� ��
��A��H2�������� B��NH3���������� C��OH-���������� D��Na+
2�������������������һ�������·�����Ӧ���У� ���� ��
�������������£� ��Br2(g)�������£� ��KOH��Һ����Ũ���ᡡ ����������ȼ�����������Һ
��A���٢ܢݡ�������B���٢ڢۢܢݢޡ����� C���٢ڢݢ� ������ D���٢ڢ�
3�����й��ڵ�ص���������ȷ���� (����)
A�����շϾɵ�ص���Ҫԭ���Ƿ�ֹ����й����Ӻ�Ǧ���ؽ������Ӷ�ˮ����������Ⱦ
B��п�̸ɵ�ع���ʱ������ӦΪZn��2e- = Zn2+
C�����������ڳ�ʪ�Ŀ����к�����ʴ���⣬��������ӦΪFe��2e- = Fe2+
D��ԭ�����һ�ֽ���ѧ��ת��Ϊ���ܵ�װ��
4��ijԪ�صĶ��������ӵĺ�����18�����ӣ�������Ϊ37����Ԫ�ص�ԭ�Ӻ��е�������Ϊ������������
A��17�������������� B��19�������������� C��20�������������� D��22
5�����и����е����ʱȽϣ���ȷ���ǡ��� (������)
�� �����ԣ�HClO4>HBrO4>HIO4�������ڼ��ԣ�KOH>Ca(OH)2>Mg(OH)2
�� ���ȶ��ԣ�H2O>H2S>PH3�������� �ܻ�ԭ�ԣ�F�� >Cl�� >Br��
��A���٢ڢܡ����� B���ڢۢܡ����� C���٢ڢۡ����� D������ȷ
6�����з�Ӧ������������ԭ��Ӧ�����Ƿ��ȷ�Ӧ���ǡ�����������������
A���������ᷴӦ�������������������� B��NaOH��HCl��Ӧ
C��Ba(OH)2��8H2O��NH4Cl�ķ�Ӧ���� D��CaCO3���ȷֽ�ΪCaO��CO2
7�����и����л�Ϊͬλ�ص��ǡ���������
A��![]() ��
�� ![]() �� B��
�� B��![]() ��
��![]() ��C��
��C��![]() ��
��![]() ��D��
��D�� ![]() ��
��![]()
8��ijͬѧ��ʵ��������п��ϡ���ᷴӦ����������ʹ��Ӧ���ʼӿ죬�ɲ�ȡ�Ĵ�ʩ�ǡ����������� �������������������������������������������� ������������������������������������������������������
A����ϡ�����Ϊ98����Ũ���ᡡ�������������� B������Ƭ����пƬ����
C���μ�������CuSO4��Һ�������������������� D���ñ��Է�Ӧ�������ȴ
9��Cs��Ԫ�����ڱ��е�IA��Ԫ�أ����й���蘆���������ȷ���� (������)
A����ͬ����Ԫ���н�������ǿ��Ԫ�ء������� B���ڻ������гʣ�1��
C��������ˮ��Ӧ�ų����������������������� D��CsOH��������������
10�����к��зǼ��Լ������ӻ������ǣ���������
A��Na2O2���������� B��NH3������������ C��H2O2�������� D��KCl
����������ѡ���⣨ÿС��4�֣���32�֡�ÿС����һ��������ѡ��������⡣��
11�����й��ڻ�ѧ����������ȷ���ǣ������� ��
A�����ӻ����ﲻ���ܺ��й��ۼ�����������
B�� ���ۻ�������ܺ����Ӽ�
C�����ۻ�������һ���������Ӽ���������������
D���κ����ʲ������Ӽ���һ�����й��ۼ�
12�����й���ȼ��ȼ�յ�˵������ȷ���ǣ������� ��
A�����Ƿ��ȷ�Ӧ������Ҫ���Ⱦ��ܽ��С���������
B��Ӧͨ���ʵ������Ŀ���
C������ȼ��ȼ��ǰҪ����
D��Һ��ȼ��ȼ��ʱ������״���
13�����������ԭ��ص��ǡ��������� (������ )����������������������
A. Cu��Cu��ϡ���ᡡ�������������� B. Zn��ʯī��ϡ����
C. Cu��Zn���ƾ������������������� D. Zn��Cu����֭
14����һ���¶��£�A2(g)
+ B2(g)![]() 2AB(g)�ﵽƽ��ı�־�ǡ� ��������
2AB(g)�ﵽƽ��ı�־�ǡ� ��������
A��A2 ��B2��AB��Ũ��֮��Ϊ1:1:2
B����λʱ�������� 2mol AB, ͬʱ����1mol A2
C����λʱ���ڼ���1mol B2��ͬʱ����1mol AB
D��A2 ��B2��AB��Ũ�Ȳ��ٱ仯
15��ijԪ��ԭ�ӵ������ֻ��2�����ӣ����Ԫ�ء�����(������)
A��һ��IIA��Ԫ�� ������������ ����B�������ǽ���Ԫ��
C��һ����������Ԫ�ء������� D�������ǽ���Ԫ�أ�Ҳ�����Ƿǽ���Ԫ��
16��ͬ�����X��Y��Z����Ԫ�أ���֪������������Ӧ��ˮ����ļ���ǿ��˳��ΪX(OH)2>Y(OH)2>Z(OH)2�������и��ж���ȷ���ǣ�����������
A��ԭ�Ӱ뾶��X<Y<Z���������������� B�����ʵĽ����ԣ�X>Y>Z
C���������ᷴӦ�ľ��ҳ̶�X>Y>Z���� D��ԭ��������X<Y<Z
17������A +3B= 2C + D�ķ�Ӧ��˵�����»�ѧ��Ӧ���ʵı�ʾ�У���Ӧ���������ǣ�������
A��V(B)=0.8mol/( L��s)�������� B.��V(A)=0.8mol/( L��s)
C.��V(C)=0.6mol/( L��s)�������� D.��V(D)=0.6mol/( L��s)
18����A��B��C��D�Ŀ����Ƭ����������ʵ�飺��A��B�õ���������ͬʱ����ϡH2SO4��Һ�У�A��Ϊ������ ��C��D�õ���������ͬʱ����ϡH2SO4��Һ�У�������D���� C ������ A��C�õ���������ͬʱ����ϡH2SO4��Һ�У�C�������������ݣ� ��B��D�õ���������ͬʱ����ϡH2SO4��Һ�У�D������������Ӧ���ݴ��ж����ֽ����Ļ��˳���ǡ������������������������������������������������� �������� ��
A��A> B > C > D������������������ B��A > C > D > B��
C��C > A > D > B������������������ D��C > B > D > A
�ڢ������ѡ���� ��78����
�������������2С�⣬��21�֣�
19��(10��)�±���Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���Ԫ�ط��Ż�ѧʽ��ջش��������⣺
| ���� �� �� ���� | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| �� | �� | �� | ||||||
| �� | �� | �� | �� | �� | �� | �� | ||
| �� | �� | �� |
��1������ЩԪ���У�����õĽ���Ԫ��������������������õķǽ���Ԫ�������� ��
��2����ѧ��������õ�Ԫ��������������������ԭ�ӵ�ԭ�ӽṹʾ��ͼΪ��������
��3��Ԫ�ص�����������Ӧ��ˮ������������ǿ������������������������ ��������ǿ���������� ���� �������Ե����������������������������� ��
��4�����Ӱ뾶�������� �� �����>������<������=�� ��
��5���õ���ʽ��ʾ������γɵĻ�������γɹ��̣�
������������������������������������������������������������������������������
![]() 20����11�֣���ͼΪ���ڱ��е�һ���֡���֪A��B��C��D��Ϊ������Ԫ�أ�A��Dԭ������֮����C��ԭ��������1 .5����
20����11�֣���ͼΪ���ڱ��е�һ���֡���֪A��B��C��D��Ϊ������Ԫ�أ�A��Dԭ������֮����C��ԭ��������1 .5����
�� д��A��B��C��DԪ�ط��ţ�
A_______��B_______��C_______��D_______��
�� A��B��C��D����̬�⻯����ȶ�����(д��ѧʽ)_______���������� ��
��A��D��Ԫ�ص���̬�⻯�����Ӧ�Ļ�ѧ����ʽΪ��______������������������ ������Ϊ_______�������������� ������Ϊ_______������(����ӡ��������ۡ�)���û���������ڴ��ڵĻ�ѧ���������������������������� ��������Ӽ����������ۼ�����
��д�����е���ʽ��
C����̬�⻯���������������� ��A�ĵ�����������������������
 �ġ����������2С�⣬��19�֣�
�ġ����������2С�⣬��19�֣�
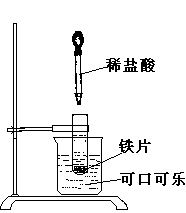
21����9�֣���ͼ��ʾ�����Թܷ���ʢ���¿�ƿ����ؿɿڿ������ϵ��ձ��У��Թܿ�ʼ���뼸С��FeƬ�����õιܵ���5mL�������Թ��С��Իش��������⣺
��1���ձ��й۲쵽��������_______________________�������������� __��
��2���������������ԭ����________________��________________�������������������� _____��
��3��д���йص����ӷ���ʽ��________________________________��
��4����ʵ����֪�����ɲ����������________���������������=������Ƭ���������������
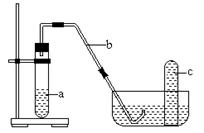 22����10�֣�������ͼ��ʾ��װ�ý���ʵ�飺
22����10�֣�������ͼ��ʾ��װ�ý���ʵ�飺
��1���ڼ���������Ժ����Թ�a�м���10mL6mol/L
ϡHNO3��1gCuƬ�������������ܵ���Ƥ�������Թܿڡ���д�����Թ�a���п��ܷ����ķ�Ӧ�Ļ�ѧ����ʽ��
�������������������� ��������������������������������
��2��ʵ������г�����ʼʱ��Ӧ���ʻ���������ӿ죬����������������������
�������������������������������������� ,��Ӧ����һ��ʱ���������������ԭ������������������������������������ ��
��3�����Ͽ���Ƶ�NO���ɲ�ȡ�Ĵ�ʩ�ǣ��� ��
A���ȡ�����B��ʹ��ͭ�ۡ��� C ������ˮ������ D������Ũ����
�塢���������2С�⣬��23�֣�
23����11�֣�һ��ԭ��ص��ܷ�ӦΪZn+Cu2+=Zn2++Cu������ѡ���Ϻ��Լ�������һ�����ϸ÷�Ӧ��ԭ���װ�ã�����ͼ��������ķ����У�ͼ��������缫���ϵ����������ش���������⣺
 ��1�����õ������Һ��д��ѧʽ������������
��1�����õ������Һ��д��ѧʽ������������
��2��д���缫��Ӧʽ��
����������������������������������������
����������������������������������������
��3��д����ʵ���п��ܳ��ֵ�����
��������������������������������������������
��������������������������������������������
24����12�֣���֤���ڱ���Ԫ�����ʵĵݱ���ɣ�
ʵ��һ���Ե�������Ϊ����֤��ͬһ������Ԫ�صĽ����Դ�������������
ʵ������Եڢ�A��Ϊ����֤��ͬһ������Ԫ�صķǽ����Դ�������������
����±��ģ�I����ѡ��ʵ�鷽�����ӣ�II����ѡ����Ӧ��ʵ���������¶�Ӧ����������ı����У�һһ��Ӧ�����Բ���������
| ʵ�鷽����I�� | ʵ������II�� |
| �ٽ�һС������Ʒ�����з�̪����ˮ�� | A ��Һ�²���Ϻ�ɫ |
| ����NaOH��Һ�е����̪ | B ��Ӧ��ʮ�־��ң����ɿ�ȼ������ |
| ����KI��Һ�����ε�����ˮ�� CCl4���� | C�۳�С����ˮ���Ĵ��ζ�����Һ��� |
| �ܽ���ĥ���þ������2mol/L�������� | D ��Һ�²�ʳȻ�ɫ |
| ����պ��Ũ��ˮ��պ��Ũ����IJ����ӽ� | E������ɫ��״�������̶���ʧ |
| ����ĥ���þ��������з�̪�ķ�ˮ�� | F���ҷ�Ӧ�����ɴ�����ȼ������ |
| ����Al2(SO4)3��Һ����ε���NaOH��Һ | G �д������̲��� |
| ����NaBr��Һ�����ε�����ˮ�� CCl4�� | H �п�ȼ�������������Һ��dz�� |
| �ὫС���Ʒ���MgCl2��Һ�� | I������ɫ�Ĺ������ |
| �⽫��ĥ�����Ƭ����2mol/L������ | J��Һ��� |
| �𰸱� | ʵ��һ ��֤��ͬ����Ԫ�صĽ����Դ����������μ����� | ʵ��� ��֤��ͬ����Ԫ�صķǽ����Դ����������μ����� | ||||||||
| I | ||||||||||
| II | ||||||||||
�������������2С�⣬��15�֣�
![]() 25����һ���¶��£���2mol�������4mol ���� B����2L�ܱ������У��������·�Ӧ��A��g��+ 3B��g������ 2C��g����2s ����40%��Aת��ΪC����ֱ���2s�ڵĦ�(B)�ͦ�(C)����6�֣�
25����һ���¶��£���2mol�������4mol ���� B����2L�ܱ������У��������·�Ӧ��A��g��+ 3B��g������ 2C��g����2s ����40%��Aת��ΪC����ֱ���2s�ڵĦ�(B)�ͦ�(C)����6�֣�
26������A��B��C����Ԫ�أ�Bԭ����������A��A��B��ԭ����֮��Ϊ27��������֮��Ϊ5��0.9 g����C��������������÷ų�1.12L��������״������������C�����Ȼ��C��������Ϊ14����ش��������⣻
��1��A���������� ��B������������ ��4�֣�
��2��д���Ƴ�C�Ĺ��̡���3�֣� ��3��ȷ��C�����ڱ��е�λ�á���2�֣�