高一化学月考卷(45分钟)
班级 姓名 学号 得分
一、选择题(每小题只有一个正确选项,把正确答案填在答卷的表格中,共60分):
1、人类使用材料的增多和变化,标志着人类文明的进步,下列材料与化学制备无关的是
(A)铁器 (B)石器 (C)青铜器 (D)合成材料
2、下列物质属于电解质的是
A、液氯 B、食盐水 C、 烧碱 D、酒精
3、化学反应都伴随着能量的变化,通常表现为热量的变化,以下叙述正确的是
(A)对于吸热反应,由于吸收热量后反应体系的温度升高
(B)对于吸热反应,生成物的总能量,高于反应物的总能量
(C)对于放热反应,放出热量后反应体系的温度降低
 (D)对于放热反应,生成物的总能量高于反应物的总能量
(D)对于放热反应,生成物的总能量高于反应物的总能量
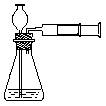
4、实验室实验时也可用推拉注射器活塞的方法检查右图中装置的气密性。当向外拉活塞时,如果装置气密性良好,可能观察到
(A)长颈漏斗下端口产生气泡 (B)瓶中液面明显上升
(C)长颈漏斗内的液面上升 (D)注射器内有液体
5、下列四种物质的溶液,其中一种与其它三种能发生离子反应,这种物质是
(A) H2SO4 (B) KOH (C) BaCl2 (D) Na2CO3
6.根据下列反应:(1)2Fe3++2I-![]() 2Fe2++I2(2)Br2+2Fe2+
2Fe2++I2(2)Br2+2Fe2+![]() 2Br-+2Fe3+判断离子的还原性由强到弱的顺序是( )
2Br-+2Fe3+判断离子的还原性由强到弱的顺序是( )
A.Br->Fe2+>I- B.I->Fe2+>Br-
C.Br->I->Fe2+ D.Fe2+>I->Br-
7、下列物质中含有自由移动的Cl-离子的是
(A) KClO3溶液 (B) MgCl2溶液 (C) 液态HCl (D) NaCl晶体
8、下列各组中的离子,能在溶液中大量共存的是:
A.Cu2+、Ba2+、Cl-、SO42- B.Na+、Fe3+、SO42-、OH-
C.H+、Na+、CO32-、NO3- D.K+、Na+、Cl-、OH-
9、黑火药的爆炸反应 :2KNO3+S+3 C == K2S +N2↑+3CO2↑ ;其中被氧化的元素是:
(A) N (B) S (C) O (D) C
10、1998年出现的全球温度大幅度升高,产生了显著的“厄尔尼诺”现象,干旱和暴雨灾难危害了许多地区。为了防止气候变暖的进一步恶化,联合国环境保护组织于1998年通过大会要求各国减少工业排放量的气体是
二氧化硫 (B)二氧化碳 (C)氮的氧化物 (D)氟里昂
11、下列粒子中,只有还原性的是
A.Br- B.H C.Mg2+ D.H2O
12、将5.36gNa2CO3・XH2O置于坩埚中加热至衡重时,质量减少3.24g,则x值为
A.10 B.3 C.9 D.6
13.在反应3Cl2+6KOH(浓)![]() KClO3+5KCl+3H2O中,氧化剂与还原剂的质量之比为( )
KClO3+5KCl+3H2O中,氧化剂与还原剂的质量之比为( )
A.5:1 B.4:1 C.1:5 D.1:4
14、下列反应中,水只作为氧化剂的是( )
A、CaO+H2O=Ca(OH)2 B.2Na2O2+2H2O=4NaOH+O2↑
C.C+H2O![]() CO+H2↑
D.Cl2+H2O=HCl+HClO
CO+H2↑
D.Cl2+H2O=HCl+HClO
15、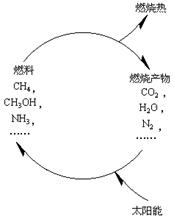 为了消除大气污染,节约燃料,缓解能源危机,化学家提出了利用太阳能促使燃料循环使用的构想图(见右图),该设想主要需解决的问题是( )
为了消除大气污染,节约燃料,缓解能源危机,化学家提出了利用太阳能促使燃料循环使用的构想图(见右图),该设想主要需解决的问题是( )
(A)使燃料充分燃烧,尽可能产生较多的燃烧热,充分利用燃料
(B)不使燃料不完全燃烧时产生的CO等有害气体进入大气,以消除污染
(C)利用太阳能使燃烧产物经化学反应重新组合,使之变成CH4、CH3OH、NH3等
(D)在太阳能的作用下燃料燃烧时不产生燃烧产物
二、填空题(40分)
16.有以下几种物质①干燥的食盐晶体 ②液态氯化氢 ③水银 ④蔗糖 ⑤冰醋酸 ⑥KNO3溶液 填空回答:(填序号)
(1)以上物质能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
(4)以上物质中溶于水后水溶液能导电的是
17.除去下表各溶液中含有的少量杂质(括号内)填写下表
| 各物质的溶液(杂质) | 除去杂质所需试剂 | 离子方程式 |
| NaOH(Na2CO3) | ||
| KCl(KHCO3) | ||
| Na2CO3(NaHCO3) |
18、有双线桥法表示下列反应的电子转移方向和数目,并指出氧化剂和还原剂、氧化产物和还原产物
(1)MnO2+4HCl=MnCl2+Cl2+2H2O;(2)2NaOH+Cl2=NaCl+NaClO+H2O
19、能用H++OH-=H2O离子方程式表示的化学反应,请举出5个不同的化学方程式。
20、把8g铁片放入100g硫酸铜溶液中,过一会儿取出该铁片,发现铁片经洗涤干燥后质量增重到了8.8g,试求有多少g还原剂参加了反应?(相对原子质量:Fe-56、Cu-64、O-16、H-1、S-32)
参考答案:
1、B 2、C 3、B 4、A 5、A 6、B 7、B 8、D 9、D 10、B 11、A 12、C 13、A 14、C 15、C
16、(1)③⑥(2)①②⑤(3)④(4)①②⑤⑥
17、Ca(OH)2或Ba(OH)2:Ca2++CO32―=CaCO3或Ba2++CO32―=BaCO3
HCl:2H++CO32-=H2O+CO2; NaOH:OH-+HCO32-=H2O+CO32-;
18、(1)转移2e-,氧化剂:MnO2、还原剂:HCl、氧化产物:Cl2、还原产物:MnCl2
(2)氧化剂、还原剂均为Cl2、氧化产物为NaClO
19、只要满足强酸与强碱反应生成可溶性盐和水均对,如HCl与NaOH、Ca(OH)2、Ba(OH)2等。
20、用差量法不难求得还原剂Fe的消耗质量是5。6g