高一化学五月月考试卷
注意点:1.本试卷总分100分,考试时间100分钟;请将答案答在答题卷中, 考试结束后只收答题卷。
2.可能用到的相对原子质量:H 1 C 12 O 16 Na 23 P 31 S 32 第Ⅰ卷(选择题 共54分)
一、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意。)
1.环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。塑料袋、废纸、旧橡胶制品等属于
A.有机物 B无机物 C盐类 D非金属单质
2.下列物质中互为同分异构体的是()
A淀粉和葡萄糖 B蔗糖和纤维素
C淀粉和纤维素 D果糖和葡萄糖
3.若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物:⑴CH3Cl, ⑵CH2Cl2,⑶CHCl3,⑷CCl4,其中正确的是
A.只有⑴ B.只有⑶ C.⑴⑵⑶的混合物 D.⑴⑵⑶⑷的混合物
4.下列属于加成反应的是()
- 己烯使酸性高锰酸钾溶液褪色。
- 将苯滴入溴水中,振荡后水层接近五色。
- 乙烯使溴水褪色。
- 甲烷与氯气混合光照一段时间后黄绿色消失。
5.下列各组混合物中,可以用分液漏斗分离的是
A.溴苯和水 B.乙酸和乙醇 C.酒精和水 D.溴苯和苯
6.除去乙酸乙酯中含有的乙酸,最好的处理方法是
A、蒸馏 B、用足量饱和碳酸钠溶液洗涤后分液
C、水洗后分液 D、用饱和食盐水洗涤后分液
7.下列各物质中,不能发生水解反应的是
A、果糖 B、油脂 C、纤维素 D、酶
8.下列变化属于物理变化的是
A、乙烯通入酸性高锰酸钾溶液褪色
B、浓硝酸滴到皮肤变黄
C.钙与酒精混合有气泡
D、苯滴入溴水中振荡后水层接近无色
9.在标准状况下,1L丙烷和2L乙烷的混和气体在80L空气中完全燃烧,生成的气体经干燥后,其体积为
A、 85L B、 75L C、73L D、 70L
10.下列说法正确的是
A、碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B、分子组成符合CnH2n+2的烃一定是烷烃
C、正戊烷分子中所有原子均在一条直线上
D、碳氢原子个数比为1:3的烃有2种
二、选择题(本题包括8小题,每小题3分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给3分,但只要选错一个该小题就为0分。)
11.钠与下列物质反应都能够产生氢气:①H2O;②CH3COOH;③CH3CH2OH。试推断这三种物质电离出H+的难易程度(从难到易的顺序)
A.①②③ B.②③① C.③①② D.②①③
12.某烷烃只能生成一种一氯化物,此烷烃的分子式可以是( )
A.CH4 B.C3H8 C、C4H10 D、C5H12 13.下列关于乙烯和聚乙烯的叙述不正确的是( )。
A、乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物
B、乙烯的化学性质比聚乙烯活泼
C、取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等D、乙烯和聚乙烯都能使溴水褪色
14.在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是( )。
A.CH4和C2H4 B.CH4和C2H6 C.C2H4和C2H6 D.C3H4和C3H6
15.1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,下列事实中它不能解释的有( )
A.苯不能使溴水褪色 B.苯能与H2发生加成反应
C.溴苯没有同分异构体 D.邻二溴苯只有一种结构
16.两种气态烃组成的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水,下列说法正确的是
A.混合气体中一定有甲烷 B.混合气体中一定是甲烷和乙烯
C.混合气体中一定没有乙烷 D.混合气体中一定有乙炔(CH≡CH)
17.下列各组物质中,不管它们以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳的量不变的是
A.乙炔(C2H2)和苯(C6H6) B.乙醇和丙醇(CH3CH2CH2OH)
C.乙醇和乙醚(C2H5OC2H5) D.甲醛( HCHO)和乙酸
18.甲醛(CH2O)、乙酸(C2H4O2)和丙醛(C3H6O)组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为
A 27% B 28% C 54% D 无法计算
请将选择题答案填在下表中:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 |
|
|
|
|
|
|
|
|
|
|
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
|
|
| 答案 |
|
|
|
|
|
|
|
|
|
|
第II卷(非选择题共46分)
三、填空题(共12分)
19.(5分)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。乙烯和氯化氢在一定条件下制得氯乙烷的化学反应方程式是(有机物用结构简式表示) ,该反应类型是 ,该反应的原子利用率为 ,决定氯乙烷能用于冷冻麻醉应急处理的具体理由是
20.(7分)某有机物的结构简式为HOOC―CH=CH―CH2OH。
⑴请你写出该有机物官能团的名称: 。
⑵验证该有机物中含有-COOH官能团常采用的方法是 ,
产生的现象为 。
四.实验题(8分)
21.(8分)糖尿病是“富贵病”,请你设计实验检验病人尿液中的葡萄糖,并与正常人作对比,设计要求:
⑴(4分)写出实验所用化学药品
⑵(4分)写出实验现象并作出结论。
五.推断题(12分)
22.已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
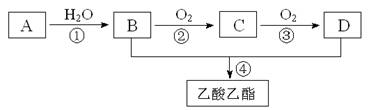
回答下列问题:
(1)写出A的电子式 。
(2)B、D分子中的官能团名称分别是 、 。
(3)写出下列反应的反应类型: ① ,② ,④ 。
(4)写出下列反应的化学方程式:
① ;
② ;
④ 。
六、计算题(本题包括2小题,共14分)
23.(6分) 0.1 mol某液态烷烃完全燃烧需要消耗0.8 mol 氧气,通过计算求该烷烃的化学式。写出符合该化学式的烃的结构简式。
24.(8分)有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
高一化学考试参考答案
一、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意。)
二、选择题(本题包括8小题,每小题3分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给3分,但只要选错一个该小题就为0分。)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | A | D | D | C | A | B | A | D | B | B |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
|
|
| 答案 | C | AD | D | A | AD | AC | AD | C |
|
|
三、填空题(共12分)
19.(5分)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。乙烯和氯化氢在一定条件下制得氯乙烷的化学反应方程式是(有机物用结构简式表示)
CH2=CH2 + HCl ![]() CH3CH2Cl
(2 分) ,该反应类型是 加成反应 (1分) ,该反应的原子利用率为 100% (1分) ,决定氯乙烷能用于冷冻麻醉应急处理的具体理由是
氯乙烷的沸点为12.27℃易液化吸收热量,使局部冷冻麻醉。(1分)
CH3CH2Cl
(2 分) ,该反应类型是 加成反应 (1分) ,该反应的原子利用率为 100% (1分) ,决定氯乙烷能用于冷冻麻醉应急处理的具体理由是
氯乙烷的沸点为12.27℃易液化吸收热量,使局部冷冻麻醉。(1分)
20.(7分)某有机物的结构简式为HOOC―CH=CH―CH2OH。
⑴请你写出该有机物官能团的名称:
羧基 、碳碳双键、羟基(3分) 。
⑵验证该有机物中含有-COOH官能团常采用的方法
是向有机物粉末(或溶液)中加入Na2CO3或石蕊溶液(其他合理答案都得分)(2分)
产生的现象为 有气泡产生 变红 (2分) 。
四.实验题(8分)
21.(8分)糖尿病是“富贵病”,请你设计实验检验病人尿液中的葡萄糖,并与正常人作对比,设计要求:
⑴(4分)写出实验所用化学药品
答案略
⑵(4分)写出实验现象并作出结论。
答案略
五.推断题(12分)
22.已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
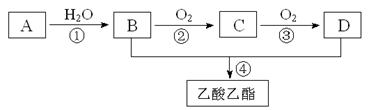
回答下列问题:
(1)写出A的电子式 略(1分) 。
(2)B、D分子中的官能团名称分别 羟基 (1分) 、 羧基(1分)。
(3)写出下列反应的反应类型:① 加成反应(1分)② 氧化反应(1分),④ 取代反应(1分)。
(4)写出下列反应的化学方程式:
①CH2=CH2+H2O![]() CH3CH2OH(2分)
CH3CH2OH(2分)
②2CH3CH2OH
+ O2 ![]() 2CH3CHO + 2H2O(2分)
2CH3CHO + 2H2O(2分)
④CH3COOH
+ CH3CH2OH![]() CH3COOC2H5 + H2O(2分)
CH3COOC2H5 + H2O(2分)
六、计算题(本题包括2小题,共14分)![]()
23.(6分) 0.1 mol某液态烷烃完全燃烧需要消耗0.8 mol 氧气,通过计算求该烷烃的化学式。写出符合该化学式的烃的结构简式。
解:设烷烃的化学式为CnH2n+2
由题意知:![]() =
=![]() =8
=8
![]() =8
=8 ![]() 3n=15
3n=15 ![]() n=5
n=5
![]() 烷烃化学式为:C5H12 (3分)
烷烃化学式为:C5H12 (3分)
结构简式为:CH3CH2CH2CH2CH3 (CH3)2CHCH2CH3 (CH3)2C(CH3)2(3分)
24.(8分)有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少?(4分)
(2)通过计算确定该有机物的分子式。(4分)
解:(1)2.3gA中含H物质的量为:![]() =0.3mol
=0.3mol
由质量守恒定律可知:
m有机物 + mO2 = m(CO2) + m(CO) + m(CO)
2.3g+![]() ×32g/mol=2.2g + m(CO) + 2.7g
×32g/mol=2.2g + m(CO) + 2.7g
m(CO)=1.4g
2.3gA中含C物质的量为![]() +
+![]() = 0.1mol
= 0.1mol
(2)2.3g有机物质中含O物质的量![]() =0.05mol
=0.05mol
该有机物中C、H、O原子个数比为:2:6:1
化学式为:C2H6O