高一下学期期中考化学试题
可能用到的相对原子量:H—1 C—12 N—14 O—16 F—19 Na—23 S—32
Cl—35.5 Cu—64 K—39 Mn—55
第Ⅰ卷(共51分)
一、选择题(本题共18小题,每小题3分,共51分。每小题只有一个选项符合题意)
1.我国城市环境中的大气污染物主要是( )
A .CO、Cl2、N2、酸雨 B.HCl、O2、N2、 粉尘
C .SO2、NO2、CO、粉尘 D .NH3、CO2、NO、雾
2. 在下列四种溶液中,分别加入少量固体二氧化锰,能产生气体的是( ) A 3%H2O2溶液 B 1 mol/L NaOH溶液 C 1 mol/LKClO3溶液 D 1 mol/L盐酸
3.下列变化需要加入还原剂方能发生的是 ( )
A. ![]() →SO2 B. S2- → S C. SO2 → S D. SO3
→H2SO4
→SO2 B. S2- → S C. SO2 → S D. SO3
→H2SO4
4.下列灭火技能用于扑灭金属钠着火的是 ( )
A.干冰 B.黄沙 C.干粉(含NaHCO3) D.泡沫灭火剂
5、有关 1224Mg中“24”的叙述正确的是( )
A、它表示镁元素的原子相对质量为24
B、它表示镁元素的原子序数为24
C、它表示镁元素的一种同位素的质量数为24
D、它表示镁元素的一种同位素的原子量为24
6.下列反应中硫化氢不做还原剂的是 ( )
A. 2H2S+3O2=2H2O+2SO2↑ B. H2S+2FeCl3=2FeCl2+S↓+2HCl
C. H2S+I2=2HI+S↓ D. 4Ag+2H2S+O2=2Ag2S↓+2H2O
7、Na和Na+两种粒子中,不相同的是( )
①核内质子数 ②核外电子数 ③最外层电子数 ④核外电子层数
A、①② B、②③ C、③④ D、②③④
8、某元素X的气态氢化物的化学式为H2X,则X的最高价氧化物的水化物的化学式( )A、H2XO3 B、HXO3 C、H3XO4 D、H2XO4
9.用下列方法制取氧气:①KClO3与MnO2混合加热 ②Na2O2跟水反应 ③H2O2滴入MnO2粉末中 ④KMnO4受热分解⑤电解H2O。要制得相同质量的氧气,上述各反应中依编号顺序电子转移数目之比( )
A. 3∶2∶2∶4∶2 B. 1∶1∶1∶1∶1
C. 2∶1∶1∶2∶2 D. 1∶2∶1∶2∶2
10. A、B、C、是周表中相邻的三种元素,且相对原子质量逐渐增大,A和B同周期,B和C同主族,三种元素原子最外层电子数总和为17,核内质子数总和为31,A、B、C三种元素是( )
A、Mg AL B B、N O S C、Li Be Mg D、O F CL
11.下列物质可盛在钢瓶中的是( )
A氯水 B浓硫酸 C 浓盐酸 D蓝矾溶液
12.SO2和Cl2都具有漂白作用,若将等物质的量的两种气体混合, 再通入品红与BaCl2的混合溶液中,则可观察到 ( )
A. 溶液立即褪色且无沉淀 B.溶液慢慢褪色,无沉淀
C. 先褪色后恢复原色 ,出现沉淀 D. 溶液不褪色,出现沉淀
13. 北大富硒康中含有微量硒元素(Se)对人体有保健作用,已知硒与氧同主族,与钾同周期,下列有关硒元素的性质描述错误的是( )
A、硒既能溶于盐酸又能溶于烧碱溶液 B、硒的最高价氧化物的化学式为SeO3
C、硒的非金属性比溴弱 D、硒的气态氢化物的化学式为H2Se
14.向50 mL18 mol/L H2SO4溶液中加入足量的铜片并加热。充分反应后,被还原的H2SO4的物质的量为( )
A小于0.45 mol B等于0.45 mol
C 在0.45和0.90mol 之间 D 大于0.90mol
15. 与NH4+离子所含的质子数和电子数都相同的微粒是( )
A、H3O+ B、NH2- C、OH- D、Na+
16. 下列各组中互为同素异形体的是( )
A 35Cl2与37Cl2 B H2O2与 H2O C O与 O2- D O2与 O3
17. 下列各组物质的性质及粒子变化正确的是( )
A酸性:HClO4 >H2SO4>H2CO3>H3PO4 B稳定性:H2S>HCl>HI>HBr
C粒子半径:Br—>K+>S2->S D还原性:Na>S2->Cl—>F—
第Ⅰ卷答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | |||
| 答案 |
第Ⅱ卷(共49分)
二、填空题(本题包括5小题,共32分)
18.(5分) (1) 写出表示含有8个质子、10个中子的原子的化学符号:________。
(2)周期表示位于第8纵行的铁元素属于第________族。
(3)周期表中最活泼的非金属元素位于第_________纵行。
(4)所含元素超过18种的周期是第_________、_________周期。
19、(6分)(1)写三种与氖原子具有相同电子数的两种元素组成的离子符号:
________ __________ ___________
(2)写出四种与氩原子具有相同电子数的气态氢化物的分子式:
________ __________ ___________
20、(6分)
已知短周期的四种元素A、B、C、D形成的四种离子:A+、B2+、C-、D2-电子层结构相同,则四种元素的原子半径按小到大的顺序排列为_____________四种元素的原子序数按由大到小的顺序排列为___________________。
21.(6分)选用合适的试剂除杂括号内的为杂质
CO2 (SO2)__________________ SO2(HCl )___________________
Cl2(HCl)___________________
22. (9分)三位学生设计了下述三个方案,并都认为, 如果观察到的现象和自己设计的方案一致,即可确证试液中有![]() 。
。
方案甲:试液 ![]() 白色沉淀
白色沉淀 ![]() 沉淀不溶解
沉淀不溶解
方案乙:试液 ![]() 无沉淀
无沉淀 ![]() 白色沉淀
白色沉淀
方案丙:试液 ![]() 无沉淀
无沉淀 ![]() 白色沉淀
白色沉淀
试评价上述各种方案是否严密,并分别说明现由。
答:______________________________________________________________________;
_________________________________________________________________________;
_________________________________________________________________________。
三、实验题(共12分)
23. (12分)为验证木炭与浓硫酸反应生成的气体M含有CO2和SO2,可按下图进行实验。各装置中可供选择的试剂是:①澄清石灰水,②品红溶液,③酸性高锰酸钾溶液。判断各装置所盛试剂后,请回答:
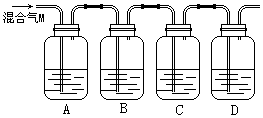
(1)A中所盛放的试剂是______(填写试剂序号),现象是 ,说明了
。
(2)B中所所盛放的试剂是_____,B装置的作用是 。
(3)C中所盛的试剂是_____,C装置的作用是 。
(4)D中所盛试剂应为 ,作用是 。
四.计算题
24.(5分)已知:KClO3+6HCl==KCl+3Cl2↑+3H2O,现用K35ClO3和H37Cl反应,求制
备的氯气的式量是多少?
答 案
一、选择题(本题共17小题,每小题3分,共51分;每小题只有一个选项符合题意)
第Ⅰ卷答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | A | C | B | C | D | D | D | C | B |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | |||
| 答案 | B | D | A | A | A | D | D |
二、填空题(共32分)
18.(5分)(1)![]() (2)Ⅷ (3)17(4)6 7
(2)Ⅷ (3)17(4)6 7
19、(6分)
(1)OH、H3O+、NH4+(或者只是10电子离子都对)
(2)PH3、H2S、HCl或SiH4(4个写3个都可以)(6╳1分)
20、(6分)(1)D2->C->A+>B2+(3分)
(2)B>A>C>D(3分)
21(共6分,每小题2分).NaHCO3溶液 NaHSO3溶液 饱和NaCl溶液
22(共9分). (3分)甲,不严密,因为不能排除仅含Ag+而不含SO42-的溶液的可能;
(3分)乙,严密,因为只有含SO42-的溶液才会出现此方案的现象;
(3分)丙,不严密,因为不能排除含SO32-而不含SO42-的溶液的可能。
三、实验题
23 (共12分,) . (1) (3分) ② 品红褪色 气体中含SO2
(2)(3分) ③ 除去SO2气体
(3)( 3分 ) ① 检验CO2气体的存在
(4)( 3分) 碱液(如NaOH溶液等) 吸收多余的尾气
四.计算题(5分)
24.3Cl2中有 35 Cl 1mol
37Cl 5mol
∴Mr(Cl2)=![]()