高一化学实验基本操作(二)]
1.用滴定管量取液体时能精确到
A.0.1 mL B.0.01 mL C.1 mL D.0.001 mL
2.使用容量瓶之前一定要
A.检查瓶塞处是否漏水 B.将容量瓶烘干
C.在瓶塞上涂凡士林,使其转动灵活 D.检查它的气密性
3.用容量瓶配制一定体积准确浓度的溶液时,容量瓶先用自来水洗,再用蒸馏水洗净后,还应注意
A.容量瓶必须干燥 B.要在室温下操作
C.要用欲配制溶液润洗2~3次 D.容量瓶瓶塞处应不漏水
4.量取10.00 mL盐酸应使用
A.酸式滴定管 B.10 mL量筒
C.碱式滴定管 D.100 mL量筒
5.下列仪器在使用前要先用试剂润洗两遍的是
A.容量瓶 B.滴定管 C.量筒 D.锥形瓶
6.下列仪器①集气瓶、②量筒、③烧杯、④表面皿、⑤蒸发皿、⑥容量瓶、⑦烧瓶,能用酒精灯加热的是
A.②③⑤ B.③⑥⑦ C.①③④ D.③⑤⑦
7.使用滴定管量取15.00 mL液体时:①若初读数时仰视,终读数时平视;②若初读数时俯视,终读数时平视;③若初读数时仰视,终读数时俯视,则所量取的液体体积将
①偏大 ②偏小 ③不变
A.①②③ B.①②① C.②①② D.②①③
8.下列量器的刻度表示正确的是
A.量筒的刻度值是由下向上增大,“0”刻度标记在下
B.250 mL容量瓶上一般刻有30℃,250 mL的标记
C.滴定管的刻度由上而下增大,“0”刻度在上
D.50 mL酸式滴定管的“50”刻度在活塞下端
9.某学生用量筒量取液体,量筒平稳且面对刻度线,起初仰视液面,读数为19 mL,倾出部分液体后,俯视液面,读数为11 mL,实际倾出液体的体积为
A.8 mL B.大于8 mL C.小于8 mL D.无法判断
10.下列实验操作中,所用仪器合理的是
A.用25 mL碱式滴定管量取14.80 mL NaOH溶液
B.用100 mL量筒量取5.2 mL盐酸
C.用托盘天平称取25.25 g氯化钠
D.用100 mL容量瓶配制50 mL一定浓度的盐酸
11.用一支25 mL的滴定管装好液体至“0”刻度,然后将液体全部放下,所得液体的体积是
A.25 mL B.小于25 mL C.大于25 mL D.无法判断
12.下面a~e是中学化学实验中常见的几种定量仪器:
a.量筒 b.容量瓶 c.滴定管 d.托盘天平e.温度计
(1)其中仪器上标明使用温度的是 ;
(2)能够用以精确量取液体体积的是 ;
(3)使用前必须检查是否漏水的有 。
13.在溶解或稀释时有明显的热量变化的溶液,就必须待溶液的温度 才能向容量瓶中转移。把烧杯中的溶液转移到容量瓶时,必须用 引流。容量瓶使用完毕,应 , (玻璃瓶塞与瓶口处垫张 以免瓶塞与瓶口 )。
14.(1)如图1―10Ⅰ表示 10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL。如果刻度A为4,量筒中液体的体积是 mL。
(2)如图1―10Ⅱ表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号) 。
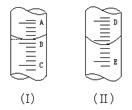
图1―10
A.是a mL B.是(50-a) mL
C.一定大于a mL D.一定大于(50-a) mL
1【答案】 B
2【答案】 A
3【答案】 BD
4【答案】 A
5【答案】 B
6【答案】 D
7【答案】 B
8【解析】 量筒的“0”刻度在下,但未标记出;容量瓶所标温度为20℃;滴定管的下端因不均匀而未标示刻度。
【答案】 C
9【解析】 量筒的刻度是自下而上逐渐增大。仰视读数为19 mL时,实际上量筒中液体体积小于19 mL;倾出部分液体后,俯视读数为11 mL,实际上量筒中剩余液体小于11 mL,则倾倒出的液体体积大于8 mL。
【答案】 B
10【解析】 量筒是粗略量取液体体积的量器,量取5.2 mL盐酸可用10 mL的量筒,用100 mL的量筒将产生较大的误差;托盘天平能称准到0.1 g;容量瓶是用来配制一定体积准确浓度的溶液,配制50 mL一定浓度的盐酸时需选用50 mL的容量瓶;滴定管能准确量取液体体积,可估读到0.01 mL。
【答案】 A
11。【答案】 C
12【答案】 (1)abc (2)c (3)bc
13【答案】 恢复到室温后 玻璃棒 洗净 晾干 纸条 粘连
14【解析】 该题主要考查学生观察、动手能力及理论联系实际能力。(1)量筒的小刻度在下,大刻度在上,所以刻度A为4,B为3,每一小格为0.2 mL,所以读数为3.2 mL。(2)由于液面处读数是a,液面至最低刻度(50 mL)的体积为(50-a) mL,又由于最低刻度下还有一段容积盛有液体,所以液体体积一定大于(50-a) mL。
【答案】 (1)3.2 (2)D