高一化学同步测试(2)―离子反应
说明:本卷答题时间60分钟,满分100分。
一、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意)
1.下列关于电解质的判断中,正确的观点是 ( )
A.在熔融状态下能导电的物质
B.在熔融或溶解状态下能导电的物质
C.在溶解或熔融状态下能导电的化合物
D.在熔融和溶液的状态下都能导电的化合物
2.下列物质的水溶液能导电,但其本身属于非电解质的是 ( )
A.液氯 B.干冰 C.酒精 D.硫酸钡
3.下列属于强电解质的是 ( )
① NaOH ② NH3・H2O ③ AgCl ④ 醋酸 ⑤NaHCO3
A.①②⑤ B.①③④
C.②③④ D.①③⑤
4.下列反应中是离子反应,但不是氧化还原反应的是 ( )
A.氯化钠溶液中滴入硝酸银溶液 B.金属钠在氯气中燃烧
C.铁片置于硫酸铜溶液中 D.金属钠放入水中生成氢氧化钠和氢气
5.对溶液中的离子反应有下列说法:①不可能是氧化还原反应.②只能是复分解反应③有可能是置换反应④不可能有分子参加,其中正确的是 ( )
A.①② B.只有③ C.②④ D.①④
6.下列四种物质的溶液,其中一种与其它三种能发生离子反应,这种物质是 ( )
A.H2SO4 B.KOH C.BaCl2 D.Na2CO3
7.在一定条件下,RO3n-和氟气可发生如下反应:RO3n-+F2+2OH-=RO4-+2F-+H2O。从而可知在RO3n-中,元素R的化合价是 ( )
A.+4 B.+5 C.+6 D.+7
8.BaCO3与稀硝酸反应,正确的离子方程式是 ( )
A.Ba2++ CO32-+2H+=Ba(NO3)2+ H2O+CO2↑
B.BaCO3+2H++2NO3-= Ba(NO3)2+ H2O+CO2↑
C.BaCO3+2H+= Ba2++ H2O+CO2↑
D.CO32-+2H+= H2O+CO2↑
9.已知某溶液中含有Na+、Ba2+、Fe3+三种阳离子,那么溶液中的阴离子可能是 ( )
A.SO42- B.Cl- C.OH- D.CO32-
10.能用H++OH-=H2O表示的化学方程式有 ( )
A.氢氧化钠溶液与醋酸反应 B.氢氧化铁与硫酸反应
C.氢氧化钡与硫酸反应 D.硫酸氢钠与氢氧化钠溶液反应
二、选择题(本题包括5小题,每小题4分,共20分。在每题给出的四个选项中,有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确给满分,但只要选错一个该小题就为0分)
11.有四位同学分别对四种溶液中所含的离子进行检测,所得结果如下,其中所得结果错误的是 ( )
A.K+、Na+、Cl-、NO3- B.OH-、CO32-、Cl-、K+
C.Ba2+、Na+、OH-、NO3- D.Cu2+、NO3-、OH-、Cl-
12.下列离子方程式书写正确的是
( )
A.饱 和 石 灰 水 跟 稀 硝 酸 反 应 Ca(OH)2+2H+=Ca2++2H2O
B.稀硫酸与锌反应:H2SO4+Zn=Zn2+ +SO42-+H2↑
C.碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O
D.小苏打溶于醋酸溶液:HCO3-+CH3COOH=CH3COO-+H2O+CO2↑
13.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是 ( )
A.Cu(OH)2与盐酸,Cu(OH)2与醋酸
B.BaCl2溶液与Na2SO4溶液,Ba(OH)2溶液与H2SO4溶液
C.NaHCO3溶液与盐酸,Na2CO3溶液与盐酸
D.石灰石与硝酸反应,石灰石与盐酸
14.下列各组溶液,不用其他试剂,就可以将它们区别开来的是 ( )
A.盐酸,氢氧化钠,碳酸钠,硫酸钠
B.盐酸,氢氧化钠,酚酞,硫酸铜
C.氢氧化钠,硫酸镁,碳酸钠,硫酸氢钠
D.氯化钡,硫酸钠,氯化钙,硝酸钙
15.在xR2++yH++O2=m R3++nH2O的离子方程式中,对系数m和R3+的判断正确的是( )
A.m=4,R3+是氧化产物 B.m=y,R3+是氧化产物
C.m=2,R3+是还原产物 D.m=y,R3+是还原产物
三、填空、简答和计算(共8个小题,满分50分)
16.(6分)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化KNO3 ⑨纯水。请回答下列问题(用序号):
(1)以上物质中能导电的是__________
(2)以上物质属于电解质的是_____________
(3)以上物质中属于非电解质的是______________
(4)以上物质中属于弱电解质的是______________
17.(8分)写出下列反应的离子方程式
(1)向澄清石灰水中加硝酸 ________________;
(2)用石灰石与盐酸反应制取二氧化碳 _________________;
(3)锌粉加入硫酸氢钠溶液中 _______________;
(4)向Na2CO3溶液中滴加几滴稀盐酸: _________________。
18.(6分)H2S的水溶液不易导电,写出2FeCl3+H2S=2FeCl2+S↓+2HCl的离子方程式是
, 是氧化剂,
是还原剂, 是氧化产物, 是还原产物。
19.(4分) 有下列离子:K+,Mg2+,Ba2+,Cu2+,Na+,CO32-,SO42-,OH-, NO3-,Cl-等按其在溶液中大量共存的原则,将上述离子等分成二组(要求每组不少于两种阳离子和两种阴离子),则两组分别是甲OH-___________________________ 乙 _____________________
20.(4分)有A、B、C、D四种可溶性离子化合物,它们的阳离子是Ag+、Na+、Mg2+、Cu2+,阴离子是Cl-、OH-、NO3-、SO42-(每种离子只能用一次)
现将溶液两两混合,记录现象如下:
A+B→白色沉淀 ;2B+ D→白色沉淀;C+D→蓝色沉淀
则A、B、C、D的化学式分别是_________、__________、___________、_________。
21.(8分)某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO3-六种离子。
(1)甲厂的废水明显呈碱性,故甲厂废水所含的三种离子是_________、_________、_________。
(2)乙厂的废水中含有另外三种离子。如果加一定量________(选填:活性炭、硫酸亚铁、硫酸亚铁、铁粉),可能回收其中的金属__________(填元素符号)
(3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的__________(填入离子符号)转化为沉淀。经过滤后的废水主要含_________________,可用来浇灌农田。
22.(8分)现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠四瓶失去标签的溶液,分别编号为A、B、C、D。每次取少量溶液两两混合,所观察到现象记录在下表中(“-”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)
(1)据此推断这四瓶溶液中的溶质分别为
A ; B ; C ; D ;
(2)写出上述实验过程中有关物质间反应的离子方程式:
| A | B | C | D | |
| A | ↑ | ↓ | - | |
| B | ↑ | ↓ | ↑ | |
| C | ↓ | ↓ | - | |
| D | - | ↑ | - |
A+B ;
C+D ;
A+C ;
23.(6分)一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物
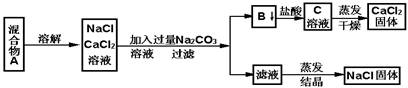
填空和回答下列问题
(1)B物质是 (写化学式)
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有毛病,这一步的正确设计方案应是 。
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 。
参考答案
一、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | B | D | A | B | A | B | C | B | D |
二、选择题
| 题号 | 11 | 12 | 13 | 14 | 15 |
| 答案 | D | D | D | BC | AB |
16.(1) ④ ⑧(2) ①③⑤⑧⑨(3)⑥⑦(4)③⑨
17.(1)OH-+2H+= H2O (2)CaCO3+2H+=Ca2++CO2↑+H2O.
(3)Zn+2H+=Zn2++H2↑(4) CO32-+H+=HCO3-
18.2Fe3++H2S==2Fe2++ S↓+ 2H+
FeCl3; H2S; S; FeCl2
19.甲:OH- 、Ba2+,K+,Na+, Cl- - 乙:Mg2+,Cu2+,SO42-, CO32- ,NO3-,
20.A、AgNO3 B、MgCl2 C、CuSO4 D、NaOH
21.(1)OH-、 K+、Cl-;(2)铁粉,Ag (3)Ag+和Cl-、Fe3+和OH-;NO3- K+。
22.(1) 稀硫酸、碳酸钠、氢氧化钡、稀盐酸
(2)CO32++2H+=CO2↑+H2O ;OH-+H+= H2O;Ba2++ 2OH-+2H++ SO42-= BaSO4↓+2H2O
23. (1)CaCO3 (2)加入适量盐酸至不产生气体 (3)A