2.下列物质中,可做光导纤维重要原料的有
A.石灰石
B.玻璃
C.二氧化硅
D.硅酸钠
3.SiO2+3C![]() SiC+2CO反应中,还原剂与氧化剂物质的量之比为
SiC+2CO反应中,还原剂与氧化剂物质的量之比为
A.3:5
B.5:3
C.1:2
D.2:1
5.生石灰中往往含有杂质碳酸钙和二氧化硅,检验是否存在这两种杂质最好选用
A.水
B.盐酸
C.硫酸
D.烧碱溶液
6.人类已知的化合物,种类最多的是
A.第ⅡA族元素的化合物
B.第ⅢA族元素的化合物
C.第ⅣA族元素的化合物
D.第ⅤA族元素的化合物
9.在标准状况下,将CO2和CO的混和气体(密度为![]() )充满一盛有足量Na2O2的密闭容器中(容积为22.4L),用间断的电火花引发至充分反应,反应完成后,对容器里存在的物质的叙述正确的是
)充满一盛有足量Na2O2的密闭容器中(容积为22.4L),用间断的电火花引发至充分反应,反应完成后,对容器里存在的物质的叙述正确的是
A.存在0.5mol CO
B.存在0.125mol O2
C.存在0.25mol Na2CO3
D.存在0.5mol Na2CO3
10.下列各组物质均属于硅酸盐工业产品的是
A.陶瓷、水泥
B.单晶硅、玻璃
C.普钙、漂白粉
D.石英玻璃、石膏
11.可以肯定溶液中大量存在![]() 的理由是
的理由是
A.加入AgNO3溶液有白色沉淀产生
B.加入酸有无色无味气体产生
C.加入CaCl2溶液时有白色沉淀产生,再加稀盐酸沉淀溶解,产生可使澄清
石灰水变浑浊的无色无味气体
D.加入Ba(OH) 2溶液有白色沉淀产生,再加稀盐酸,反应现象如C所述
12.分析某硅酸盐得如下结果:SiO2
45.7%、Al2O3
38.41%、K2O 12.1%、H2O 4.42%,该盐的化学式为
A.![]()
B.![]()
C.![]()
D.![]()
13.不另加任何试剂就可以将:①Na2SiO3;②Na2SO4;③CaCl2;④KCl;⑤Ba(NO3)2五种溶液鉴别出来,其鉴别检出的顺序是
A.③④⑤①②
B.③①⑤②④
C.①③④②⑤
D.③②①④⑤
14.为了干燥CO2并除去混有的少量SO2,混和气应依次通过
A.碱石灰,浓H2SO4
B.烧碱,浓H2SO4
C.饱和小苏打溶液,浓H2SO4
D.碳酸钠溶液,浓H2SO4
15.某混和气体可能含有H2、CO、CO2、HCl、NH3和水蒸气中的两种或多种,当混和气体依次通过:①澄清石灰水(无浑浊现象);②氢氧化钡溶液(有浑浊现象);③浓H2SO4(无现象);④灼热氧化铜(变红);⑤无水硫酸铜(变蓝)(假设每一次吸收均完全)。对该混和气体成分判断正确的是
A.一定没有CO2,肯定有H2
B.一定有CO、CO2和水蒸气
C.一定有H2、CO2和HCl
D.可能有CO2、NH3和水蒸气
17.关于锗及其化合物的性质叙述中,错误的是
A.GeO2不溶于NaOH溶液
B.单质锗具有导电性
C.锗易与盐酸反应放出H2
D.GeO不稳定,易被氧化
18.下列几种情况都有白色沉淀物质生成,其生成物的化学成分相同的是
①块状纯碱久置于空气中生成的白色粉末
②盛澄清石灰水的烧杯内壁附着的白色物质
③生石灰久置于空气中生成的白色物质
④Na2SiO3水溶液置于敞口容器中,溶液中出现的白色浑浊
A.①④
B.②③
C.①②
D.③④
19.能够解释CO2比SiO2的熔、沸点低的原因是
A.C―O键能大于Si―O键能
B.C―O键能小于Si―O键能
C.破坏CO2晶体只需克服分子间作用力,破坏SiO2晶体要破坏Si―O共价键
D.以上说法均不对
20.有一碱性溶液250mL,它可能是NaOH、Na2CO3、NaHCO3中的一种或两种。若加入足量的盐酸,产生的挥发性气体用Ba(OH)2溶液吸收,可得14.775g的白色沉淀物,另取同样体积该碱性溶液,恰能使浓度为0.625mol/L的NaOH溶液100mL完全反应,该碱溶液的可能组成是
A.NaOH、Na2CO3
B.NaHCO3、Na2CO3
C.只含NaHCO3
D.只含Na2CO3
二.填空题
21.BGO是我国研制的一种闪烁晶体材料,曾用于诺贝尔奖获得者丁肇中的著名实验,它是锗酸铋的简称。若知:①在BGO中,锗处于其最高价态,②在BGO中,铋的价态与铋跟氯形成某种共价氯化物时所呈的价态相同,在此氯化物中铋具有最外层8电子稳定结构,③BGO可看成是由锗和铋两种元素的氧化物所形成的复杂氧化物,且在BGO晶体的化学式中,这两种氧化物所含氧的总质量相同。请填空:
①锗和铋的元素符号分别是
和
。
②BGO晶体的化学式是
。
③BGO晶体中所含铋氧化物的化学式是
。
22.实验室用右图的装置将CO2和CO进行分离和干燥。已知A.b均为活塞,试回答
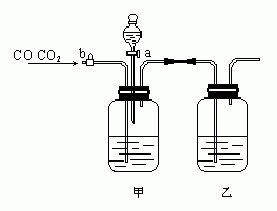
(1)甲瓶中装的是
溶液,乙瓶中装的是
溶液,分液漏斗中装的是
。
(2)当CO2与CO的混和气体通过该装置时,先分离得到的是 ,活塞操作是 ;然后得到 ,活塞操作是 。
23.在没有现成CO2气体发生器的情况下,请你选用如图中部分仪器装配成一个简易的、能随开随用的、随关随停的CO2气体发生装置。
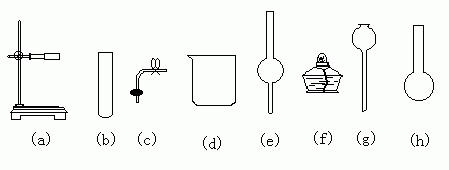
(1)应选用的仪器是(填入编号)
。
(2)若用上面已装配好的实验装置制取CO2气体,而实验室只有稀H2SO4、浓HNO3、水、块状纯碱、块状大理石。比较合理的方案,你认为应选的药品是
。
24.试用下图所列各装置设计一个实验来确证某无色气体中含有H2、CO2、SO2、HCl、CO五种气体。
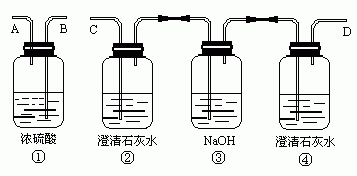
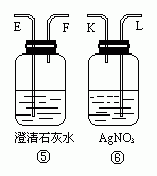
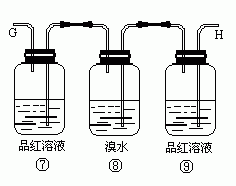
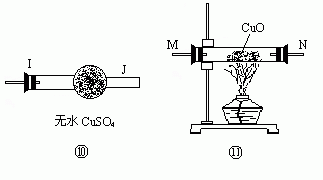
(1)若气体的流向是从左到右,连接上述装置的正确顺序是(填各装置玻璃接口的代码字母)
混和气→( )( )接( )( )接( )( )接( )( )接( )( )接( )( )接( )( )
(2)确认混合气体中有CO的实验现象是 ,确认混和气体中有H2的实验现象是 。
(3)装置瓶④的作用是
,装置瓶⑨的作用是
。
三.计算题
25.某白色固体由(NH4)2CO3与Na2CO3・nH2O组成,取混和物5.84g溶于足量盐酸中生成气体896mL(标况),另取5.84g该固体与足量Ca(OH)2共热,生成的气体通入25mL,1
mol/L的H2SO4溶液中,反应后用25 mL 0.5
mol/L NaOH溶液恰好中和过量的H2SO4。求混和物中的Na2CO3・nH2O中的n值。
26.现有氧化铜和炭粉的混和物A mol,将它在隔绝空气的条件下加热,反应完全后,冷却,得残留固体。
(1)写出可能发生反应的化学方程式。
(2)若氧化铜在混和物中物质的量的比值为x(0<x<1),问:x为何值时,残留固体为何种物质?写出残留固体的物质的量与x值之间的关系,将结果填入下表(不一定填满)
| x值 | 残留固体 | |
| 化学式 | 物质的量(mol) | |
| (a) |
|
|
| (b) |
|
|
| (c) |
|
|
| (d) |
|
|
| (e) |
|
|
参考答案
一.
1.AB 2.C 3.D 4.BD 5.B
6.C 7.AD 8.CD 9.B 10.A
11.C 12.D 13.B 14.C 15.C
16.BC 17.A 18.B 19.C 20.B
二.
21.(1)Ge Bi (2)![]() (3)Bi2O3
(3)Bi2O3
22.(1)NaOH,浓H2SO4,稀盐酸 (2)CO;打开b关闭a;CO2;打开a关闭b
23.(1)a,c,d,e (2)浓HNO3、水、块状大理石
24.(1)L、K、H、G、C、D、B、A、M、N、I、J、E、F
(2)瓶⑤中澄清石灰水变浑浊;⑩中无水CuSO4变蓝;
(3)确证CO2已被吸收完全,检验有无SO2
25.n=5
26.
(1)2CuO+C![]() CO2+2Cu
CO2+2Cu
CO2+C![]() 2CO
2CO
CO+CuO![]() Cu+CO2
Cu+CO2
(2)
| x值 | 残留固体 | |
| 化学式 | 物质的量(mol) | |
| (a) | Cu 、CuO |
|
| (b) | Cu |
|
| (c) | Cu |
|
| (d) | Cu |
|
| (e) | Cu、C |
|