�ٲ���ѧ��������ι�ҵ����Ԫ������
�����õ���ԭ������C-12��O-16��H-1��Si-28, Ca-40, Fe-56, Na-23
1������̫���ܵ����Ҫ�ߴ��ȵĹ裬��ҵ���ɴֹ��Ƹߴ��ȹ賣ͨ�����·�Ӧʵ�֣�
(1)Si(s)+3HCl(g)![]() SiHCl3(g)+H2(g)
SiHCl3(g)+H2(g)
(2)SiHCl3+H2![]() Si+3HCl
Si+3HCl
�������������µ�������Ӧ����������ȷ���ǣ�
��A��������Ӧ�����û���Ӧ ��������B����Ӧ(1)�Ǹ��ֽⷴӦ
��C��������Ӧ�ǿ��淴Ӧ ����������D��������Ӧ����������-��ԭ��Ӧ
2����֪�·��ֵ�114��Ԫ��X������ԭ�Ӻ�������������4�����ӣ������й�������ȷ����
A.X���ȶ�����̬�⻯��XH4���� B.X����۵������ﻯѧʽ��XO2
C.XΪ�ǽ���Ԫ�ء����������� D.X����۵��������Ӧ��ˮ����Ļ�ѧʽ��H4XO4
3������������ѧ�ҷ���һ���·��ӣ������п��ĵ���������״�ṹ����ѧʽΪC60������˵����ȷ����
A.C60��һ�����ͻ���������������������� B.C60��ʯī����̼��ͬ��������
C. C60�к����Ӽ��������������������������� D��C60��Ħ������Ϊ720
4���������ӷ���ʽ�в���ȷ����
A.̼�������Һ�����ᷴӦ�������� Ca(HCO3)2��2H��====Ca2����2H2O��2CO2��
B.�⻯����Һ��������ˮ��Ӧ��������2������Br2====��2��2Br��
C.��������Ͷ��ˮ�С������������� 2Na��2H2O====2Na����2OH����H2��
D.������ͨ���Ȼ�������Һ�С�������2F��2����C��2====2F��3����2C����
5�������ռ�Ӧѡ�õ�������
A.ʯӢ������������B.��ͨ��������������C.����������������� D.�մ�����
6�����ڡ�������ѧ��־���������й���ѧ���Զ�����̼Ϊ̼Դ��������Ϊ��ԭ������470�桢80 Mpa�ºϳɳ����ʯ��������Զ���塣����˵������ȷ���ǡ�����������
������ A. �ɶ�����̼�ϳɽ��ʯ�ǻ�ѧ�仯����B. ���ʯ��̼��һ��ͬλ��
������ C. �Ʊ�������������̼���ơ��������� D. ���ʯ��ֻ���зǼ��Թ��ۼ�
7�������£�����SiO2������Ӧ��������
A.�ռ�� ����������B.Ũ���ᡡ����������C.ˮ�������������� D.������
8������˵����ȷ����
A.��Ϊ�����к�SiO2���ʲ����Լ�ƿ����ʢװ��Һ
B.ˮ�����ڿ������ܱ���ǣ�ˮ�������ڿ����л�ˮ�ж���Ӳ��
C.�Ʊ����ά����Ҫԭ���Dz���
D.SiO2��������ǿ��Һ������������ᷴӦ������������������
9�����۲�����ȼ�յ���ɫ��ȼ�����ܿڵIJ��������
A.�Ʋ�������������B.�ز��������������� C.ʯӢ��������������D.ͭ��
10��Al2O3��2SiO2��2H2O��
A.����� ����������������������������B.�����������ˮ����
C.�������������������������������� D.������
11�����и����������ڴ��������
�� ˮ���� �� ˮ�� �� ��ͨ���� �� Ư�� ��.Na2CO3��10H2O �� ��ˮ �� Һ�� �ി��������
����A���� �ܡ���B���٢� �ߢࡡC���� �� �ޡ���D���� ��
12����������մɣ�Ҳ��һ���������ǽ������ϣ����������Ƴ��������������������������ϵ�
A.���µ����� ���� B.��ѧ���ԡ��������� C.��ѧ���� ���������� D.���﹦��
13�����в��ϵ���������;��˵������ȷ����
A.�������մɾ������ԣ�������������������
B.�������մ������Ҳ��״��ȣ�������������ͻ�
C.���ά����������ܺ�ǿ���Ƿdz��õ�ͨѶ����
D.�������Ӳ�ȸߣ��������������ĥ��
14��������Һ����ʢ���ڲ����Լ�ƿ�У���������ĥ�ڲ���������
A.��������Һ�� B.����ᡡ�� C.Ũ���� ��������D.�Ȼ�����Һ
15��.�մ��ѹ㷺Ӧ��������������У������������մ���Ʒ����
A.�����еľ�Ե�ɹܡ������������������� B.ʵ�����е�����
C.ʵ�����е��Թܡ��������������������� D.���������Ƶ�ש��
16�����й��ڲ��ϵ���������ȷ����
A.��ͳ�����������в����ŵ㣬���ʴྭ�����ȳ��
B.�������ǽ���������Ȼ�˷��˴�ͳ�����ϵ�ȱ�㣬��ǿ�ȱȽϲ�
C.���½ṹ���Ͼ����ܳ��ܸ��¡���������������ʴ��Ӳ�ȴ���ĥ���ܶ�С���ŵ�
D.�������ǽ�����������֮һ�Ǿ��е�ѧ����
17���������һ�־������﹦�ܵ��������ǽ������ϡ����������˹Ǻ���Ȼ�������ʺͽṹ������ǿ�������������Һ�в���ijЩ�����γ��¹ǡ����ڹ����ӺϽ�������ֽ⡢���ա������ȷ�Ӧ��ʵ�ֹ����ι̽�ϡ������ֲ����������Ҫ����������(����)�����γ��¹ǡ�
A.Ca2��������������
B.Cl����������������
C.Na��������������
D.SO![]()
18������ͭ���ǵ��������¿�ѧ�����źϳɵ�һ�����ʣ�Ȼ����ѧ�Ҿ���ط��֣��ҹ��س�����ٸ�õ�һ�����Ͼ�Ҳ�ǹ���ͭ������������ʵ�Ʋ���ڹ���ͭ����˵���������
A.������ˮ�������� B.������ˮ���������� C.���ڹ����Ρ����� D.���ڴ�����
19��.���Ƽ��ǿ������¿Ƽ������������Ŀ��Ⱦ۽�������Χ�ڣ����������������٣���DNA���ӽ��г��ͻ������������������εİ�֢���Ŵ����������������Ƽ���������ʶ��Ȼ��һ���²�Σ�1 nm ����
A.10��6 m������������ B.10��9 m������������ C.10��10 m���������� D.10��12 m
20������ͨ����������ͬ��ɵ��ǣ��� ��
A�� ��ѧ���������� B����ɫ�������� C���ֻ����������� D��ˮ������
21����һ��ɫ������ܺ���CO2��CO��H2O(g)��H2�е�һ�ֻ��֣����ν������´���(�ٶ�ÿ�δ�������Ӧ��ȫ)��
(1)ͨ����ʯ��ʱ�����������С��
(2)ͨ�����ȵ�����ͭʱ�������Ϊ��ɫ��
(3)ͨ����ɫ����ͭ��ĩʱ����ĩ��Ϊ��ɫ��
(4)ͨ������ʯ��ˮʱ����Һ����ǡ�
�ɴ˿���ȷ��ԭ��ɫ�����У�һ������
A. CO2��CO��H2O(g)��H2��������B. H2��CO��������C. H2��CO2������ D. H2��CO��H2O
22������������������ԭ���Ǫ�
��������������ˮ����Ӧ���ᡡ������
�£�����Ӧ��ˮ�����ǿ�����ǿ��
�����ã�����ǿ�Ӧֻ�����κ�ˮ�� �ģ����Ƿǽ���������
23����̼��Ԫ���У����ϵ�����С���������
A����ԭ�ӵ����������� B����̬�⻯����ȶ��ԡ�C�����ʵĻ�ԭ�ԡ�D��ԭ�Ӱ뾶
24�����������������������
A��̼�� ��B������ ��C������ ��D��������
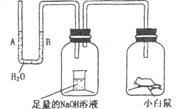 25�����ͼ�ʴ𣬾���Сʱ��u�ι�A��B������Һ�����������������(ʵ��װ����Ŀ�������ά��ʵ���ڼ�С������������ƿ���ܷ⣬����ˮ�������¶ȱ仯��ʵ������Ӱ��)����(����)
25�����ͼ�ʴ𣬾���Сʱ��u�ι�A��B������Һ�����������������(ʵ��װ����Ŀ�������ά��ʵ���ڼ�С������������ƿ���ܷ⣬����ˮ�������¶ȱ仯��ʵ������Ӱ��)����(����)
��A��A��������B���½���B��A��B�������½�
��C��A���½���B��������D��A��B����������
26�����������ҹ�������н�ֹ����ʹ�ú�Ǧ���ͣ�����Ҫԭ���ǡ���(����)
��A���������ȼ��Ч�ʡ��� B.�������ͳɱ���C������Ǧ��Ⱦ����������D.Ǧ��Դ��ȱ
27�����ơ�����ЧӦ�����ܶ���Ч�Ĵ�ʩ��(����)
A.����ú��ʯ�͵�ȼ�ա������� �� B.����ȫ���˿ڵļ�������
C.����ɭ��ֲ����������ľ�������� D.��ҵ��ú������Ȼ��
28�����и��������ڼ����������ܴ����������(����)
A.Na+��Cl-��Al3+��Ca2+�������� �� B.K+��HCO3-��CO32-��SiO32-
C.Na+��CO32-��SiO32-��AlO2-������ ��D.Ca2+��Cl-��SO42-��CO32-
29�����б仯������ͨ��һ����Ӧʵ�ֵ���(����)
A.Na2CO3��Na2SiO3���������� ���� B.Si��SiO2
C.SiO2��H2SiO3������������������ D.CuSO4��CuCl2
30����ȥSiO2�����л��е�CaCO3 ���巽����ȷ���ǣ��� ��
A.��ˮ���ˡ����� B.���ȡ��� C.�����ᡢ���ˡ��� D.��NaOH��Һ������
��������⣨22�֣�
31��6�֣���NaHCO3��Na2SiO3��K2SO4������Һ�У�
(1)ֻ�ܸ�H����Ӧ����__����_____����Ӧ�����ӷ���ʽΪ___���������������� ___��
(2)���ܸ�H����Ӧ�����ܸ�OH����Ӧ����___������������ ____����Ӧ�����ӷ���ʽ
____������������������ __����__���������������������� _____��
32��4�֣�������ʯ�Ļ�ѧʽΪKAlSi3Ox����x=�������������� ��������ʯд�����������ʽ������������������������������������ ��
33��2�֣�����Ȫˮһ��������ʯ�绯����ˮ�ܽ����п��ܲ������ɵġ��˴���ָ�ķ绯������ָ������ˮ��CO2ͬʱ���õĹ��̡�����س�ʯ(KAlSi3O8)�绯���ɸ����� ��Al2Si2O5(OH)4�� ���˷�Ӧ�����ӷ���ʽΪ��2KAlSi3O8��2CO2��7H2O====2K����2HCO![]() ��4H2SiO3��Al2Si2O5(OH)4�������Ӧ�ܹ�������ԭ��������������������������������
��
��4H2SiO3��Al2Si2O5(OH)4�������Ӧ�ܹ�������ԭ��������������������������������
��
34��6�֣�����̼��Ԫ���У��ǽ�������ǿ��Ԫ����_______����������ǿ��Ԫ����_______�����������뵼���Ԫ����_______����2�����ȶ���Ԫ������ ������̬�⻯�����ȶ�����_______�����������ˮ����������ǿ����_____ ___��
35(4��)���軯��(SiH4)�ڿ���������ȼ�����ݼ���ȼ�յĻ�ѧ����ʽ��д���軯����ȼ�Ļ�ѧ����ʽ�����������������������������������������˷�Ӧ�й軯�����������õ���ʧȥ�����ӣ���Ϊ��������������
����ʵ���⣨14�֣�
36��7�֣���A��B��C��D��E�������ʵ�ת����ϵ����ͼ
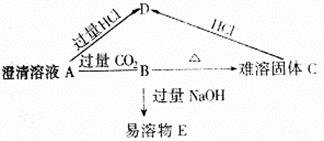
����֪AΪ��Ԫ�����������Ӻ�����18�����ӣ�д�������ʵĻ�ѧʽ��A_______��C_______��E_______��
(2)д�����������仯�����ӷ���ʽ
B��D_________________________��
A��B______________������������ _______��
37��7�֣�����ͼ��װʵ������о�CO�Ļ�ԭ�ԣ�
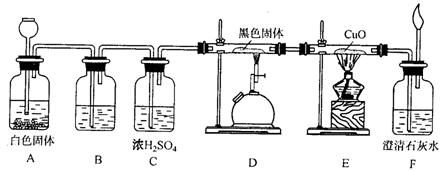
��д���пհף�
(1)��A�ij���©��Ӧ������Լ���______________(����)
A.ϡ���ᡡ����B.Ũ���ᡡ�� ������C.ϡ���ᡡ�� D.Ũ����
(2)װ��B�������˵��Լ���_______��__��
(3)װ��D�з�����Ӧ�Ļ�ѧ����ʽ��_____________________________________��
(4)װ��E�з�����������___________________________�������� __________
(5)������װ��C���ճ�ȥ������ˮ������������Ҫ��_________________________��
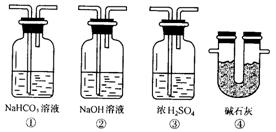
(6)������F��ʯ��ˮ����ǵ�����Ҳ��ȷ��CO���л�ԭ�ԣ�Ӧ��ͼ��װ��______________��______________֮��������ͼ����һ��װ��______________(����)��
�ġ������⣨4�֣�
38����9gSiO2�� 20gCaCO3������ڸ����¼��ȵ��������ٸı䡣�Լ��㣺��1������CO2�ڱ�״���µ��������2����Ӧ��Ĺ�̬���ʵ����ʵ�����
�ٲ���ѧ��������ι�ҵ����Ԫ����������
![]()
 һ��ѡ���⣨ÿС��2�֣�
һ��ѡ���⣨ÿС��2�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| �� | |||||||||||||||
| ��� | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| �� |
��������⣨22�֣�
31���������������� ��������������������������������������������
�������������� ���������������������� ��������������������������
32��X=�������� ������������������������������������������������
33����������������������������������������������������������������������
34������������ ������������������������ ����������������������
�� �������������������������������������� ������������������������
35������������������������������������������ ������������ �� ��������
����ʵ���⣨14�֣�
36���� A___ _�� ___��C_____���������������� __��E__���������� _____
�� B��D_________���������������������� ________________��
A��B______________�������������������������� _______��
37��(1) ______________
(2) _______ __��
(3) ________________������������������������ _____________________��
(4) _________________________���������� _ _�������� __________
(5) ________���������������������������������� _________________��
(6)װ��______________��______________֮������______________
�ġ������⣨4�֣�
38��
�ٲ���ѧ��������ι�ҵ����Ԫ������ο���
һ��ѡ���⣨ÿС��2�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| �� | A | B | B | A | C | B | A | B | C | C | D | D | A | A | C |
| ��� | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| �� | B | A | A | B | C | B | C | B | B | C | C | A | C | C | C |
��������⣨22�֣�
31����NaSiO3�� SiO32-+2H+ =H2SiO3 ����
�� NaHCO3 ����HCO3 - +H+=H2O+CO2 ������HCO3 - +OH-=CO32-+H2O��
32��X=����8������������K2O��Al2O3��6SiO2����
33����Ϊ̼������Ա�ԭ����ǿ���ɽ�ǿ�������ͨ�����ֽⷴӦ�Ƶý���������
34������ C���� �������� Pb�������������� ������ Si,Ge����
�� ������Pb��������������CH4������������ ��������H2CO3����
35���� SiH4+2O2==SiO2+2H2O�������� ���� ʧȥ������������ ��ԭ������
����ʵ���⣨14�֣�
36���� A___Ca(OH)2 _�� ___��C____CaCO3_����_��E__���� Na2CO3������ _____
�� B��D_______ HCO3 - +H+=H2O+CO2 ��__�� ___��
A��B________ OH_-+CO2 =��HCO3 -������_____��
37��(1)�� C �������������� (2)����NaHCO3��Һ��
(3)CO2+C![]() 2CO ������(4)��ɫ��ĩ��Ϊ��ɫ��
2CO ������(4)��ɫ��ĩ��Ϊ��ɫ��
(5)������ˮ����������ܷ���H2O+C![]() CO+H2����H2�ɻ�ԭCuO��
CO+H2����H2�ɻ�ԭCuO��
(6)D��E�������� ����
�ġ������⣨4�֣�
38��SiO2+CaCO3![]() CaSiO3+CO2������������
CaCO3
CaSiO3+CO2������������
CaCO3![]() CaO+CO2��
CaO+CO2��
����60g��100g���� 1mol�� 22.4L���������� 100g�� 1mol��22.4L
����9g��20g(����) 0.15mol 3.36L���������� 5g�� 0.05mol 1.12L
.����������5g
V(CO2)=4.48L�� n( �� )=0.2mol