高 一 化 学 实 验 专 题 复 习
基础部分
1、下列仪器不能用于加热的是 ( )
(A)容量瓶 (B)圆底烧瓶 (C)试管 (D)烧杯
2、下列气体不能用浓H2SO4干燥的是 ( )
(A)CO2 (B)CO (C)NH3 (D)SO2
3、要除去混在CO2气体中少量SO2,最好让气体通过 ( )
(A)Na2CO3溶液 (B)溴水 (C)NaOH溶液 (D)饱和NaHCO3溶液
4、下列实验操作中,正确的是 ( )
(A)稀释浓硫酸可先在量筒中加入一定体积水,再在不断搅拌下沿量筒壁慢慢加入浓硫酸
(B)过滤时,漏斗里的滤液应低于滤纸的边缘
(C)燃着的酒精灯不慎打翻,应立即用水灭火
(D)测定溶液的pH值时,应用玻棒蘸取待测液,直接滴在干燥的pH试纸上
5、某学生要提纯混有泥沙的食盐,他设计的主要操作有:溶解、过滤、蒸发。在这些操作中都需要使用的仪器是 ( )
(A)烧杯 (B)漏斗 (C)玻璃棒 (D)酒精灯
6、下列试纸在使用时不宜用水湿润的是 ( )
(A)蓝色石蕊试纸 (B)淀粉碘化钾试纸 (C)pH试纸 (D)红色石蕊试纸
7、不能用浓硫酸而只用碱石灰干燥的气体是 ( )
(A)H2 (B)H2S (C)Cl2 (D)NH3
8、下列物质在空气中久置,不会变质的是 ( )
(A)Ca(OH)2 (B)漂白粉 (C)氯化钾 (D)氢SO42-
9、下列仪器中,“0”刻度在上端的是 ( )
(A)量筒 (B)滴定管 (C)温度计 (D)容量瓶
10、在用氢氧化钠固体配制250ml 0.1mol/L NaOH溶液的过程中不需要的仪器是
(A)250ml容量瓶 (B)托盘天平 (C)胶头滴管 (D)烧瓶
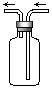 11、右图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是 ( )
11、右图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是 ( )
(A)NO (B) NO2
(C) CO (D)SO2
12、实验室进行NaCl液蒸发时,一般有以下操作过程
① 固定铁圈位置 ② 放置酒精灯 ③ 放上石棉网 ④ 放上蒸发皿
⑤加热搅拌 ⑥停止加热、余热蒸干其,正确的操作顺序为 ( )
(A) ①②③④⑤⑥ (B) ②①③④⑤⑥
(C) ②①④⑤⑥ (D) ②①③④⑤
13、对下列仪器回答问题:
①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗
(1) 对允许加热的仪器,加热时必须垫石棉网的有 (填序号)
(2) 使用时必须检查是否漏水的有 (填序号)
(3) 标有“0”刻度的有 (填序号)
14、如图装置中,若关闭活塞,则品红溶液无变化,石蕊试液变红,石灰水变浑浊.若打开活塞,则品红溶液褪色,石蕊试液变红,石灰水变浑浊.据此判断气体和广口瓶中盛放的物质是( )
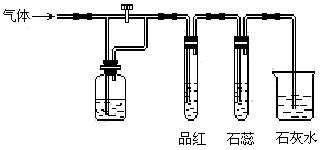
(A) H2S和浓H2SO4 (B)SO2和NaHCO3溶液
(C) Cl2和NaHCO3溶液 (D) Cl2和氯水
15、(1)下列实验操作中,正确的是__________。
A、称量固体药品时,将药品直接放在天平托盘上。
B、实验室用氯酸钾制氧气结束时,先从水槽中移出导气管,再熄灭酒精灯
C、先将pH试纸用蒸馏水润湿后,再测定溶液的pH
D、在量筒中稀释浓硫酸
E、金属锂保存在煤油中
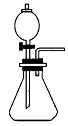 F、金属钠不慎燃烧立即用沙子覆盖
F、金属钠不慎燃烧立即用沙子覆盖
G、用100mL量筒量取2.50mL盐酸
16、右图是实验室制取气体的一种装置。
(1)这种制气装置在加入反应物前,应首先进行的实验操作是 。
(2)该装置可制取的气体 。
(写出物质的化学式)。
(3)若用上述装置制取O2,除了可选择二氧化锰和 (填物质名称),
还能选择 (填物质的化学式)和水。
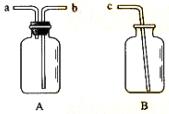
(4)若用排空气法收集H2,可选择下图中的A装置,收集时气体应从 口进气。(填“a”或“b”)。
若用排水法收集H2,可选择同时使用下图中的A和B两套装置,其操作是:在A中加满水,盖紧瓶塞,
。
综 合 部 分
17、(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ________________。
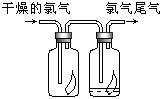 (2)为防止氯气尾气污染空气,根据氯水显酸性的性质,
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,
可用 溶液吸收多余的氯气,原理是(用化学方程
式表示)_________________________________。
根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得
漂白粉,漂白粉的有效成分是__________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
(3)据“北方网”报道,2004年4月15日至16日,位于重庆市江北区的天原化工总厂相继发生氯气泄漏和爆炸事故。截至记者发稿时,已有9人在事故中失踪死亡,3人受伤,15万人被紧急疏散。当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是 。
A.NaOH B.NaCl C. KBr D. Na2CO3
18、有一瓶澄清的溶液,其中可能含有NH4+ 、 K+ 、 Na+ 、 Mg2+、 Ba2+ 、 Al3+ 、Fe3+、Cl-、I-、 NO3-、CO32 -、S2- 、SO42- 、AlO2- 、SO32-、MnO4-, 取该溶液进行以下实验:
(1)、取PH试纸检验,溶液呈强酸性,可以排除 离子的存在。
(2)、取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色,可以排除 离子的存在。
(3)、另取出部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生,则又可以排除 离子的存在。
(4)、取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,证明 离子存在,又可排除 离子的存在。
(5)、将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定:该溶液中肯定存在的离子是
肯定不存在的离子是
还不能确定是否存在的离子是
19、 选用如下实验装置组合后完成用浓盐酸、二氧化锰共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉的实验。已知反应2Cl2+2Ca(OH)2==Ca(ClO)2+CaCl2+2H2O+Q温度稍高即发生副反应6Cl2+6Ca(OH)2==5CaCl2+Ca(ClO3)2+6H2O。
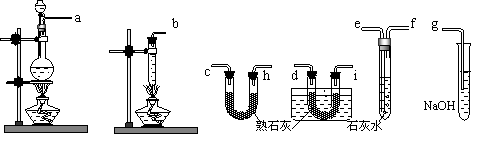 |
A B C D E F
⑴选用各装置的接口顺序为
⑵各装置所起的作用
⑶实验中若用12mol﹒L-1的浓盐酸100ml与足量的MnO2反应,最终生成Ca(ClO)2的物质
的量总是小于0.15mol,其可能的主要原因是
。(假定各步反应均无反应物损耗且无副反应发生)
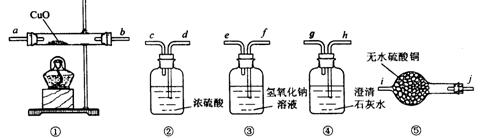
20、有一种由CO、CO2、H2、水蒸气四种气体组成的混合气体,要证明其中含有CO和 H2,可选用的仪器及药品如下:
(1)实验时,连接装置的顺序是 ;导管接口的顺序是 。
(2)装置①内发生反应的化学方程式是 。
 (3)证明混合气体中含有氢气的实验现象是
。
(3)证明混合气体中含有氢气的实验现象是
。
高 一 化 学 实 验 专 题 复 习
答案:
1.A 2.C 3.D 4.BD 5.C 6.C 7.D 8.C 9.B 10.D 11.BD 12.B
13.⑴②⑤ ⑵①⑦ ⑶③④ 14.B 15.BF
16.(1)检查装置的气密性
(2)CO2、NO、NO2选填两个,其他合理答案也给分(如NH3、HCl、H2S、SO2、Cl2 )
(3)双氧水(或过氧化氢水溶液)Na2O2 (4)a
用胶管连接b和c接口,由a导入H2气体,(水通过b和c排入B中)。
17.(1)潮湿有色布条褪色而干燥有色布条不褪色 (2)氢氧化钠(NaOH);2NaOH+Cl2=NaClO+NaCl+H2O ; Ca(ClO)2 ; C (3)D
18.(1). CO32 -、S2- 、AlO2- 、SO32- (2). Fe3+、NO3-、MnO4- (3) . Mg2+、Al3+
(4) . Ba2+ ; SO42- (5) .I- 、NH4+ 、Ba2+; Mg2+、Al3+ 、Fe3+、NO3-、CO32 -、S2- 、SO42- 、AlO2- 、SO32-、MnO4-; K+ 、Na+、Cl-
19.⑴adig (2)A制备Cl2 D制漂白粉 F尾气处理 (3) 随着反应进行浓盐酸浓度下降,到一定程度反应就不能进行
20.⑴ ③②①⑤④,f e d c a b j i h g
⑵ CO + CuO ═ Cu + CO2 ; H2 + CuO ═ Cu + H2O
⑶ ⑤中的无水硫酸铜变蓝