�ڶ��ڡ� �����ι�ҵ���
��ѧϰ�ص㪥
1.��ԭ�ϡ���Ӧ������ԭ������Ҫ�豸����Ҫ�ɷݼ����ʾ�����ȷ���Ƚ���ͨ��������ͨ ˮ�������������
2.�����εı�ʾ����������̬���ʵ��ص㪥
һ��ѡ���⪥
1.���в����ڹ����ι�ҵ��Ʒ����(����)��
A.ˮ�ࡡ����B.�մɡ��� C.ש�ߡ����� D.ʯӢ������
2.�������ʲ����ڹ����ε���(����)��
A.ճ��������B.���������� C.Al2(Si2O5)(OH)4���� D.Mg2SiO4��
3.����ˮ�����Ҫ�豸��(�� )��
A.��¯����B.��תҤ���� C.����¯���� D.�ϳ�����
4.ij��������Ʒ��п����������Ϊ58.6%���仯ѧ�������������ʽ�ɱ�ʾΪnZnO��SiO2����nֵ����(����)��
A.0.5���� B.1����C.2���� D.3��
5.����Ȼ����������Ȼ���е����ʣ����ڳ����±����ڿ����в���Ӳ������(����)��
A.ʯ��Ĩǽ���Ӳ��������ˮ������������ B.��ʯ���ˮ�����ģ�б�Ӳ��
C.ˮ����Ĩ�ڵ�Ƥ�ϲ��ñ�Ӳ�ʲ���״������D.ˮ��ɰ��������Ӳ��
6.��ˮ���м�ʯ���Ŀ����(����)��
A.����ˮ��Ļ�еǿ�ȡ������� B.����ˮ���Ӳ���ٶȪ�
C.����ˮ��ijɱ����������� D.����ˮ���ʹ�÷�Χ��
7.����ˮ�������˵�����������(���� )��
A.ˮ����ˮ�ͻᷢ��Ӳ����
B.ˮ���ǻ����瘟
C.ˮ��ɰ���ͻ������ض�Ҫ��ˮ�થ
D.ˮ���תҤ�����ϺͿ�����ú������������Ī�
8.��1 L 1.0mol/LNaOH��Һ���ձ�״̬��17.92 L CO2��������Һ��CO2-3�� HCO-3��Ħ��Ũ��֮��Լ��(����)��
A.1��3 ����B.2��1��������C.2��3������ D.3��2��
9.���������У���ȡʱ������ʯ��ʯ��ԭ�ϵ���(����)
A.���ᡡ�� B.ˮ�ࡡ�� C.���������� D.��ʯ��
10.��������ɳ���������ʯ�ҹ��ۺ������
��ˮ�ࡡ �ڲ����� �۴����� �ܻ������� ��һ�ֹ����β�Ʒ(���� )
A.�ٺ͢ܡ��� B.�ں͢ݡ��� C.�ۡ��� D.�ڪ�
11.����ˮ��Ͳ������������ܽ�������ι�ҵ��һ���ص��Ǫ�
���������ǹ����Σ��ڷ�Ӧ�� ���Ǹ��£��ۺ��й��������ԭ�ϣ��ܷ�Ӧԭ����һϵ�и��ӵ�����-��ѧ�仯(�� )��
A.�٢ۡ�����B.�٢ڢۡ��� C.�٢ڢۢܡ����� D.�٢ۢܪ�
12.����ͨ������Ҫ�ɷ�һ������(����)��
A.�ֻ��������� B.����ֽ���� C.�л��������� D.ˮ������
13.���۲�����ȼ�յ���ɫ��ȼ�����ܿڵIJ�����õ���(���� )��
A.�Ʋ���������B.�ز��������� C.ʯӢ����������D.ͭ�ܪ�
14.���������й̶��۵����(���� )��
A.����������B.ˮ�ࡡ������C.ˮ�������� D.Na2O��SiO2��
15.��ʵ�����ۻ�NaOH���壬����ѡ�õ������(���� )��
A.����������� B.����������� C.�����������D.ʯī�����
16.�ڲ�����ҵ��ˮ�ҵ�ж��õ���ԭ����(���� )��
A.�������B.ʯӢ������ C.ʯ��ʯ������D.ճ����
17.���������ȶ�����ǿ�������Ǫ�
��CaSiO3,��H2CO3,��CaCO3,��Ca(HCO3)2(����)��
A.�٢ڢۢܡ���B.�ڢܢۢ١� C.�٢ۢܢڡ���D.�٢ܢۢڪ�
18.���й��ڸֻ������������д������(����)��
A.���ijɷ���Na2SiO3��CaSiO3��SiO2�ۻ���һ�����õ������ʪ�
B.�ǰ���ͨ�������ڵ�¯����ȣ�ʹ֮������Ȼ������ȴ�ƵõĪ�
C.���Ǿ��пռ���״�ṹ��ԭ�Ӿ��壬Ӳ�Ⱥܴ��۵�Ҳ�ܸߪ�
D.���Ļ�еǿ�ȱ���ͨ������4��6�����������飬������ʱ�����û�м�������Ǫ�
��������⪥
19.������ͨˮ�����Ҫԭ����������������������.��ͨˮ�����Ҫ�ɷ���(д����)���������������������������������ǵĻ�ѧʽ�ֱ�������������������������������.ˮ�����Ҫ����������������
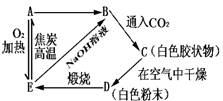 20.������ͼ������ʾ�ı仯��ϵ��д�������ʵĻ�ѧʽ.��
20.������ͼ������ʾ�ı仯��ϵ��д�������ʵĻ�ѧʽ.��
A������������B������������C������������D������������E����������.��
21.��ҵ��������ͨ��������Ҫԭ������������������������������������Ҫ�豸��������������Ҫԭ���ۻ���������Ҫ��ѧ��Ӧ��������������������.��ͨ�����ijɷ�����������.��
���������⪥
22.Ϊ���Ƽز������������ϣ�360���ص�ʯӢɰ��67.2���صĿ��Լغ�88.8���ص���ʯ�� .�ٶ���Щ���ϲ�������.��
(1)�������Ƶõļز����и����������������.��
(2)�����������ʽ��ʾ�ز��������.
23.SiO2��CaCO3�Ļ����26g���ڸ����¼��ȵ��������ٸı䣬��ȴ�������Ϊ17.2g. (1)д�����ܷ�����Ӧ�Ļ�ѧ����ʽ��
(2)������������ڱ�״��ʱ�������
(3)��ԭ������е�SiO2������.
�ڶ��ڡ������ι�ҵ���ο���
һ��1.D��2.B 3 .B��4.C 5.AC��6.B��7.B 8.A��9.B��10.B��11.C��12.A��13.C ��14.C 15.BC��16.C��17.C��18.C��
����19.ʯ��ʯ��ճ����������ơ��������ơ��������ơ�2CaO��SiO2��3CaO��SiO2O��3��3CaO��Al2O��3��ˮӲ�Ԫ�
20.Si��Na2SiO3��H4SiO4��H2SiO3��SiO2��
21.���ʯ��ʯ��ʯӢ��������¯����
| |
![]() SiO2+Na2CO3����������
Na2SiO3+CO2����
SiO2+Na2CO3����������
Na2SiO3+CO2����
���������� ����
![]() SiO2+CaCO3����������
CaSiO3+CO2����
SiO2+CaCO3����������
CaSiO3+CO2����
Na2SiO3��CaSiO3��SiO2��
����22.(1)K2O��11.7%��CaO����13.9%��SiO2�� 74.4%��
(2)K2O��2CaO��10SiO2��
��
![]() 23.(1)SiO2+CaCO3����������
CaSiO3+CO2����
23.(1)SiO2+CaCO3����������
CaSiO3+CO2����
��
![]() CaCO3����������
CaO+CO2��
CaCO3����������
CaO+CO2��
(2)4.48L
(3)6g