高一化学上学期期中考试试题
说明: 1.考试时间:90分钟 试卷满分:100分
2.本试卷可能用到的相对原子质量:H―1 Li―7 C―12 O―16
Na―23 K―39 Rb―85
第I卷(共55分)
一、(本题共5小题,每题只有1个选项符合题意,每题2分,共10分)
1.下列元素属于碱金属元素的是
A.Pb B.Sb C.Rb D.Lu
2.据报道,某国一集团拟在太空建造巨大的集光装置,把太阳光变成激光用于分解海水制
|
氢气:2H2O === 2H2↑ + O2↑ 下列说法不正确的是( )
A. 水的分解反应是放热反应
B. 反应物所具有的总能量低于生成物所具有的总能量
C. 使用氢气做燃料有助于控制温室效应
D. 氢能源将是21世纪中后期最理想的能源剂
3. 下列比较不正确的是
A.熔点:Li>Na>K B.热稳定性:Na2CO3>CaCO3>NaHCO3
C.密度:煤油<Li<Na<H2O D.还原性:Li<Na<K
4.吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”。中国科学家尝试用Na2SeO3清除人体内活性氧,Na2SeO3的作用是
A.还原剂 B.氧化剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
5.氢化钠(NaH)是生氢剂,可发生如下反应:NaH + H2O == NaOH + H2↑,对这一反应的叙述正确的是
A.NaH是氧化剂 B.NaOH是氧化产物
C.NaOH是还原产物 D.氧化产物和还原产物的质量比是1:1
二、(本题共15小题,每小题只有一个选项符合题意,每小题3分,共45分)
6.根据下列物质中N的化合价判断,下列说法中错误的是
①HNO3具有氧化性 ②HNO3具有还原性
③NH3具有氧化性 ④NH3具有还原性
A.①② B.③④ C.①③ D.②③
7.下列各组中的离子,能在溶液中大量共存的是
A.H+,Ca2+,Cl-,CO32- B.Na+,Fe3+,,OH-,SO42-
C.K+,Na+,OH-,Cl- D.Cu2+,Ba2+,Cl-, SO42-
8.下列物质属于强电解质的是
A.CO2 B.CaCO3 C.石墨 D.H2CO3
9.下列反应的离子方程式有错误的是
A.硫酸氢钠溶液与氢氧化钠溶液 ![]()
![]()
B.钾与水 ![]()
C.碳酸氢钙溶液与氢氧化钠溶液![]()
![]()
D.小苏打与盐酸反应![]()
![]()
10.下列有关Na2CO3和NaHCO3性质的比较中,正确的是
A.热稳定性:Na2 CO3<NaHCO3 B.与稀盐酸反应的快慢:Na2CO3>NaHCO3
C.106gNa2CO3和84gNaHCO3分别与过量的盐酸反应,放出CO2的质量:
Na2 CO3>NaHCO3
D.常温时水溶性:Na2 CO3>NaHCO3
11.某碱金属0.195g与足量的水反应时,生成0.0050g氢气,这种金属是
A.锂 B.钠 C.钾 D.铷
12.现有NaOH、Na2CO3和Ba(OH)2三种无色溶液,用一种试剂就可将它们鉴别出来,这种试剂是
A.HCl B.H2SO4 C.Na2SO4 D.CaCl2
13.下列各种方法中,可以用于除去苏打中混有的少量小苏打的是
A.水洗 B.加盐酸 C.通入CO2 D.加热
14.下列关于过氧化钠的说法中,不正确的是
A.是白色固体 B.是强氧化剂
C.能与水反应生成碱和氧气 D.能与二氧化碳起反应生成盐和氧气
15.下列关于碱金属中性质递变中,叙述错误的是
A.随着核电荷数的递增,碱金属的单质熔点依次升高
B.随着核电荷数的递增,碱金属的单质与水反应的剧烈程度越来越大
C.随着核电荷数的递增,单质的还原性越来越强
D.随着核电荷数的递增,单质与氧气反应剧烈程度越来越大,生成物的氧化物越来越复杂
16.关于Na的描述正确的是
①Na在自然界既有游离态又有化合态存在 ②金属Na着火可以用泡沫灭火器救火 ③实验室中少量的Na保存在煤油里 ④Na-K合金做原子反应堆的导热剂 ⑤Na比Cu活泼,因而Na可以从CuCl2溶液中置换出Cu ⑥Na在空气中燃烧,主要产物是Na2O2
A.①③④⑤⑥ B.③④⑥ C. ③④ D.全部
17.下列各组物质中,没有任何化学反应发生的是
A.CH3COOH溶液+NaOH溶液 B.Na2SO4溶液+Cu(OH)2
C.Na2CO3溶液+Ca(OH)2澄清液 D.Na投入NaCl溶液中
18.将铜片溶于稀硝酸中,发生下列反应
|
A.3:8 B.8:3 C.2:3 D.3:2
19.一定温度下,Wg下列物质在足量氧气中充分燃烧,产物与过量的过氧化钠完全反应,过氧化钠固体增重Wg,符合此要求的是
(1)H2 (2)CO (3)CO和H2 (4)HCOOCH3 (5)HOOC-COOH
A.全部 B.仅(4)(5) C.仅(1)(2)(3) D.除(5)以外
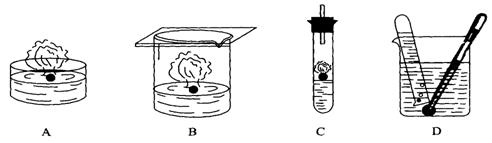
20.在下列四种演示金属钾与水反应的实验装置中正确的是
三、填空题(本题包括4小题,共23分)
|
剧烈燃烧起来。
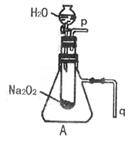
(1) 由上述实验现象所得出的有关过氧化钠跟水
反应的结论是:a:有氧气生成,b:________________。
(2) 写出Na2O2和H2O反应的化学方程式并标出
电子转移的方向与数目: 。
其中还原剂是 ,氧化剂是 。
|
用以验证第二条结论的实验方法是:_______________
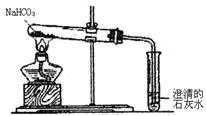
22.( 5分)右图是加热分解碳酸氢钠的实验装置图。
(1)盛澄清石灰水的试管中可观察到的现象
是 有关反应的离子方程式
(2)盛澄清石灰水的试管中不再出现气泡时,
 停止实验的正确操作是
停止实验的正确操作是
(3)证明试验中碳酸氢钠已完全分解的方法是
(4)实验结束时发现盛澄清石灰水的试管中又重新变成透明澄清的溶液,写出其中发生反应的离子方程式
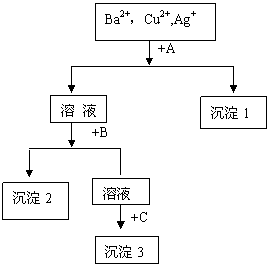
23.( 5分)某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下(写出最佳答案)
(1)沉淀的化学式:沉淀1 ,
沉淀2 ,沉淀3 ;
(2)写出混合液+A的离子方程式
溶液+B的离子方程式
| |
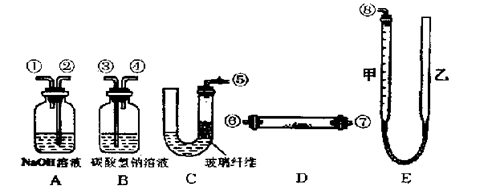
上图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0 ― 50 mL),供量气用;乙管可上下移动,以调节液面高低,C装置可作启普发生器使用。上述装置的连接顺序是(各接口的编号,其中连接胶管及夹持装置均省略):
⑤ ⑧(⑥⑦顺序可对调) 。
实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。
试回答:
(1) 装置C中放入的反应物是 和 。
(2) 装置A的作用是 ,装置B的作用是 。
(3) 为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数,求其差值的过程中,应注意视线与液面最低处相平和
(填写字母编号)
a. 读数时不一定使甲、乙两管液面相平
b. 读数时应上下移动乙管,使甲、乙两管液面相平
25.( 6分)
(1)用实验证明Na2CO3溶液中含有NaOH,所用试剂 ,简述方法 。
(2)用实验证明Na2CO3溶液中含有NaHCO3,所用试剂 ,简述方法 。
四、计算题:(6分)
26.(6分)有一表面被部分氧化的金属钠,质量为10.8g,投入到100g水中完全反应后,收集到0.2g氢气,试计算:
(1) 被氧化的金属钠的质量是多少克?
(2) 未被氧化前金属钠的质量?
(3) 反应后所得溶质的质量分数?
高一化学答题卡
一、(本题共5小题,每题只有1个选项符合题意,每题2分,共10分)
| 题号 | 1 | 2 | 3 | 4 | 5 |
| 答案 |
|
|
|
|
|
二、(本题共15小题,每小题只有一个选项符合题意,每小题3分,共45分)
| 题号 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 |
|
|
|
|
|
|
|
|
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | |
| 答案 |
|
|
|
|
|
|
|
三、填空题(本题包括5小题,共39分)
21.(1) 。
(2) 。
, 。
(3)
。
22.(1) ,
(2)
(3)
(4)
23.(1) , , 。
(2) ; 。
24.
⑤ ⑧
(1) , ;
(2) , ;
(3) ;
25.(1) ,
。
(2) ,
。
四、计算题:(6分)
26.
 |
商丘市回民中学2007―2008学年度上学期期中考试
高一化学参考答案
一、(本题共5小题,每题只有1个选项符合题意,每题2分,共10分)
| 题号 | 1 | 2 | 3 | 4 | 5 |
| 答案 | C | A | C | A | D |
二、(本题共15小题,每小题只有一个选项符合题意,每小题3分,共45分)
| 题号 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | D | C | B | B | D | C | B | D |
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | |
| 答案 | A | A | B | B | C | D | B |
三、填空题(本题包括4小题,共39分)
21. (1)该反应是放热反应 (1分)
失2×e-
(2)2Na2O2+4H2O======4NaOH+2H2O+O2↑ (2分)
得2×e-
Na2O2; (1分) Na2O2 (1分)
(3)将带火星的木条靠近导管口P处,木条复燃;(1分)将导管q浸入水中,反应过程中导管口有气泡冒出;反应后冷却,在导管q形成一段水柱。(1分)
22.(1) 出现白色沉淀 (1分) Ca2++2OH-+CO2=CaCO3↓+H2O (1分)
(2) 先撤导管后移开酒精灯 (1分)
(3) 盛澄清石灰水的试管中无气泡产生 (1分)
(4)CaCO3+CO2+H2O=Ca2++2HCO3- (1分)
23.(1)AgCl (1分) BaSO4 (1分) Cu(OH)2 (1分)
(2)Ag++Cl-=AgCl↓ (1分) Ba2++SO2-4=BaSO4↓ (1分)
24. ③④⑥⑦②① (1分)
(1) 大理石 , 盐酸 (各1分)
(2) 吸收混在O2中未反应的CO2, 吸收CO2中混有的HCl (各1分)
(3) b (1分)
25.(1)CaCl2(BaCl2)和酚酞,略(3分) (2)CaCl2(BaCl2)和NaOH,略(3分)
四、计算题:(本题包括2小题,共12分
26.(1)4.6g (2)9.2g (3)14.5%
解析:设被氧化的钠xg,未被氧化的钠yg
2Na+2H2O =2NaOH+H2↑
2×23 80 2
x 8g 0.2g
x=4.6g
m Na2O=10.8g-4.6g=6.2g
4Na + O2=2Na2O
4×23 2×62
Na2O + H2O=2NaOH
62 2×40
6.2g 8g
y=4.6g
4.6g+4.6g=9.2g
![]()