高一化学上学期第一次月考试题
可能用到的原子量:H 1 O 16 Na 23 c 12 Cu 64
Mg 24 Ca 40
第I卷(48分)
一.选择题(每小题只有一个选项符合题意,每小题 2分,共48分)
1.苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有( )
A.氧化性 B.还原性
C.碱性
D.酸性
2.只能表示一个化学反应的离子方程式是 ( )
A.H++OH-=H2O B.Cu2++2OH-+Ba2++SO42- =BaSO4↓+Cu(OH)2↓
C.Zn(OH)2+2H+=Zn2++2H2O D.CO32- + 2H+=H2O+CO2↑
3.一定条件下硝酸铵受热分解的未配平化学方程式为:NH4NO3—HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为( )
A.1∶1 B.5∶4
C.5∶3 D.3∶5
4. 下列关于Na和Na+性质的叙述正确的是(
)
A 它们都显碱性 B 它们都有强还原性
C 它们都能同H2O,O2反应 D Na只有还原性,Na+只有氧化性
5. 在显碱性的无色溶液中能大量共存的离子组是( )
A、Na+,Ca2+,HCO3-,NO-3 B、Na+,Ba2+,Cl-,MnO4-
C、K+,Na+,Cl-,Cu2+ D、Na+,Ba2+,NO3-,I-
6.为减少对环境的污染,某甲、乙两个相邻的工厂做了横向联合。已知两厂排放的污水经初步处理后,只溶有Ag+、Ba2+、Fe3+、Na+、Cl-、SO42-、NO3-、OH-的各不相同的4种离子(设各离子浓度比较大)。若单独排放仍会造成环境污染,如将两厂的污水按适当的比例混合沉淀后,污水变成无色澄清的硝酸钠排出,则污染程度会大为降低。你认为下列分析判断正确的是( )
A.SO42-和NO3-可存在于同一工厂 B.Cl-和NO3-一定在不同的工厂
C.Ag+和Na+可能在同一工厂 D.NaNO3来自同一工厂
7.A-E均为含氯的化合物,转换关系如下:
①B+H2O→C+H2 ②A→B+NaCl ③E+NaOH→B+C+H2O
④D+NaOH→A+B+H2O 则其中Cl的化合价由低到高的顺序为( )
A.CEBDA B.ECBDA C.BDECA D.ADBEC
8.金属钠着火时,可以灭火的物质是( )B
A.水 B.黄沙 C.煤油 D.泡沫灭火剂
9. 下列关于 Na2CO3 和NaHCO3的说法中正确的是( )
A.热稳定性: NaHCO3比Na2CO3稳定 B.常温时,在水中的溶解性: Na2CO3<NaHCO3
C.两者都与盐酸反应生成CO2 D.它们都属于盐类,所以水溶液显中性
10.通常情况下,下列物质露置在空气中不会发生变化的是( )
A.NaOH B.Na 2O2 C.NaHCO3 D.Na2CO3·10H2O
11.下列说法正确的是( )
A.纯碱就是碱 B.食盐不是盐 C.烧碱不是碱 D.干冰不是冰
12.下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),不会引起产物种类改变的是 ( )
A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.木炭(C)和O2
13.下列离子方程式正确的是( )
A.钠与水反应:Na + H2O == Na+ + OH- + H2↑
B.氧化钠与盐酸反应:O2- + 2H+ == H2O
C.NaHCO3溶液与稀硫酸反应:CO32- + 2H+ == CO2↑+ H2O
D.NaOH溶液与小苏打溶液:HCO3- + OH- == CO32- + H2O
14.在一定温度下,向足量的饱和Na2CO3溶液中加入1.06g无水Na2CO3,搅拌后静置,最终所得晶体的质量为( )
A.等于1.06g B.大于1.06g而小于2.86g
C.等于2.86g D.大于2.86g
15.如图,在一只盛有饱和Ca(HCO3)2溶液的烧杯中漂浮着一个木块。小心地向烧杯中滴加石灰水,至二者恰好反应时停止滴加,静置一段时间,可以观察到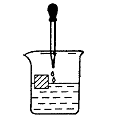 的现象是( )
的现象是( )
A.滴加过程中有气泡产生 B.滴加过程中无白色沉淀产生
C.静置后,木块浸入水中的体积比滴加石灰水前减小
D.静置后,木块浸入水中的体积比滴加石灰水前增大
16.向紫色石蕊溶液中加入过量的过氧化钠粉末,振荡,其现象是( )
A.溶液仍为紫色 B.溶液变蓝色且不褪
C.溶液先变蓝后褪色 D.有沉淀生成
17.将等质量的金属钠投入到下列物质的水溶液中,溶液的质量减轻最大的是( )
A.HCl B.CuSO4 C.MgCl2 D.Ca(HCO3)2
18.某学生将一包固体溶于水,检出溶液中含有K+、Na+、NO3-、Cl-四种离子,则该固体物质的组成是( )
A.NaCl和KNO3 B.NaCl、KNO3、KCl和NaNO3
C.KCl和NaNO3 D.以上三种情况都有可能
19.下列六种物质中,不能与CO2反应的是( )
① Na2O ② Na2O2 ③ NaCl(aq) ④ Na2CO3(aq) ⑤ NaOH(aq) ⑥ NaHCO3 (aq)
A.③④ B.③⑥ C.②③ D.②⑤
20.某同学用托盘天平称量镁粉25.2g(1g以下用游码),他把镁粉放在右盘,当天平平衡时,所称取的镁粉的实际质量是B
A.25.2g B.24.8g C.24.2g D.25.8g
21.有水参与的下列反应:
① Na + H2O—; ② Na2O + H2O—; ③ Na2O2 + H2O—;
④ 3Fe+
4H2O![]() Fe3O4 + 4H2 ;⑤ SO2 + H2O—,
Fe3O4 + 4H2 ;⑤ SO2 + H2O—,
其中水既不是氧化剂,又不是还原剂的反应是( )
A.①③ B.②③⑤ C.③④ D.③④⑤
22.20g纯碱和小苏打的混合物,加热至恒重时称量固体质量为13.8g,则在混合物中纯碱的质量分数是( )
A.84% B.8.4% C.16% D.1.6%
23.将等质量的① Na ② Na2O ③ Na2O2 ④ NaOH ⑤ Na2CO3·10H2O露置于空气中,最后质量由小到大的顺序是( )
A.⑤<④<③<②<① B.①<②<③<④<⑤
C.⑤<④<②=③<① D.⑤<③<④<②<①
24.将8.4gNaHCO3和7.8gNa2O2在密闭容器中灼烧,充分反应后,容器内的物质是( )
A.Na2CO3、Na2O和O2 B.Na2CO3、O2和H2O(g)
C.Na2CO3、CO2、O2和H2O(g) D.Na2CO3、NaOH和O2
| 密 封 线 |
第II卷 非选择题(共60分)
二.(非选择题 ,每空2分,共60分 )
25 在S2-, Fe2+, Fe3+ ,Mg2+, S , I- , H+ O22- 中,只有氧
化性的是 ,只有还原性的是 ,
既有氧化性又有氧化性的是
26.已知:2A3+ +2B- =2A2+ +
B2,C2 +2A2+ =2A3+ +2C-
,
2C- +D2 = C2 + 2D-。现向含有A2+、B-、C-、D-的溶液中加入足量的C2,则反应后溶液中离子数量明显减少的是
,离子数量基本不变的是
27.现有下列物质:①NaCl晶体 ②液态SO2 ③液态的 醋酸 ④汞 ⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧KOH溶液
⑴以上能导电的是 ; ⑵以上属电解质的是 ; ⑶属强电解质的是 ;
⑷以上属非电解质的是 。
28.下列物质中:①钠 ②过氧化钠 ③碳酸钠 ④碳酸氢 钠(填序号)
⑴可用于漂白织物、麦杆、羽毛的是 ;
⑵可用于电光源上的是 ;
⑶制糕点所用的发酵粉的主要成分是 ;
⑷广泛用于玻璃、制皂、造纸、纺织工业的是 ;
⑸医疗上用于治疗胃酸过多的药剂是 。
29.写出两种以NaHCO3为原料制取CO2的化学反应方程式:
方法a
方法b
这两种方法中,方法 的碳酸氢钠的利用率高,原因是
30.一氧化氮是大气的主要污染物之一。近几年来,又发现在生物体内存在少量的一氧化氮,它有扩张血管和增强记忆力的功能,成为当前生命科学研究的热点。
⑴一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为
4X+5O2 ==4NO+6H2O,根据质量守恒定律可以推出X的化学式为 ,此反应中转移的电子数为 个,氧化剂为 。
⑵汽车尾气中含有一氧化氮、一氧化碳等有毒气体,治理的方法是在汽车尾气的排气管上装一个催化转换器,在催化剂的作用下,一氧化氮与一氧化碳反应可生成二氧化碳和氮气,该反应的化学方程式为
,还原产物为
31.已知在下列反应关系中,E为淡黄色固体,C,F为无色气体,D为无色液体,它们有如下关系:
A→B+C↑+D , E+C→B+F , E+D→G + F↑ , A+G →B+D
(1)试推断C ,D ,E ,F
(2)如果G溶液中含有少量的B杂质,选用 溶液可除去B杂质,离子方程式为
(3)现有A,B,G三种溶液,请设计简单实验鉴别之
参考答案
一.选择题 :
1.B 2.B 3.C 4.D 5.D 6.B 7.D 8.B 9.C 11.D 12.C 13.D 14.D
15.D 16.C 17.D 18.D 19.B 20.B 21.B 22.C 23.A 24.D
二.非选择题:
25.Fe3+ Mg2+ H+ S2- I- Fe2+ S O22-
26.A2+、B- D-
27.④⑧ ①③⑤ ①⑤ ②⑥⑦
28.② ① ④ ③ ④
29.a. 2NaHCO3 =Na2CO3 + H2O + CO2↑
b. NaHCO3 + HCl=NaCl+ H2O + CO2↑
b 制取相等质量的CO2 所需NaHCO3 的质量比Na2CO3 的质量少,并C元素全部转变为CO2
30.(1)NH3 20个 O2
(2)2CO +2 NO =2 CO2 + N2 N2
31.(1)C、CO2 D、H2O E、Na2O2 F、O2
(2)适量的石灰水 Ca2+ + CO2- = CaCO3 ↓
(3)