高一年级化学第一学期期终考试
化学试卷
命题教师:孙焱 审题教师:陈如松
(所需相对原子质量:H-1,N-14,O-16,S-32 )
一、选择题(每题只有一个正确选项,每题3分,共30分)
1、放射性核素12553I可用于治疗肿瘤,该核素的中子数为 ( )
A、19 B、53 C、72 D、125
2、环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的。下列环境问题与所对应的物质不相关的是 ( )
A、温室效应――二氧化碳 B、光化学污染――二氧化氮
C、酸雨――二氧化碳 D、臭氧层破坏――氟氯烃
3、铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门等。下列性质与这些用途无关的是 ( )
A、强度高 B、不易生锈 C、密度小 D、导电、导热性好
4、下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是 ( )
A、碘水 B、溴水 C、氯水 D、NaOH溶液
5、下列物质中既能与盐酸反应,又能与NaOH溶液反应的是 ( )
①Na2SiO3;②Al(OH)3;③NH4HCO3;④Al2O3
A、①②④ B、②③④ C、②④ D、全部
6、关于HCl、H2SO4、HNO3三大强酸的说法正确的是 ( )
A、都是含氧酸 B、都属于强电解质
C、都容易挥发 D、都能与金属Mg发生置换反应
7、能由单质直接化合而得的化合物是
A、FeS B、CuS C、FeCl2 D、SO3
8、最新的研究表明:一氧化氮吸入治疗法可快速改善SARS中重症患者的缺氧状况,缓解病情。病毒学研究证实,一氧化氮对SARS病毒有直接抑制作用。下列关于一氧化氮的叙述正确的是 ( )
A、一氧化氮是一种红棕色的气体
B、常温常压下,一氧化氮不能与空气中的氧气直接化合
C、一氧化氮可以由氮气和氧气在放电条件下直接化合得到
D、一氧化氮易溶于水,不能用排水法收集
9、下列说法正确的是 ( )
A、浓硝酸和浓硫酸都应该保存在棕色试剂瓶中
B、NaOH溶液用带有橡胶塞的试剂瓶保存
C、工业制得的浓盐酸、浓硝酸通常带有黄色是由于含有Fe3+杂质
D、铝制或铁制容器可贮运浓硫酸、浓硝酸和浓盐酸这三大强酸
10、在体积为V L的密闭容器中通入a mol NO和b mol O2。反应后容器内氮原子数和氧原子数之比为 ( )
A、a/b B、a/2b C、a/(2a+b) D、a/(a+2b)
二、选择题(本题包括10小题,每小题3分,共30分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给3分,但只要选错一个,该小题就为0分。)
11、在无色强酸性溶液中,下列各组离子能够大量共存的是........................... ( )
A、Cl-、Na+、NO3-、Ca2+ B、NH4+、HCO3-、Cl-、K+
C、K+、Ba2+、Cl-、SO42- D、Cu2+、NH4+、I-、Cl-
12、下列离子方程式的书写正确的是…………..…………………..………….…..( )
A、NaHCO3溶液与NaOH溶液反应: OH- + HCO3- = CO32- + H2O
B、铁和稀硝酸反应:Fe + 2H+ = H 2↑+ Fe 2+
C、向AlCl3溶液中加入过量的NaOH溶液:Al3+ + 3OH- = Al(OH)3↓
D、实验室用大理石和稀盐酸制取CO2:2H+ + CO32- = CO2↑+ H2O
13、只用一种试剂,可区别Na2SO4、AlCl3、NH4Cl、MgSO4四种溶液,这种试剂是( )
A、HCl B、BaCl2 C、NaOH D、AgNO3
14、盛满NO2气体的试管,倒置在水槽中,反应后,液面上升的高度是试管的( )
A、1/2 B、1/3 C、2/3 D、5/6
15、下列气体中不能用浓硫酸干燥的是 ( )
A、NH3 B、H2 C、Cl2 D、SO2
16、在实验室中,对下列事故或药品的处理正确的是..................................... ( )
A、漂白粉长期放置在烧杯中
B、金属钠着火燃烧时,不能用泡沫灭火器灭火,应该用沙子灭火
C、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
D、有大量的氯气泄漏时,用碳酸钠溶液浸湿软布蒙面,并迅速离开现场
17、在常温常压下,下列各组气体不能共存的是 ( )
A、SO2与O2 B、H2S与SO2 C、O2与N2 D、NO与O2
18、向盛有氯化铁溶液的烧杯中加入过量的铜粉,反应结束后,溶液中大量存在的金属离子是 ( )
A、Fe 2+、Cu2+ B、Fe 2+、Fe3+ C、Fe 3+、Cu2+ D、Cu+、Cu2+
19、将铜粉放入稀硫酸中,加热无明显现象发生。但加入某盐后,发现铜粉质量逐渐减少,则该盐可能是 ( )
A、ZnSO4 B、Fe2(SO4)3 C、NaCl D、KNO3
20、在一定温度和压强下,将一支容积为15mL的试管充满NO2后,倒置于一个盛水的水槽中,当试管内液面上升一定高度不再变化时,在相同条件下再通入O2,若要使试管内的液面仍保持在原高度,则通入O2的体积为 ( )
A、8.75mL B、7.5mL C、3.75mL D、10.5mL
三、填空题(共29’)
21、(7’)用化学方程式解释下列有关实验现象:
⑴、向氨水中滴几滴酚酞试液,溶液变红色:
⑵、两只棉球分别滴有几滴浓氨水和浓盐酸放入同一只烧杯中,用表面皿盖住烧杯口,烧杯内有白烟:
⑶、一瓶无色气体打开瓶盖后,瓶口呈现出红棕色:
⑷、长期暴露在空气中的亚硫酸钠变质:
⑸、当电闪雷鸣之时,空气会发生很多化学反应,试写出与氮元素有关的化学方程式:
; ; 。
22、(6’)今有HCl、Cl2、H2S、NH3、NO2、CO2、H2、SO2等气体,问:
⑴、形成酸雨的是____________________________;
⑵、比空气轻的气体是____________________________;
⑶、用水做溶剂,可作喷泉实验的氢化物是____________________________;
⑷、能用碱石灰干燥的是____________________________;
⑸、能使品红试液褪色的是____________________________;
⑹、可导致光化学烟雾的是____________________________。
23、(6’)已知A.B.C.D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①A+B→白色沉淀,加入稀硝酸,沉淀不溶解。
②B+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色。
③C+D→白色沉淀,继续加D溶液,白色沉淀逐渐消失。
⑴、则各是什么物质的化学式为:A 、B 、C 、D 。
⑵、现象③中所发生反应的离子方程式为:
、 。
24、(5’+5’)某学生做实验:
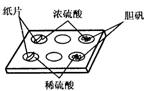 实验一:在一个白色的点滴板的孔穴中分别故入小纸片、少量CuSO4・5H2O。然后如图所示,分别滴入几滴浓硫酸或稀硫酸,观察现象。回答下列问题:
实验一:在一个白色的点滴板的孔穴中分别故入小纸片、少量CuSO4・5H2O。然后如图所示,分别滴入几滴浓硫酸或稀硫酸,观察现象。回答下列问题:
⑴、浓硫酸滴入小纸片上,小纸片变 __________________(填实验现象),说明浓硫酸具有_____________性。
⑵、稀硫酸滴入CuSO4・5H2O中,胆矾_______________(填实验现象);
浓硫酸滴入CuSO4・5H2O中,胆矾_____________________(填实验现象),说明浓硫酸具有_______________性。
实验二:为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
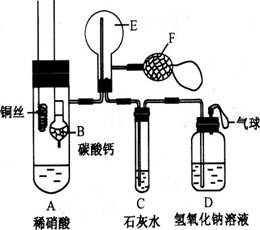
⑴、实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先赶出去其中的空气。将装CaCO3的干燥管下移与稀HNO3反应产生CO2,当看到C处有_____________现象可以确定E中空气已被赶尽:
⑵、将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为:__________________________________。
⑶、如何证明E中收集到的是NO而不是H2?
______________________________________________________
当证明出是NO后,C中白色沉淀溶解,其原因是
________________________________________________________
⑷、装置D的作用是___________________________________________________
四、计算题(共11’)
25、(5’)二氧化硫是一种酸性氧化物,能与氢氧化钠溶液发生反应。反应产物与反应物的量有关,当二氧化硫过量时,生成亚硫酸氢钠;当氢氧化钠过量时,生成亚硫酸钠。
⑴、请写出上述反应的离子方程式。
⑵、某硫酸厂每天排放2.24×104 m3(标准状况)尾气,其中含0.2%(体积分数)的SO2,现欲用2.0 mol/L氢氧化钠溶液进行处理,每天至少需氢氧化钠溶液多少升?
26、(6’)一种氮肥由硝铵和硫铵混合而成,取此氮肥2.92g跟足量的碱溶液反应,放出氨0.896L(标准状况)。求:
⑴、硝铵和硫铵的物质的量分别为多少?
⑵、氮肥中氮的质量分数。
化学试卷答案
一、二 选择题(3’×20=60’)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | C | D | D | B | B | A | C | B | D |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | A | A | C | C | A | BD | BD | A | BD | A |
三、填空题(共29’)
21、⑴、 NH3 + H2O
![]() NH3・H2O
NH3・H2O![]() NH4+ +OH-;
NH4+ +OH-;
⑵、NH3+HCl==NH4Cl ⑶、2NO+O2==2NO2;
⑷、2Na2SO3 + O2==2Na2SO4 ⑸、 (略)。
22、(6’) ⑴、NO2 、SO2 ; ⑵、NH3、H2; ⑶、HCl、NH3;
⑷、NH3、H2; ⑸、Cl2、SO2; ⑹、NO2。
23、(6’) ⑴、A、BaCl2 B、FeSO4 C、AlCl3 D、NaOH。
⑵、Al3+ +3OH-==Al(OH)3↓、Al(OH)3+OH-==AlO2-+2H2O。
24、(5’) 实验一: ⑴、变黑;脱水性。⑵、无明显现象;蓝色晶体变成白色;吸水性。
(5’) 实验二:
⑴、白色浑浊; ⑵、(略)。
⑶、用双连打气球向E中鼓入空气,若气体变红,则收集的就是NO。
⑷、NO2和水反应生成硝酸,硝酸使沉淀溶解。(也可用方程式回答)
四、计算题(共11’)
25、(5’)⑴ SO2+OH-==HSO3- SO2 + 2OH-==SO32-+H2O ⑵ 1000L
26、(6’) ⑴ 0.02mol、0.01mol ⑵ 28.8%