��һ�꼶��ѧ��һѧ�ڽο����Ծ�
����ѧ��������
����ʱ��:90���ӡ� ��ֵ:100�֡���
�����õ������ԭ��������H��1��C��12��N��14��O��16��Na��23��Al��27��
S��32��Cl ��35.5��Ca��40��Fe��56��Cu��64
ע�����
1���ش��һ��ǰ��������ؽ��Լ�����������֤�ţ�����д��ɫ�ּ���0.5����ǩ�ֱ���д�ڴ���ֽ�������ڣ�����2BǦ��Ϳд�ڴ���ϡ�
2����һ���𰸱�����2BǦ����Ϳ�ڴ���ϣ�������λ������һ����Ч��ÿС��ѡ���𰸺���2BǦ�ʰѴ���϶�Ӧ��Ŀ�Ĵ𰸱��Ϳ�ڡ�����Ķ�������Ƥ���ɾ�����ѡͿ�����𰸡�
��I����ѡ��������55�֣�
һ��ѡ���⣨��20С�⣬1~5ÿ��2��, 6~20ÿ��3�֣�ÿС��ֻ��һ����ȷ��������55�֣����������II����ʼ����Ӧ�����ڣ�
1��ͬѧ�������Ѿ���Ϊ����Ϊһ�������Ĺ���ͨ�����л�ѧ��ѧϰ����ÿһλ����Ӧ�þ߱������б�����ȷ�е��ǣ���������������������������������(���� )
A��δ������Ļ�ѧ������������ B��ѧ������������ ������
C��Ԩ����רҵ��ѧ֪ʶ�������� D���������ļ�ֵ��
2����ѧ����������Ľ��ݣ����ǽ�������������Ѿ����뿪��ѧ��������ʵ�뻯ѧ�ص��ǡ�������������������������������������������������������������(���� )
A�����ȼ�������������� B��ҩ��ϳɡ���C��ұ����²��������������� D�� ��Ų�
3�������ǵ����ߣ����и������ʴ��������ǡ������������������� (����)
A������� ����B��������� C�����ʡ��������� D�������
4�����������Һ���Բ�ȡ�ķ����ǡ��������������������� (����)
A���������� B������۹۲졡��
C��ϡ�͡�����D�����ö����ЧӦ��ʵ��
5�����л�ѧҩƷ�İ�ȫ��ʾ�Ա�ע��ȷ���� ��������������������������(����)������������������������
A��Ũ���ᡪ�綾Ʒ�� B�����ס���ըƷ��
C���ƾ�����ȼƷ����D��̼���ơ���ʴƷ
6����Na2S��S8��(����)��BaSO4�������У�������Ӧ��������ʵĻ�ѧʽ��(����)
A��Na2SO4������������������B��KHSO3������������������ C��H2S���������������� D��SO3
7��ƫ�����£�C2H8N2����һ�ָ���ȼ�ϣ�ȼ�ղ����ľ���������Ϊ�������ػ�����ƶ���������������ȷ���ǡ����������������������������������������� (���� )
A��ƫ�����£�C2H8N2����Ħ������Ϊ60g
B��6.02��1023��ƫ�����£�C2H8N2�����ӵ�����Ϊ60g
C��1 mol ƫ�����£�C2H8N2��������Ϊ60 g/mol
D��6gƫ�����£�C2H8N2������NA��ƫ�����£�C2H8N2������
8�����и����е����ӣ�������Һ�д���������ǡ��������������������� (���� )
A�� H�� Na����CO32�� Cl������������ B�� Ba2�� Na����Cl�� SO42��
C�� K����H����SO42����OH������������ D�� Ag����Al3����NO3����H��
9����״���£���������������ԭ���������ǡ����������� �������� (����)
A��7.5g C2H6������������B��33.6L N2������������ C��7g CO�������������� D��22.4L H2O
10����ʵ�����У��������¹ʻ�ҩƷ�Ĵ�����ȷ���ǡ�������������������(���� )
A���д���������й©ʱ���÷���ˮ��ʪ�������棬��Ѹ���뿪�ֳ�
B���������Ż�ȼ��ʱ������ĭ��������
C������Ũ����մ��Ƥ���ϣ�����������������Һ��ϴ
D��������ķ�Һ����ˮ�ۣ���ˮ������ˮ��
11������ƿ������У����¶ȡ� ��Ũ�ȡ���������������ѹǿ�����ݿ̶��ߡ�������ʽ���ʽ�����еģ� �������������������������������������������������� (���� )
A���٢ۢݡ�������B���ۢݢޡ�������C���٢ڢܡ������� D���ڢܢ�
12��ijͬѧ��ʵ�鱨����������ʵ�����ݣ�����������ƽ��ȡ11.7 gʳ�Σ�������Ͳ��ȡ5.26 mL������ù㷺pH��ֽ�����Һ��pHֵ��3.5���������ݺ������� (���� )
A���١�������B���ڢۡ������� C���٢ۡ��� ��������D���ڡ�
13������ˮ�Dz�������������,Ϊ�˼���Cl-�Ĵ���,���ѡ�����������еġ���(���� )
A��ʯ����Һ������B�� ���Ȼ�̼������C������������Һ������ D����������Һ��
14���ӵ�ˮ����ȡ����Բ��õķ����ǡ������������������������������� (����)
A����ȡ����������������B�������������������������� C������������������ D������
15��n mol N2��n mol CO��Ƚϣ����������в���ȷ���ǡ��������� (����)
A�������ȡ���B����������ȡ��� C��������ȡ�����D�����������
16����VL��������Һ�У�����wgAl3+��������Һ��SO42�������ʵ���Ũ���� (����)
A��W/27V������B��W/54������ C��W/18V������ D��W/54V
17������ͨ������ʵ����������ʵ�������: �ٹ��� ������ ���ܽ� ��ȡҺ���Լ� ��ȡ�����Լ�.һ��Ҫ�õ����������ǡ��������������������������������� (���� )
A���٢ڢۡ����� B���ܢݡ�����C���٢ܡ������� D���٢ۢ�
18������ͨ������ʵ�������������ӷ���ʽ����д��ȷ���ǡ��������� (���� )
A��ʵ�����ô���ʯ��ϡ������ȡCO2��2H+ + CO32- �� CO2��+ H2O
B������ͭ��Ba(OH)2��Һ��Ӧ�� Cu2++ 2OH-== Cu��OH��2��
C��Cu(OH)2�����ᷴӦ��H+ + OH��===H2O
D��NaHCO3��Һ��NaOH��Һ��Ӧ�� OH- + HCO3- �� CO32-��+ H2O
19������ͨ������ʵ��������ͬ�����FeCl3 ��MgCl2 ��NaCl��Һ������Cl����Ŀ��ͬ����FeCl3 ��MgCl2 ��NaCl��Һ�����ʵ���֮��Ϊ���������� (���� )
A��1��1 ��1������ B��2��3��6������ C��3��2��1������ D��1��2��3
20������ͨ������ʵ������ͨ���ܽ⣬���ˣ������Ȳ������ɽ����и������������ǡ� (����)������
A�������ơ��������ơ� B������ͭ���������̡�
C���Ȼ��ء��������̡� D������ͭ����������
17����ʵ���������ͨ��������з�Ӧ�У�HCl����ԭ�����ǡ��������� (����)
A��Zn + 2HCl = ZnCl2��+ H2������
B��CaCO3 + 2HCl = CaCl2 + H2O + CO2��
C��NaOH + HCl = NaCl + H2O������
D��MnO2 + 4HCl(Ũ) ���� MnCl2 + Cl2��+ 2H2O��
18����ʵ���������ͨ��������и���������Һ��ķ�Ӧ��������ͬһ���ӷ���ʽ��ʾ���� ������������������������������������������������������������ (�� )
A��CH3COOH��Na2CO3��CH3COOH��CaCO3
B��AgNO3��HCl��Ag2CO3��HCl
C��BaCl2��Na2CO3��Ba(OH)2��NaHCO3
D��KOH��NH4Cl��Ba(OH)2��NH4Cl
19����ʵ���������ͨ���������Һ��XO4����H2O2���Ӹ�����ǡ��Ϊ2�U5ʱ����Һ��XO4�����ӱ���ԭΪ�ϵͼ�̬����XԪ�صĻ��ϼ۱�Ϊ������������������ (����)
A��+1�������� B��+2�������� C��+3���������� D��+4
20����ʵ���������ͨ������Ʊ��谱�����ƵĻ�ѧ����ʽ CaCO3 + 2HCN �� CaCN2 + CO + H2��+ CO2 �ڷ�Ӧ�С����������������������������������������� (����)
������Ԫ�ر�������̼Ԫ�ر���ԭ�������� �£�HCN���������������ǻ�ԭ��
�ã�CaCN2���������H2�ǻ�ԭ����� �ģ�COΪ�������H2Ϊ��ԭ����
��һ�꼶��ѧ��һѧ�ڽο����Ծ�
��ѧ�Ծ�����ֽ
һ��ѡ����
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� |
|
|
|
|
|
|
|
|
|
|
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� |
|
|
|
|
|
|
|
|
|
|
��II������ѡ���� 45�֣�
��������⣨������3С�⣬��38�֣�
21.��12�֣�����ͨ������ʵ��������ͼ��������ˮ��ȡ��������ˮ�ļ���װ�ã������ȼ��̶������ԣ�����ԭ����̲��е�ʵ����ȫ��ͬ���ش��������⣺
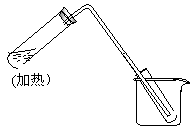
��
�� ��ߴ��Թ���Ҫ���뼸Ƭ���Ƭ������������������������������ ������������ ��
�� ��װ����ʹ�õIJ������ܽϳ����������������������������������������������� .
�� �ձ��л�Ҫʢ�е��������������������������������������������������������� .
21����12�֣���ʵ���������ͨ�������ʮ����ҹ����ձ�����һ���ƶ�������ÿ�������϶���һ����С�Ŀף�ԭ���dz���ǰ������ȡ�����͡�ͨ���������ϵ�֪����ȡ���ͷ�����ѹե�����л��ܼ�����Һ̬CO2�ܽ���ȡ����
��1����ԭ���Ͽ��� �������������� ��������������ԭ����һ����
��2������������ȡ����ԭ��������������������������������������
��3��������л��ܼ������ȡ��������ѡ�������ܼ�������������������������
A�������� B�����Ȼ�̼���� C���Ҵ�������D������
��4������Һ̬CO2�ܽ���ȡ������ȱ�㣨���ٸ�һ�㣩
�ŵ㣺������������������������������������������������������������ ����
ȱ�㣺����������������������������������������������������������������
��5���Ա������ṩ�IJ�������ʲô����������������������������������������
22��(14��)ʵ�����ù���NaOH����0.5mol/L��NaOH��Һ500ml������������
���ձ� ��100ml��Ͳ ��100ml����ƿ ��500ml����ƿ �ݲ����� ��������ƽ�������룩
��1������ʱ������ʹ�õ�������___________������ţ�����ȱ�ٵ�������_____ _____����ʵ���������õ��������������÷ֱ���__���� ____�� ����________�������� ___�������������������������������������������������������������� _��
��2��ʹ������ƿǰ������е�һ��������______���������������� ___________��
��3��������Һʱ��һ����Է�Ϊ���¼������裺
�ٳ��� �ڼ��� ���ܽ� ��ҡ�� ��ת�� ��ϴ�� �߶��� ����ȴ��
����ȷ�IJ���˳��Ϊ________________���������������������� ____________��
����4�������ƹ����У�������������ȷ�ģ����в�����������������__________��
���� ��û��ϴ���ձ��Ͳ�������������
��δ��NaOH��Һ��ȴ�����¾�ת�Ƶ�������
���� ������ƿ�����������������ˮ��
�ܶ���ʱ���ӱ��ߡ�
�ݶ���ʱ���ӱ��ߡ�
23��(12��)�ס��ҡ�����λͬѧ�����һ��ʵ�飬�������Ϊ�Լ��������к���SO42������ʵ��Ϊ��
 |
��1������Ϊ��ʵ�鲻�Ͻ�����Ϊ����A���������������� ���ӣ�����һ�֣���Ҳ���д�����
�ҵ�ʵ��Ϊ��
 |
��2������Ϊ�ҵ�ʵ�鲻�Ͻ�����Ϊ����B���������������� ���ӣ�����һ�֣���Ҳ���д�������ʵ��Ϊ��
 |
�����ķ����������Իش�
��3�����Լ��������������� ��������������������������������������������� ��
�Լ��������������� ��������������������������������������������� ������������Ϊ���������������������ݿɲ��
���������⣺����7�֣�
24������ͨ������ʵ������������ˮ����������Ϊ0.9%��NaCl ��Һ���ܶ�Ϊ1.0 g/cm3��
�ʣ���1������Һ�����ʵ���Ũ��Ϊ���٣�
��2��500mL������ˮ�к�NaCl �������ٿˣ�
����
24����ʵ���������ͨ�����ѪҺ�к������ǣ�Ѫ�ǣ���������������Ѫ���ֻᵼ���˻��ʡ������˵�Ѫ��ӦΪ3.9~6.2mmol/L��ijͬѧ��Ѫ���֪��Ѫ�ǵ���������Ϊ0.09%����֪�����ǵ���Է�������Ϊ180����ѪҺ���ܶ�Ϊ1g/mL�����ѧ��ѪҺ��Ѫ�ǵ����ʵ���Ũ���Ƿ���������˵ķ�Χ����ͨ������ش�
��һ�꼶��ѧ��һѧ�ڽο����Ծ�
��ѧ�Ծ���
һ��ѡ��������20С�⣬1~5ÿ��2��, 6~20ÿ��3�֣�ÿС��ֻ��һ����ȷ��������55�֣�
����ͨ��ѡ����𰸣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� | C | D | D | D | C | B | B | D | D | A |
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� | A | A | D | A | A | C | A | D | B | C |
��ʵ���ѡ����𰸣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� | C | D | D | D | C | B | B | D | D | A |
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� | A | A | D | A | A | C | C | D | B | B |
��II������ѡ���� 45�֣�
��������⣨������3С�⣬��38�֣�
21.��12�֣�����ͨ������ʵ������
�� ��ֹ���У�4�֣����� ������ȴ��������ã�4�֣����� ��ˮ��4�֣���
21����12�֣���ʵ���������ͨ�������ÿ��2�֣�
��1��ѹե������ ��2�� �ܽ��ԣ�����ȡҲ�ɣ�������3����C��
��4���ŵ㣺 ������ࡢ��Ч���������������֣�
ȱ�㣺 ����Ҫ��ߡ��豸���ո��ӡ���ʼͶ��ɱ��� ���������֣�
��5���Ա������ṩ�IJ�������ʲô���� ���������֣�
22��(14��)��ÿ��2�֣�
��1���٢ܢݢ� �� �٢ڢܢݢޡ� ��ͷ�ιܡ��������ܽ⡡�� ����
��2������Ƿ�©ҹ��
��3���ڢ٢ۢ�ݢޢܢߢ� �� �ڢ٢ۢ�ݢޢߢܡ�����4����
23��(12��)��1��Ag+ ��3�֣� (2)SO32-����ÿ��3�֣�
(3)����HCl����1�֣������������������2�֣�
BaCl2����1�֣��а�ɫ����������2�֣�
���������⣺����7�֣���������û�й��̲����֣�
24������ͨ������ʵ������
��1��0.154 mol/L ��4�֣����� ��2�� 4.5 g��3�֣�
����24����ʵ���������ͨ�����5mmol/L ��5�֣����� ������2�֣�