高一化学认识化学科学测试题
编辑人:黄贯峰 07.10.06
第Ⅰ卷(选择题 共40分):
一、选择题(本题包括20小题,每小题2分,共40分,每小题只有一个选项符合题意)
1.下列广告用语在科学性上没有错误的是( )。
A.这种饮料中不含任何化学物质
B.这种蒸馏水绝对纯净,其中不含任何离子
C.这种口服液含丰富的氮、磷、锌等微量元素
D.没有水就没有生命
2.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是( )。
A.化学不做实验,就什么都不知道 B.化学不再需要实验
C.化学不再是纯实验科学 D.未来化学的方向是经验化
3.下列对于“摩尔”的理解正确的是( )。
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔是物质的量的单位,简称摩,符号为mol
C.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
4.从生活常识角度考虑,试推断钠元素在自然界中存在的主要形式是( )。
A.Na B.NaCl C.NaOH D.Na2O
5.在科学史上,中国有许多重大的发明和发现,它们为世界的现代化奠定了基础,以下发明和发现属于化学史上中国对世界作出重大贡献的是( )。
①火药 ②指南针 ③造纸 ④印刷术 ⑤炼铜、炼钢、炼铁 ⑥元素周期律的发现 ⑦人工合成蛋白 ⑧原子学说的提出
A.②④⑥⑧ B.①③⑤⑦ C.④⑤⑦⑧ D.①③④⑧
6.通过你的观察和推理,判断下列实验室中对于少量Na的保存方法正确的是()
A.保存在水中 B.密封,保存在广口瓶中
C.用铝箔包裹,密封在广口瓶中 D.密封,保存在煤油中
7.氯化碘(ICl)的化学性质跟氯气相似,请预计它跟水反应的最初生成物是( )
A.HI和HClO
B.HCl和HIO
C.HClO3和HIO D.HClO和HIO
8.容量瓶是用来配制物质的量浓度溶液的定量仪器,其上标有:
①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的( )。
A.②④⑥ B.③⑤⑥ C.①②④ D.①③⑤
9.试预测下列物质中不具备漂白性的是( )。
A.Na2O B.Na2O2 C.HClO D.NaClO
10.实验室中需要配制2mol・L-1的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )。
A.950mL,111.2g B.500mL,117g
C.1000mL,117g D.任意规格,111.2g
11.可以用于除去氯气中水蒸气的干燥剂是( )。
A.碱石灰 B.浓硫酸 C.生石灰 D.固体烧碱
12.自来水可以用氯气消毒。如果实验室中临时没有蒸馏水,可以用自来水配制某些急需的药品,但有些药品若用自来水配制,则明显会导致药品变质。下列哪些药品不能用自来水配制( )。
A.Na2SO4 B.NaCl C.AgNO3 D.AlCl3
13.下列有关气体摩尔体积的描述中正确的是( )。
A.单位物质的量的气体所占的体积就是气体摩尔体积
B.通常状况下的气体摩尔体积约为22.4L
C.标准状况下的气体摩尔体积约为22.4L
D.相同物质的量的气体摩尔体积也相同
14.2mol Cl2和2mol CO2相比较,下列叙述中正确的是( )。
A.分子数相等 B.原子数相等 C.体积相等 D.质量相等
15.下列物质中,不能使干燥的有色布条褪色的是( )。
A.Cl2 B.氯水 C.NaClO溶液 D.Na2O2与水反应后的溶液
16.一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H2 0.2g,则被氧化的钠是( )。
A.9.2g B.10.6g C.6.2g D.4.6g
17.下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应的本质并不改变的是( )。
A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.木炭(C)和O2
18.右图是一种试验某气体化学性质的实验装置,图中B为开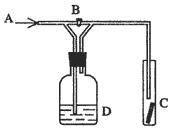 关。如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是(
)。
关。如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是(
)。
A.浓硫酸 B.饱和NaCl溶液
C.浓NaOH溶液 D.浓NaBr溶液
19.已知钡的金属活动性处于钾和钠之间。下列反应可以实现的是( )。
A.钡可以从氯化钾溶液中置换出钾
B.钡可与冷水反应并产生氢气
C.钡可以从氯化钠溶液中置换出钠
D.在溶液中,钡离子可与金属锌反应使之成为锌离子
|
| KCl | K2SO4 | ZnSO4 | ZnCl2 |
| 1 | 0.3mol | 0.2mol | 0.1mol |
|
| 2 | 0.1mol | 0.3mol |
| 0.2mol |
20.有两种体积相同的某植物的营养液,其配方如下:对于两种营养液的成分,下列说法中,正确的是( )。
A.只有K+的物质的量相等
B.只有Cl-的物质的量相等
C.完全相同
D.各离子的物质的量完全不同
(以上选择题答案务必答在第Ⅱ卷的答题栏中,否则不得分)
第Ⅱ卷(非选择题 共60分)
选择题答题表:
一、选择题(本题包括15小题,每小题3分,共45分,每小题只有一个正确答案)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 |
说明:1.答题前请将密封线内各项内容填写清楚。
2.考试结束后,只把第Ⅱ卷交回(第I卷自己保留好,以备评讲)。
二、填空题(本题包括2小题,共13分)
21.(10分)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g・mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为_______ 个。
(3)该气体在标准状况下的体积为_________L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为______ _。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为______ _。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____ g・mol-1。
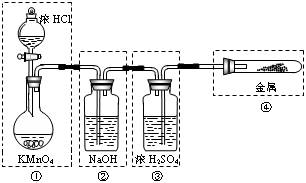
22.(3分)已知KMnO4与浓盐酸在常温下反应能产生Cl2。若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是 。
三、实验题(本题包括3小题,共40分)
23.(20分)某校环保小组处理污水样品,需配制250mL 0.1mol・L-1的盐酸溶液。试回答:
(1)请写出该实验的实验步骤
① ,② ,③ ,④ ,⑤ 。
(2)所需仪器为:容量瓶(规格: )、量筒,还需要那些实验仪器才能完成该实验,请写出: 。
(3)试分析下列操作对所配溶液的浓度有何影响及造成该影响的原因。
①为加速固体溶解,可稍微加热并不断搅拌。在未降至室温时,立即将溶液转移至溶量瓶定容。对所配溶液浓度的影响: ,原因是: 。
②定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度。对所配
溶液浓度的影响: ,原因是: 。
(4)在容量瓶的使用方法中,下列操作不正确的是____________
A.使用容量瓶前检验是否漏水
B.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近标线2~3cm处,用滴管加蒸馏水至标线。
C.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
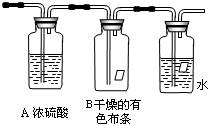
24.(10分)某同学应用如下所示装置研究物质的性质。其中气体A的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题:
(1)该项研究的主要目的是_________________。
(2)浓硫酸的作用是_______________。
(3)观察到的实验现象是____________________。
(4)从物质性质方面来看,这样的实验设计还存在事故隐患,事故表现在______。
25.(10分)实验室用一般的气体发生装置来制备氯气时,反应即使在停止加热后,还是会继续一段时间,当要收集多瓶氯气时,常有较多的氯气逸散到空气中去。氯气有毒,为了避免氯气的逸散,并对多余的氯气随时取用,有人设计了如图甲所示制取装置。试回答:
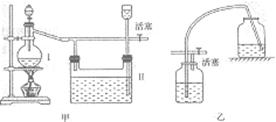
(1)设计甲装置是依据了________(填已学某仪器名称)的原理。甲中装置II_____(填“能”或“不能”)用乙装置来代替;
(2)甲中装置II盛有的液体是________,该装置可看作是一个___________(填某仪器名称),简述其主要原理。
四、计算题(本题包括2小题,共10分)
26.(4分)某温度下质量分数为22%的NaNO3 150mL,加100g水稀释后质量分数变为14%,求原溶液的物质的量浓度。
27.(6分)已知Na2O2与CO2、H2O反应的方程式是:①2Na2O2+2CO2==2Na2CO3+O2;②2Na2O2+2H2O==4NaOH+O2↑。将8.4 g 的CO2和H2O混合气体,通入足量的Na2O2中,可得O2(标准状况)2.8 L,求原混合气体中CO2与H2O的物质的量。
参考答案
一、选择题
1-5. D C B B B 6-10. D B D A C
11-15.B C C A A 16-20.D C B B C
二、填空题
21.(1)m/M (2)2mNA/M (3)22.4m/M (4)m/(m+1000) (5)m/MV
22.②③④ (提示:②中NaOH溶液会吸收Cl2,③中导管应“长进短出”,④中无加热装置,且该装置为封闭装置,不正确。)
三、实验题
23.(1)①计算 ②量取 ③溶解转移 ④洗涤转移 ⑤定容摇匀
(2)500mL 烧杯、玻璃棒、胶头滴管
(3)①偏高 因恢复到室温时,溶液的体积将小于500mL
②降低 因为溶液体积大于500mL
(4)B
24.(1)探究氯气具有漂白性的条件
(2)吸收气体A中的水
(3)干燥的布条不褪色,湿润的布条褪色
(4)没有尾气处理装置,造成环境污染
25.(1)启普发生器 能
(2)饱和食盐水 储气瓶 实验原理:关闭活塞时继续产生的Cl2被迫进入II,由于Cl2在饱和食盐水中的溶解度较小,大部分Cl2充满液面上的空间,使压强增大,将液体压入漏斗内,故保存在瓶II中的Cl2可以随时开启活塞取用。
(提示:该实验欲制取Cl2并对过量反应产生的Cl2随取随用,不难想到启普发生器的原理,再从甲中II图可以推测这不是一个洗气瓶(进气管太短),而应该是一个排液装置,我们就应考虑为何要排液?题目要求多余的Cl2随取随用,可推知II中所盛放的液体必然不能溶解Cl2,故应为饱和食盐水,即此装置相当于一个储气瓶。仔细观察不难发现,甲中II与乙形异实同。)
26.(1)按住橡皮塞,将大头针向上拔出,使钠块落入水中。
(2)钠在水和煤油接触的界面上岗上下沉浮,不断减小直至消失,同时有气泡产生。
四、计算题
27.解:设原混合气体中CO2和H2O的物质的量分别为2x、2y,
2Na2O2 + 2CO2 = 2Na2CO3 + O2
2x x
2Na2O2 + 2H2O = 4NaOH + O2↑
2y y
2x×44 g・mol-1+2y×18 g・mol-1=8.4 g……①
x+y=2.8 L /22.4L・mol-1=0.125 mol……②
解①和②所组成的方程组,
得x=0.15 mol y=0.1 mol