高一化学第一学期试题卷
相对原子质量: H:1 He:4 C:12 N:14 O:16 Na:23 Mg:24 S:32 Cl:35.5 K:39 Br:80
第Ⅰ卷(选择题 共70分)
一、选择题(10×3分=30分,每小题只有一个选项符合题意。)
1.以下是一些常用的危险品标志图标,在装运乙醇的包装箱上应贴的图标是




A B C D
2.下列实验操作中,正确的是
A.为了使过滤速度加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动
B.为了防止液滴外洒,应将胶头滴管伸入容器内再挤捏胶头
C.为加速固体物质的溶解可采用粉碎、振荡、搅拌、加热等方法
D.为增大气体物质的溶解度,常采取搅拌、加热等措施
3.下列有关实验室一般事故的预防和处理方法中,合理的是
A.皮肤上沾有少量浓硫酸,可立即用大量水冲洗,然后再涂上稀的碳酸氢钠溶液
B.若实验室发生火灾,应立即打开门窗(或排风扇)通风透气
C.在蒸馏操作过程中,发现忘了加沸石,便立即打开橡胶塞添加
D.蒸发食盐溶液时,发生液滴飞溅现象,应立即加水冷却
4.下列实验基本操作(或实验注意事项)中,主要不是从实验安全角度考虑的是
A.酒精灯内的酒精用量一般不超过其容积的2/3,也不少于其容积的1/3
B.用氢气还原氧化铜时,应先通入氢气一会儿,然后再点燃酒精灯加热
C.实验室用高锰酸钾制取氧气结束时,应先将导管从水中取出,然后再停止加热
D.在分液操作中,应将上层液体从分液漏斗的上口倒出
5.过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤................................................................... ,下列操作顺序不合理的是
A.③②①⑤④ B.③①②⑤④ C.②③①⑤④ D.①③②④⑤
6.下列混合物的分离和提纯方法中,主要不是从物质的溶解性角度考虑的是
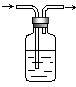 A.过滤 B.蒸馏 C.结晶 D.萃取
A.过滤 B.蒸馏 C.结晶 D.萃取
7.化学实验中的很多气体是用盐酸来制取的,这就导致了这些制取的气体
中往往含有HCl杂质,要除去HCl杂质而得到纯净的目标气体,可用右
图所示装置。如果广口瓶中盛装的是饱和NaHCO3溶液,则下列气体中
可用该装置除杂是
A.H2 B. Cl2 C. H2S D.CO2
8.下列物质中,在标准状况下所占体积最大的是
A.28gN2 B.48gO2 C.50gHCl D.100gBr2
9.下列气体中,所含原子数最多的是A
A.1.5g H2 B.5g C2H6 C.7g CO D.14g N2
10.有一种气体在标准状况下体积是4.48升,质量是14.2g,则该气体的摩尔质量是
A.28.4 B.28.4g・mol-1 C.71 D.71g・mol-1
二、选择题(每题4分,每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
11.下列物质溶于水能电离出的Cl― 数目,一定与1 mol BaCl2溶于水电离出的Cl― 数目相同的是
A.2 molKClO3 B.22.4LHCl气体 C.2 molNaCl D.1 mol AlCl3
12.下列溶液中的氯离子的物质的量浓度与50 mL 1 mol・L-1的AlCl3溶液中氯离子物质的量浓度相等的是 ( )
A.150 mL 1 mol・L-1的NaCl B.75 mL 2 mol・L-1的NH4Cl
C.150 mL 3 mol・L-1的KCl D.75 mL 2 mol・L-1的CaCl2
13.现有四组混合液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质碘的水溶液 ④石灰浆,分离以上各混合液的正确方法依次是
A.过滤、分液、萃取、蒸馏 B.萃取、蒸馏、过滤、分液
C.分液、蒸馏、萃取、过滤 D.蒸馏、过滤、萃取、分液
14.在同温同压下,相同体积的N2、O2的混合气体与NO气体相比,含有相同的
A.分子数 B.原子数 C.质子数 D.质量
15.设NA为阿伏加德罗常数的数值,Vm为气体摩尔体积的数值,则下列说法中正确的是
A.2.4g金属镁所含电子数目为1.2NA B.标准状况下22.4L CCl4所含分子数目为NA
C.Vm 体积CH4所含质子数目为10NA D.18g NH4+所含中子数目为10 NA
16.下列说法正确的是( )
(A)在标准状况下,1mol水和1molH2的体积都约是22.4L
(B)2gH2和44gCO2的体积相等
(C)1mol某气体的体积为22.4L,则该气体一定处于标准状况
(D)在标准状况下,1gH2和11.2LO2的物质的量相等
17.下列说法正确的是
A.1 mol 氮的质量为28 g
B.标准状况下,1L无水乙醇(C2H5OH)完全燃烧后生成CO2的物质的量为1/11.2 mol
C.1mol・L-1的氨水是指每1L该溶液中溶解了1 mol NH3,而不是含有1 mol NH3
D.将18.4mol・L-1的浓硫酸沿烧杯内壁慢慢地加入等体积的水中,并不断地用玻璃棒搅拌,所得硫酸溶液的物质的量浓度变为9.2mol・L-1
18.容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的 ( )
A.②④⑥ B.③⑤⑥ C.①②④ D.①③⑤
19.下列叙述正确的是 ( )
A.同温同压下,相同体积的物质,其物质的量一定相等
B.任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C.1L一氧化碳气体一定比1L氧气的质量小
D.相同条件下的一氧化碳气体和氮气,若体积相等,则质量一定相等
20.实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是 ( )
A.950mL,111.2g B.500mL,117g C.1000mL,117g D.任意规格,111.2g
第Ⅱ卷(非选择题 共30分)
班别 姓名 得分
21.(10分)现有m g某气体,它是由双原子分子构成,它的摩尔质量为M g・mol-1。若阿伏加德罗常数的数值用NA表示,则:
(1)该气体的物质的量为 mol。 (2)该气体所含原子总数为 个。
(3)该气体在标准状况下的体积为 L。
(4)若该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 。
(5)若该气体溶于1L水后所得溶液的密度为ρ g・cm-3,其物质的量浓度为 mol/L。
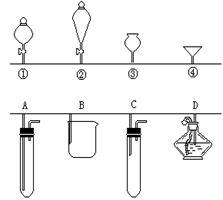 22.(8分)右图中的①、②、③、④分别是几种常见漏斗的上部,A、B、C、D分别是实际操作时,各漏斗的下部插入容器的示意图。
22.(8分)右图中的①、②、③、④分别是几种常见漏斗的上部,A、B、C、D分别是实际操作时,各漏斗的下部插入容器的示意图。
请根据实际使用上述漏斗操作时的使用范围和它们的形状,指出:①与____ 组合,用于制取气体(或滴加液体);
②与 组合,用于 ;③与___ 组合,
用于制取气体(或添加液体);④与___ 组合,用于 ___ 或④与___ 组合,用于 。
23.(12分)在某次实验中,要用500mL 0.52 mol・L-1的NaOH
溶液,回答下列问题:
(1)实际配制时,应用托盘天平称取NaOH固体 g;
(2)若在称量样品时,药品放在天平的右盘上,砝码放在天平的左盘上,1g 以下移动游码,天平平衡时实际称得的NaOH固体质量是 g
(3)配制NaOH溶液时需用的主要仪器有托盘天平(附砝码、镊子)、药匙、量筒、烧杯、胶头滴管、 和 ;
(4)下列操作对所配浓度有何影响(填写字母)?
偏大的有 ;偏小的有 。
A、称量时用了生锈的砝码; B、将NaOH放在纸张上称量;
C、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中; E、定容时俯视刻度线;
D、往容量瓶转移时,有少量液体溅出; F、容量瓶未干燥即用来配制溶液;
G、定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
以下为附加题:
26.(14分)某样品中含有碳酸钠及少量的硫酸钠和氯化钠。某学生为了检验其成分,按照下图所示步骤进行实验。
(1)请用适当的文字和化学式将所加试剂及有关结论填写在相应的空格中。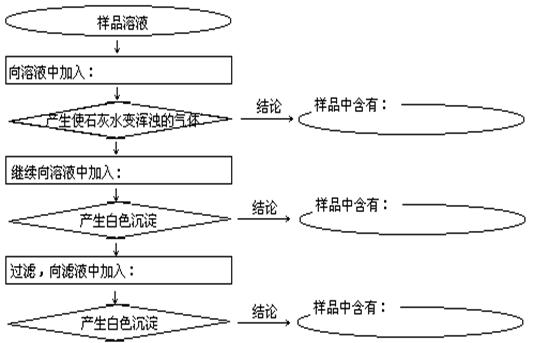
(2)若在此实验过程中要将溶液中的SO42-沉淀完全,其操作方法是
;
(3)若在此实验过程中要将过滤后的沉淀进行洗涤,其操作方法是
;检验此沉淀是否洗涤干净的操作方法是
。
请把选择题答案填入下表:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 |
高一年级第一次月考
化学试题参考答案及评分标准
第Ⅰ卷(选择题 共70分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | D | C | A | D | D | B | D | B | A | D |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | C | C | C | AB | AC | D | C | D | BD | C |
第Ⅱ卷(非选择题 共80分)
21.(2分×5 == 10分)
(1)m/M (2)2 mNA/M (3)22.4 m/M
(4)m/(m+1000)×100% (5)1000ρm/M(m+1000)
22.(每空1分,共8分)
①与C组合 ②与B组合 用于分液 ③与A组合
④与B组合 用于过滤或④与D组合 用于(向酒精灯内)添加酒精
23.(共12分)
(1)10.4g(2分) (2)9.6g(2分)
(3)玻璃棒(1分) 500 mL的容量瓶(1分)
(4)偏大的有A、C、E;(3分) 偏小的有B、D、G(3分)
注意:其他合理答案均参照给分。
24.(共14分)
(1)足量稀HNO3 Na2CO3 足量Ba(NO3)2溶液 Na2SO4 AgNO3溶液 NaCl(每个1分)
(2)静置,继续向上层清液中滴加硝酸钡溶液,若有白色沉淀生成,则SO42-没有沉淀完全;若没有白色沉淀生成,则SO42-已沉淀完全(2分) 调整滤纸的三层重叠多少,使滤纸的倾角与漏斗的倾角一致(2分)
(3)沿玻璃棒向过滤器中加蒸馏水至淹(或浸)没沉淀,待水过滤完后再重复上述两到三次操作(2分) 用试管(或小烧杯)取最后的洗涤液少许,滴加几滴硝酸银(或硫酸钠或其他合理的)溶液,若有白色沉淀生成,则未洗涤干净;若没有白色沉淀生成,则已洗涤干净(2分)