高二文科化学第一学期期中考试
化学试卷(文科)
时间:75分钟
可能用到的相对原子质量:H―1;C―12;N―14;O―16;S―32;Cl―35.5
一、单选题(本题包括20小题,每小题3分,共60分。每小题只有一个选项符合题意)。
1、下列物质中不能发生水解反应的是…………………………………………………( )
A.、淀粉 B、纤维素 C、葡萄糖 D、蛋白质
2.、假酒中所含有的有毒成分主要是……………………………………………………( )
A、CH3CH2OH B、CH3OH C、CH3COOH D、CH3COOCH2CH3
3、鉴别织物成分是真丝还是人造丝,简单可行的操作方法是…………………………( )
A、滴加氢氧化钠溶液 B、滴加浓硫酸 C、滴加酒精 D、灼烧
4、酒精能用于消毒,主要是它对蛋白质起了……………………………………………( )
A、变性作用 B、还原作用 C、盐析作用 D、溶解作用
5、正常雨水的PH大约是…………………………………………………………………( )
A、5.6 B、6.5 C、7.0 D、8.0
6、下列各组都属于人体内常量元素的是………………………………………………( )
A、铜、铁 B、锌、硒 C、氮、氢 D、碘、氟
7、油炸虾条、薯片等容易挤碎的食品,不宜选用真空袋装,而应采用充气袋装。下列气体中最不应该充入的是……………………………………………………………( )
A、氮气 B、氧气 C、空气 D、二氧化碳
8、现代以石油化工为基础的三大合成材料是…………………………………………( )
①合成氨 ②塑料 ③医药 ④合成橡胶 ⑤合成尿素 ⑥合成纤维 ⑦合成洗涤剂
A、②④⑥ B、②④⑦ C、①③⑤ D、④⑤⑥
9、把NaOH溶液和CuSO4 溶液按适当比例加入某人的尿液中,加热后,如果观察到红色沉淀出现,则此人尿液中含有…………………………………………………………( )
A、蛋白质 B、食盐 C、葡萄糖 D、食醋
10、“垃圾是放错了地方的资源”,应分类回收利用。生活中废弃的废纸、塑料袋、旧轮胎等都属于……………………………………………………………………………( )
A、有机物 B、合成材料 C、无机物 D、天然材料
11、家庭生活中所用的铁锅,在下列哪种情况下最容易生锈…………………………( )
A、用水洗涤后烘干 B、用水洗涤后未擦干 C、炒过菜未洗涤 D、加满水的
12、下列对有关药物的叙述正确的是……………………………………………………( )
A、麻黄是一种中药,呈碱性,对人体没有副作用
B、碘酊中含有碘,主要以碘离子形式存在
C、青霉素发现的伟大之外在于它适用于任何人
D、碳酸氢钠、碳酸镁等都可用于抗酸药物
13、人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒, 因为亚硝酸盐会使Fe2+离子转变成Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有………………………………( )
A、碱性 B、还原性 C、氧化性 D、酸性
14、下列物质具有固定熔、沸点的是……………………………………………………( )
A、硬铝 B、玻璃 C、水泥 D、水银
15、下列说法中,正确的是………………………………………………………………( )
A、铅笔芯的主要成分是铅 B、CO有毒,冬天生火取暖时,室内多放几盆水即可吸收CO
C、臭氧层的破坏对人的健康有害 D、绿色食品绿颜色的食品
16、商品“纯净水”、“太空水”、“蒸馏水”等作为日常饮用水,因缺少某些成分而不利于儿童身体健康发育,你认为制备上述商品饮用水时至少还需要添加的化学物质是( )
A、含碘酸钾的食盐 B、钙、镁的碳酸氢盐 C、漂白粉消毒剂 D、小苏打
17、下列不是室内污染物的是…………………………………………………………( )
A、CO B、甲苯 C、尼古丁 D、食品袋
18、下列食品中属于碱性食品的是……………………………………………………( )
A、鸡肉 B、猪肉 C、柠檬 D、鱼肉
19、钢铁发生吸氧腐蚀时,正极上发生的电极反应是…………………………………( )
A、2H+ + 2e- == H2↑ B、Fe2+ + 2e- == Fe
C、2H2O + O2 + 4e- == 4OH- D、Fe3+ + e- == Fe2+
20、在四种化合物①NaHCO3 ②Al(OH)3 ③Al2O3 ④H2N-CH2-COOH中跟盐酸和氢氧化钠溶液都能反应的是…………………………………………………………………( )
A、只有②④ B、只有①② C、只有①②③ D、①②③④
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 |
二、填空题
21、(12分)人们为保证身体健康,生病时需要服药,但药品通常既有治疗作用,又有副作用.据此回答:
(1)(6分)阿司匹林是一种治疗 且具有 等作用的西药.其结构简式为 但长期服用有_____________________等不良反应。工业上制备阿司匹林的反应方程式为: 。
(2)(2分)麻黄碱是一种用治疗 的中草药,但具有副作用,属于 剂。
(3)(4分)抗酸药是治疗胃酸过多的一类药品.请写出以下几种抗酸药中和胃酸过多的离子方程式:
① Al(OH)3:
② NaHCO3:
22、(8分)X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收。已知X是化石燃料燃烧的产物之一,是形成酸雨的主要物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应。请写出下列反应的化学方程式。
(1)X溶于雨水,形成酸雨 、
(2)Y与NaOH溶液反应 ;
(3)Z与水反应 。
23、(4分)链状结构的塑料具有_______ __性,而多数网状结构的塑料一经加工成型就不会受热熔化,因而具有 性。聚乙烯塑料的单体为 (写结构简式),它属于 塑料
24、(5分)氨基酸是具有两性特点的有机物,在结构上都具有的官能团名称是___________、___________。我们从食物中摄取的____________在胃液中的胃蛋白酶和胰蛋白酶的作用下发生__________反应,生成氨基酸,它被人体吸收后,重新合成人体所需要的各种_________________。
25、(6分)汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO和NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式_________________________________________________________________
(2)“催化转换器”的缺点是在一定程度上提高空气的酸度,其原因是______________________________________________________
(3)控制城市空气污染源的方法可以有 。
A、开发氢能源 B、使用电动车 C、植树造林 D、戴上呼吸面具
三、计算(5分)
26、煤等化石燃料燃烧时产生的SO2会对大气造成污染。如果某火力发电厂每秒燃烧10 kg 煤,煤中硫元素的质量分数为1%。假设煤中的硫全部转化为SO2,试计算该发电厂每天产生的SO2的物质的量是多少?
化学试卷(文科)答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | B | D | A | A | C | B | A | C | A |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | B | D | B | D | C | B | D | C | C | D |
![]() 21、(1)(6分) 感冒 、 解热镇痛 、
、胃肠道反应和水杨酸反应 、
21、(1)(6分) 感冒 、 解热镇痛 、
、胃肠道反应和水杨酸反应 、
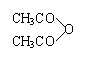 | |||||||
![]() +
+ CH3COOH
+
+ CH3COOH
(2)(2分) 支气管哮喘 、 兴奋
(3)(4分)Al(OH)3: Al(OH)3+3H+=Al3++3H2O
NaHCO3: HCO3-+H+ = H2O+CO2↑
22、(8分)(1) SO2+H2O = H2CO3 、 2H2CO3+O2 = 2H2SO4
(2) Cl2+2NaOH = NaCl+NaClO+H2O
(3) 3NO2+2H2O = 2HNO3+NO
23、(4分) 热塑 、 热固 、 CH2=CH2 、 热塑性
24、(5分) 羧基 、 氨基 、 蛋白质 、 水解 、 蛋白质
25、(6分)(1) 2CO+2NO = N2+2CO2
(2) SO2转化为SO3,产生硫酸酸雾
(3) AB
26、(5分)解:n(SO2) = n(S) = 1000g/kg×10kg×1%×24×3600/32g/mol=270000mol
答:该发电厂每天产生的SO2的物质的量为270000mol。