高二理科化学上学期期末考试试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分,时间90分钟,
能用到的相对原子质量: H:1 C:12 N:14 O:16 Na:23 AI:27 S:32 Fe:56 Zn:65
第I卷(选择题50分)
一、选择题(本题包括10小题,每小题只有一个正确答案,每小题2分共20分)
1、与KSCN溶液反应,使溶液呈红色的物质是
A.FeCl2溶液 B.FeCl3溶液
C.NaCl溶液 D.CuCl2溶液
2、下列物质中,不能用单质直接化合而得到的是:
A. FeCl3 B. FeCl2
C. FeS D. Fe3O4
3、下列烷烃的一氯代物没有同分异构体的是:
A. 2-甲基丙烷 B. 丙烷
C. 丁烷 D. 乙烷
4、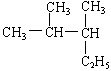 的名称是
的名称是
A. 2—甲基—3—乙基丁烷 B. 3,4—二甲基戊烷
C. 2,3—二甲基—4—乙基丙烷 D. 2,3—二甲基戊烷
5、下列叙述中错误的是:
A.点燃甲烷不必象点燃氢气那样事先验纯
B.甲烷燃烧能放出大量的热,所以是一种很好的气体燃烧
C.煤矿的矿井要注意通风和严禁烟火,以防爆炸事故的发生
D.如果隔绝空气,将甲烷加热到1000℃以上,能分解成炭黑和氢气
6、下列化学反应的化学能可直接转变成电能的是
A.2FeCl3+Cu=CuCl2+2FeCl2
B.AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl
C.2Fe(OH)3 =Fe2O3+3H2O
D.Na2O+CO2=Na2CO3
7、甲溶液的PH为4,乙溶液的PH为2,则甲、乙两溶液的c(H+)的大小为
A.甲>乙 B.甲=乙
C.甲<乙 D.无法判断
8、下列各组烃的混合物,只要总质量一定,无论它们按何种比例混合,完全燃烧后生成的CO2和H2O都是恒量的是( )
A. C2H2、C2H4 B. C2H4、C3H6
C. C2H6、C3H8 D. CH4、C2H2
9、物质的量浓度都是0.1摩/升的下列各溶液中,PH值最大的是:
A. HCl B. Al2(SO4)3
C. H2SO4 D. CH3COONa
10、能证明乙醇中含有水的试剂是
A.无水硫酸铜粉末 B.新制生石灰
C.金属钠 D.胆矾
二、选择题(本题包括10小题,每小题只有一个正确答案,每小题3分共30分)
11、下列事实与胶体性质无关的是
A. 在豆浆里加入盐卤做豆腐
B.河流入海处易形成沙洲
C.一束平行光照射蛋白质溶液时,从侧面可以看到一条光亮的通路
D.往氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
12、若溶液中由水电离产生的c(OH-)=1×10-14 mol·L-1,满足此条件的溶液中一定能大量共存的离子组是
A.Al3+ Na+ NO3- Cl- B.K+ Na+ Cl- NO3-
C.K+ Na+ Cl- HCO3- D.K+ Fe2+ SO42- NO3-
13、在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是
A.CH4和C2H4 B.CH4和C2H6
C.C2H4和C2H6 D.C3H4和C3H6
14、甲烷分子中的4个氢原子都可以被取代,若它们都被苯基取代,则可得到的物质分子的结构简式如右图所示,对该分子的下列描述中,不正确的是
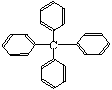 A.分子式为C25H20
A.分子式为C25H20
B.此物质属于芳香烃
C.此物质是非极性分子
D.所有碳原子都在同一平面内
15、NA为阿佛加德罗常数的值,下列说法正确的是
A.标准状况下,11.2L的戊烷所含的分子数为0.5NA
B.28g乙烯所含共价键数目为NA
C.标准状况下,铝和NaOH溶液反应生成11.2L气体时,电子转移数为NA
D.1L 1mol/L的FeCl3溶液中的Fe3+的个数为NA
16、将agFe2O3、Al2O3样品溶解在过量的200mL pH=1的硫酸溶液中,然后向其中加入NaOH溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为
A.0.1mol·L-1 B.0.2mol·L-1
C.0.4mol·L-1 D.0.8mol·L-1
17、法国化学家伊夫·肖万获2005年诺贝尔化学奖。他发现了烯烃里的碳-碳双键会被拆散、重组,形成新分子,这种过程被命名为烯烃复分解反应 。烯烃复分解反应可形象地描述为交换舞伴。(如图所示)
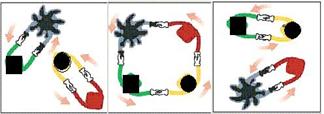
烯烃复分解反应中的催化剂是金属卡宾(如CH2==M),金属卡宾与烯烃分子相遇后,两对舞伴会暂时组合起来,手拉手跳起四人舞蹈。随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴。后者会继续寻找下一个烯烃分子,再次“交换舞伴”。把C6H5CH2CH==CH2与CH2==M在一定条件下混合反应,下列产物不可能存在的是
A.C6H5CH2CH==M B.CH2= CH2
C.C6H5CH2 CH2 C6H5 D.C6H5CH2CH==CH CH2 C6H5
18、在一个固定体积的密闭容器中,加入2 molA和1 molB发生如下反应:2A(g)+B(g) ![]() 3C(g)十D(s),达到平衡时C的浓度为1.2 mol/L。若维持容器体积和温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2 mol/L的是
3C(g)十D(s),达到平衡时C的浓度为1.2 mol/L。若维持容器体积和温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2 mol/L的是
A.4 mol A十2 mol B
B.3 mol C+1 mol D+l mol B
C.3 mol C十0.8 m01 D
D.1.6 mol A+0.8 mol B+0.6 mol C+0.3 mol D
19、在体积都为1L,pH都等于2的盐酸和醋酸溶液中,投入0.65g锌粒,则下图所示比较符合客观事实的是
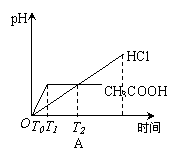 | 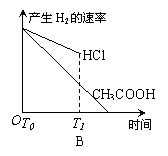 | |||||
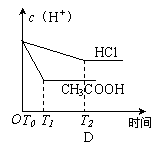 | ||||||
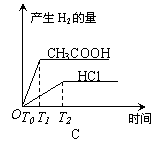 | ||||||
20、美国康乃尔大学的魏考克斯(C. Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛。因而称为释迦牟尼分子(所有原子在同一平面)。
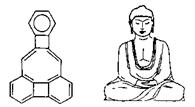
有关该有机分子的说法不正确的是
A.该有机物属于芳香烃 B.该有机物属于苯的同系物
C.该有机物分子中含有22个碳原子 D.该有机物一氯代物只有6种
高二化学(理科)答题卡
第I卷(选择题50分)
一、二、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 |
第Ⅱ卷(非选择题50分)
三、填空题(本题包括4小题,共26分)
![]() 21、(8分)已知某有机物的结构简式为: CH2=CH-CH-CH2OH
21、(8分)已知某有机物的结构简式为: CH2=CH-CH-CH2OH
CH3
(1)该有机物中所含官能团的名称是_______________________________。
(2)该有机物发生加成聚合反应后,所得产物的结构简式为_____________ _。
(3)写出该有机物发生消去反应的化学方程式(注明反应条件):
_____________________________________________________________ _
22、(6分)把下列物质的相互关系填入下表中的空格中(填序号)
①同种物质 ②同位素 ③同系物 ④同素异形体 ⑤同分异构体
| 物质名称 | 相互关系 |
| 丙烷与2-甲基丙烷 | |
| 金刚石和石墨 | |
| 辛烷与壬烷 | |
| 氯仿与三氯甲烷 | |
| 氕、氘、氚 | |
| 新戊烷与2-甲基丁烷 |
23、(4分)在实验室进行的下列实验中,有关仪器的下端必须插入液面以下的
是 (填编号)。
①分馏石油时用的温度计
②制备乙烯时用的温度计
③用水吸收溴化氢的导管口
④用碱液吸收多余氯气的导管口
⑤制备H2的简易装置中加入稀硫酸用的长颈漏斗
⑥制备Fe(OH)2时,向FeSO4溶液中滴入NaOH溶液用的胶头滴管
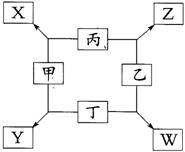
24、(共8分)如图所示已知:
①甲、乙、丙、丁均为前三周期元素的单质。
②在一定条件下甲与丙和甲与丁都按物质的量之比1:3反应,分别生成X和Y,在产物中元素甲呈负价。
③在一定条件下乙与丙和乙与丁都按物质的量之比1:2反应,分别生成Z和W,在产物中元素乙呈负价。请填空:
(1)甲是 ,乙是 。
(2)甲与丙反应生成X的化学方程式是
(3)乙与丁反应生成W的化学方程式是
四、实验题(本题包括1小题,共14分)
|
(1)写出生成烯的化学方程式
;
(2)浓硫酸的作用是 ;
(3)I试管中的现象有 ,
反应的化学方程式为 ;
II试管中发生的反应属于 反应(填反应类型);
(4)实验的最后阶段,反应混合物的液体会变黑色,并有气体杂质生成,要除
去这些杂质,应在洗气瓶中装入 溶液;
若无此装置,I试管中还可能发生另外一个反应,该反应的离子方程式为
(5)验纯后,在导管末端点燃生成的气体,所观察到的现象是
, 反应的化学方程式是
五、计算题(本题包括1小题,共10分)
26、(10分)已知某化合物甲,分子中只含C、H、O三种元素,相对分子质量小于200,其C、H的质量分数合计为78.4%。又已知甲分子中有一个碳原子它的四个价键分别连在四个不同的原子或原子团上。
(1)写出甲可能的分子式。
(2)写出甲可能的其中一种结构式。
高二化学(理科)参考答案
第I卷(选择题50分)
一、二、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | B | B | D | D | A | A | C | B | D | A |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | D | B | A | D | C | B | C | D | C | B |
第Ⅱ卷(非选择题50分)
三、填空题(本题包括4小题,共26分)
21.(共8分)
[1](各2分)碳碳双键、羟基;
[2](2分)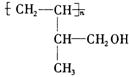
[3](2分)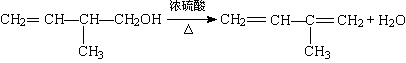
22、(各1分共3分) ③ ④ ③ ① ② ⑤
23、 ②④⑤⑥(4分)
24、(1)氮 氧(各2分)
(2)N2+3H2![]() 2NH3 (2分)
2NH3 (2分)
(3)O2+2Mg ![]() 2MgO(2分)
2MgO(2分)
四、实验题(本题包括1小题,共14分)
|
![]() (1)CH3CH2OH
CH2=CH2↑+H2O
(2分)
(1)CH3CH2OH
CH2=CH2↑+H2O
(2分)
(2)催化剂、脱水剂 (2分)
(3)溴水褪色,试管底部有少量油状物 (1分)
![]() CH2
CH2 CH2+Br2
CH2—CH2 (2分)
氧化(1分)
|
|
(4)NaOH(1分) SO2+Br2+2H2O=SO42-+2Br-+4H- (2分)
(5)火焰明亮,并伴有黑烟 (1分)
|
![]() CH2
CH2
CH2+3O2 2CO2+2H2O (2分)
五、计算题(本题包括1小题,共10分)
26、(10分)
(1)C4H10O (2分) ; C9H8O2 (2分)
(2) H OH
![]()
![]()
![]()
![]()
![]() CH3 C CH2CH3 HC≡C- C -
(各3分)
CH3 C CH2CH3 HC≡C- C -
(各3分)
![]()
![]() OH
H
OH
H
有其它合理的答案可参照给分。
![]()