高二级化学月考试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,第Ⅰ卷(第1题至18题),第Ⅱ卷(第19题至25题)。共110分,考试时间100分钟。
一、选择题(本题包括18小题,每小题3分,共54分。每小题只有一个选项符合题意)
1、对于反应A2+3B2![]() 2AB3以下表示的反应速率中,速率最小的是:
2AB3以下表示的反应速率中,速率最小的是:
A.VA2 = 0.4 mol·L-1min-1 B.VB2 = 0.8 mol·L-1min-1
C.VAB3 = 0.6 mol·L-1min-1 D.VA2 = 0.01 mol·L-1·S-1
2、对已达化学平衡的下列反应 2X(g)+Y(g)![]() 2Z(g)减小压强时,对反应产生的影响是:
2Z(g)减小压强时,对反应产生的影响是:
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
3、在一定温度下将1molCO和1molH2O(g)通入一个密闭容器中反应:
CO(g)+H2O(g![]() CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g)达到平衡后CO2的物质的量可能是 :
CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g)达到平衡后CO2的物质的量可能是 :
A.等于0.6mol B.等于1mol
C.大于1mol D.大于0.6mol,小于1mol
4、对于反应2SO2+O2![]() 2SO3,下列判断正确的是:
2SO3,下列判断正确的是:
A.2体积SO2和足量O2反应,必定生成2体积SO3
B.其他条件不变,增大容器体积,平衡必定向右移动
C.平衡时,SO2消耗速度必定等于O2消耗速度
D.平衡时,SO2浓度必定等于O2浓度的两倍
5、在某密闭容器中存在下列化学平衡: aA(g)![]() bB(g) + cC(g), 在温度不变的条件下,再充入一定量的A物质, 重新达到平衡时, 下列判断中正确的是:
bB(g) + cC(g), 在温度不变的条件下,再充入一定量的A物质, 重新达到平衡时, 下列判断中正确的是:
A.若a = b + c, B的物质的量分数变大
B.若 a = b + c , B 的物质的量分数不变
C.若a > b + c时, A的转化率不变
D.若 a < b + c时 , A的转化率变大
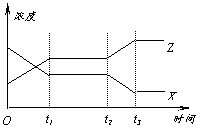 6、今有反应X(g)+Y(g)
6、今有反应X(g)+Y(g) ![]() 2Z(g)(正反应放热)。右图表示该反应在t1时达到平衡,在t2时因改变某个条件而发生变化的曲线。则下图中的t2时改变的条件是
2Z(g)(正反应放热)。右图表示该反应在t1时达到平衡,在t2时因改变某个条件而发生变化的曲线。则下图中的t2时改变的条件是
A.升高温度或降低Y的浓度
B.加入催化剂或增大X的浓度
C.降低温度或增大Y的浓度
D.缩小体积或降低X的浓度
7、将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应 2A(g)+B(g)![]() 2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1③ 2 s 时物质 A 的转化率为70% ④ 2 s 时物质 B 的浓度为 0.7 mol·L-1其中正确的是:
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1③ 2 s 时物质 A 的转化率为70% ④ 2 s 时物质 B 的浓度为 0.7 mol·L-1其中正确的是:
A.①③ B. ①④ C.②③ D.③④
8、在一定温度下的定容密闭容器中,当下列物理量不再改变时,表明反应:
A(s)+2B(g)![]() C(g)+D(g)已达平衡的是:
C(g)+D(g)已达平衡的是:
A.混合气体的压强 B.混合气体的密度
C.B的消耗速率等于D的生成速率 D.气体的总物质的量
9、某可变的密闭容器中,盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B![]() 2C。若保持温度和压强不变,当达到平衡时,容器的体积为V(L),其中C气体的体积占10%,下列推断正确的是:
2C。若保持温度和压强不变,当达到平衡时,容器的体积为V(L),其中C气体的体积占10%,下列推断正确的是:
A.原混合气体的体积为1.2V(L)
B.原混合气体的体积为1.1V(L)
 C.反应达平衡时气体A消耗掉0.15V(L)
C.反应达平衡时气体A消耗掉0.15V(L)
D.反应达平衡时气体B消耗掉0.05V(L)
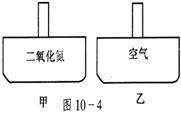
10、常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器(如图10-4)里,分别充有二氧化氮和空气,现分别进行下列两项实验:
(a)将两容器置于沸水中加热
(b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是:
A.(a)甲>乙(b)甲>乙 B.(a)甲>乙(b)甲<乙
C.(a)甲<乙(b)甲>乙 D.(a)甲>乙(b)甲=乙
11、一定条件下反应mA(g)+ nB(g)![]() pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度v(C)= 2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是:
pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度v(C)= 2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是:
A.2、6、3、5 B.3、1、2、2 C.3、1、2、1 D.1、3、2、2
12、某温度下,密闭容器中发生反应aX(g)![]() bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是:
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是:
A.可逆反应的化学计量数数:a>b+c
B.压缩容器的容积时,v正增大,v逆减小
C.达到新平衡时,物质X的转化率减小
D.达到新平衡时,混合物中Z的质量分数增大
13、同温同压下,当反应物分解了8%时,总体积也增加8%的是:
A.2NH3(g) ![]() N2(g)+3H2(g)
N2(g)+3H2(g)
B.2NO(g) ![]() N2(g)+O2(g)
N2(g)+O2(g)
C.2NO3(g) ![]() 4NO2(g)+O2(g)
4NO2(g)+O2(g)
D.2NO2(g) ![]() 2NO(g)+O2(g)
2NO(g)+O2(g)
14、两个体积相同的密闭容器A、B,在A中充入SO2和O2各1mol,在B中充入SO2和O2各2
mol,加热到相同温度,有如下反应2SO2(g)+ O2(g)![]() 2SO3(g),对此反应,下述不正确的是:
2SO3(g),对此反应,下述不正确的是:
A.反应速率B>A B.SO2的转化率B>A
C.平衡时各组分含量B = A D.平衡时容器的压强B>A
 15、下图所示的直型石英玻璃封管中充有CO气体,左端放置不纯的镍(Ni)粉。在一定条件下,Ni可以与CO(g)发生如下反应:
15、下图所示的直型石英玻璃封管中充有CO气体,左端放置不纯的镍(Ni)粉。在一定条件下,Ni可以与CO(g)发生如下反应:
 |
但Ni粉中的杂质不与CO(g)发生反应。玻璃管内左右两端的温度分别稳定在350K和470K,经过足够长时间后,右端的主要物质是 :
A.纯Ni(s)和Ni(CO)4(g) B.纯Ni(s)和CO(g)
C.不纯Ni(s)和CO(g) D.不纯Ni(s)和Ni(CO)4(g)
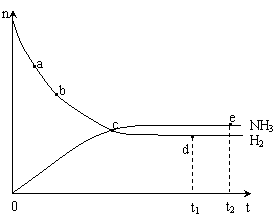 16、合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
16、合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
N2(g)+3H2(g) ![]() 2NH3(g),673K,
2NH3(g),673K,
30MPa下n(NH3)和n(H2)随时间变化的关系
如右图所示。下列叙述正确的是:
A.点a的正反应速率比点b的小
B.点 c处反应达到平衡
C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大
17、某反应:2A(g)![]() B(g)+C(g),在甲、乙两个容积都是1L而且不变的容器中进行,开始时在两个容器中均放入0.5 mol A,甲容器中3s后B的物质的量浓度达到0.18 mol/L而且保持不变,乙容器中2s时B的物质的量浓度即达到0.18mol/L,而且保持不变,则:
B(g)+C(g),在甲、乙两个容积都是1L而且不变的容器中进行,开始时在两个容器中均放入0.5 mol A,甲容器中3s后B的物质的量浓度达到0.18 mol/L而且保持不变,乙容器中2s时B的物质的量浓度即达到0.18mol/L,而且保持不变,则:
A.乙容器中使用了比甲容器更高的温度
B.乙容器中加入了某种不与体系气体反应的气体增大了容器内的压强
C.乙容器中使用了催化剂
D.乙容器中可能既升高了温度又使用了催化剂
18、金属卤化物与卤素互化可生成多卤化物,如KI+I2![]() KI3,在有关KI3的叙述中不正确的是:
KI3,在有关KI3的叙述中不正确的是:
A.I2在KI溶液中溶解度增大是由于生成了I3-离子
B.I3-离子在溶液中存在下列平衡:I3-![]() I2+I-
I2+I-
C.KI3溶液遇淀粉溶液不显蓝色
D.将Cl2通入KI3溶液中,I3-离子的浓度减小
2009级化学月考试题
Ⅰ卷答案栏
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
|
| ||||||||
| 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
第II卷 (非选择题共56分)
二、填空题(本题包括4小题,共45分)
19、(6分)反应A(g)+B(s)
![]() C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:
C(g);△H<0,在其他条件不变时,改变其中一个条件,则生成C的速率:
(1) 升温____________; (2) 增大压强________; (3) 增大容器容积__________;
(4) 加入A_________; (5) 加入B__________; (6) 加正催化剂_______________。
20、(10分)可逆反应3A(g)
![]() 3B(?)+C(?)(正反应吸热)达到化学平衡后,升高温度。用“变大”、“变小”、“不变”或“无法确定”填空。
3B(?)+C(?)(正反应吸热)达到化学平衡后,升高温度。用“变大”、“变小”、“不变”或“无法确定”填空。
⑴若B、C都是气体,气体的平均相对分子质量 ;
⑵若B、C都不是气体,气体的平均相对分子质量 ;
⑶若B是气体,C不是气体,气体的平均相对分子质量 ;
⑷若B不是气体,C是气体。
①如果A的摩尔质量大于C的摩尔质量,气体的平均相对分子质量 ;
②如果A的摩尔质量小于C的摩尔质量,气体的平均相对分子质量 。
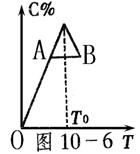 21、(8分)对于反应2A+B
21、(8分)对于反应2A+B![]() 2C的反应过程中C的百分含量随温度变化如图10-6所示,则:
2C的反应过程中C的百分含量随温度变化如图10-6所示,则:
(1)![]() 对应的v(正)与v(逆)的关系是__________________。
对应的v(正)与v(逆)的关系是__________________。
(2)正反应为____________________热反应。
(3)A、B两点正反应速率的大小关系是________________。
(4)反应温度![]() 时,C%逐渐增大的原因是__________________。
时,C%逐渐增大的原因是__________________。
22、(8分)在10℃和2´105pa的条件下,反应aA(g)
![]() dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(温度维持不变)。下表列出了不同压强下反应建立平衡时物质D的浓度。
dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(温度维持不变)。下表列出了不同压强下反应建立平衡时物质D的浓度。
| 压强/pa | 2´105 | 5´105 | 1´106 |
| D的浓度/mol·L—1 | 0.085 | 0.20 | 0.44 |
根据表中数据,回答下列问题:
⑴压强以2´105pa增加到5´105pa时,平衡向________反应方向移动(填“正”或“逆”),理由是________________________________________________________________
⑵压强从5´105pa增加到1´106pa时,平衡向________反应方向移动(填“正”或“逆”),理由是__________________________________________________________________,平衡之所以向该方向移动,可能的原因是_______________________________
_________________________________________________________________________
23、(8分)在一固定容积的密闭容器中,保持一定温度,在一定条件下进行以下反应:
A(g)+2B(g)
![]() 3C(g),已知加入1molA和3molB且达到平衡后,生成了a molC。
3C(g),已知加入1molA和3molB且达到平衡后,生成了a molC。
(1)达到平衡时,C在反应混合气中的体积分数是_____________(用含字母a的代数式表示)。
(2)在相同实验条件下,若在同一容器中改为加入2molA和6 mol B,达到平衡后,C的物质的量为 mol(用含字母a的代数式表示)。此时C在反应混合气中的体积分数与原平衡相比 (选填“增大”“减小”或“不变”)。
(3)在相同实验条件下,若在同一容器中改为加入2 mol A和8 mol B,若要求平衡后C在反应混合气中体积分数仍与原平衡相同,则还应加入C mol。
24、(10分)在一个容积固定的反应器中,有一可左右滑动的密封隔板,左、右两侧
分别进行如下可逆反应:2SO2(g) +O2(g) ![]() 2SO3(g);
2SO3(g);
3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)。左侧中加入SO2、O2、SO3的物质的量分别为
Fe3O4(s)+4H2(g)。左侧中加入SO2、O2、SO3的物质的量分别为
xmol、3.25mol、1mol;右侧中加入9mol的水蒸气和适量的铁粉(忽略铁粉体积对容
器体积的影响)。当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧
反应都达到平衡,并且隔板恰好处于反应器位置2处。请填写以下空白:
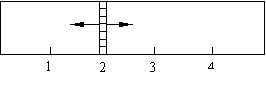 |
⑴若x=1.5,则左侧反应在起始时向 (填“正反应”或“逆反应”)方向进
行。欲使起始反应维持向该方向进行,则x的取值范围是 。
⑵若x=2,则左侧反应在起始时向 (填“正反应”或“逆反应”)方向进行,
平衡时混合气中SO2所占的体积分数为 。欲使起始反应维持向该方向进
行,则x的最大值应小于 。
三、计算题(6分)
25、(6分)将2molN2和8mol H2在适宜条件下按下式进行反应:N2+3H2![]() 2NH3,当在某一温度下达到化学平衡状态,若测得平衡混合气体对氢气的相对密度为4.0时,求N2的转化率?
2NH3,当在某一温度下达到化学平衡状态,若测得平衡混合气体对氢气的相对密度为4.0时,求N2的转化率?
答案
一、选择题
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| B | C | D | BC | B | C | B | B | B |
| 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| B | B | C | A | C | B | D | C | C |
19、增大;增大;减小;增大;不变;增大
20、⑴变小 ⑵不变 ⑶变小 ⑷①变小 ②变大
21、(1)v(正)=v(逆)
(2)放 (3)![]() (4)
(4)![]() ,可逆反应未达平衡,反应正向进行使C%增大
,可逆反应未达平衡,反应正向进行使C%增大
22、⑴逆,压强增加2.5倍,D的浓度增加小于2.5倍,则D的浓度降低,平衡逆向移动
⑵正,压强增加2倍,D的浓度增加大于2倍,平衡正向移动。E加压后,变为液态或固态,且a ﹥ d
23、(1)25a% (2)2a 不变 (3)6
24、(1)逆反应、1.25﹤x﹤1.75
(2)正反应、25% 、3.5