���б�ҵ��ѧ�ῼģ�⿼�ԣ�һ��
���� ѧ�� �ԡ� ��
�������������������� ����ʱ�䣺90���ӡ��������������� 2008��5
�ڢ��������������50�֣�
| �� �� �� ֪ | 1������Ҫ������д��λ��š� 2��������Ϊѡ���⣬ֻ��һ�����⣬��3ҳ������ǰҪ�������⣬������ĿҪ��Ҫ���������� 3�����������������2BǦ�ʰ��涨Ҫ���ڡ�������������������Ҫ��Ӧ����ͿҪ�淶�� 4�����Խ�������Ӧ���Ծ��͡�������������������ϣ����Ա�ջء� |
�����õ������ԭ��������
H��1��C��12��N��14��O��16��Na��23�� Al��27��Cl��35.5��Fe��56��Mg��24
ѡ���⣨ÿС��ֻ��һ��ѡ��������⡣ÿС��2�֣���50�֣�
1��2008��8�±������ٰ���˻ᣬ��������Ϊ�������Ĺ���֮һ�ǻ�����ʵ�е�˫�ų��С��������������Ա��Ͻ�ͨ��ͨ�������������������������ŷ���ɵĿ�����Ⱦ
A��O2���������� B��N2������������ C��NO2���������� D��Cl2
2��������������������
A��C2H5Br�������� B��C2H6�������� C��C2H5OH��������D��CH3COOH
3�����и������У���Ϊͬλ�ص���
A����![]() ��
��![]() �� B����
�� B����![]() ��
��![]() ����C����H2O��D2O�� D���� O2��O3
����C����H2O��D2O�� D���� O2��O3
4����֪ҿ��һ��ԭ����![]() �����ԭ�Ӻ��ڵ�������Ϊ
�����ԭ�Ӻ��ڵ�������Ϊ
A�� 77�� ��������B��114 ���������� C��191�� ������������D��268
5�������л���������ˮ�ұ�ˮ�����
A�� �Ҵ��������� B�����ᡡ�������� C������������������ D�����Ȼ�̼
6�����������У�����������ʵ���
A�� NaOH������������ B��NH4Cl���������������� C��CH3COOH�������� D��HCl
7�����������У��������ڼ��ȵ���
A������ƿ�������� B��Բ����ƿ��������C���Թܡ����������� D���ձ�
��ѧ�Ծ���������1ҳ����3ҳ��
8��ʵ�����ռ���������ʱ��ֻ������ˮ���ռ����ǣ��� ��
A��NO2 ������������ B��NH3 ������������C��Cl2 ������������D��NO
9���������ӵĽṹʾ��ͼ�У���ʾ�����ӵ���

10�����������У��������Ͻ����
A�� Ӳ������������ B����ͭ���������� C�� �������������� D��ˮ��
11�����е���ʽ�У���д����ȷ����
A���������������� B�������������� �� C������������������ D��
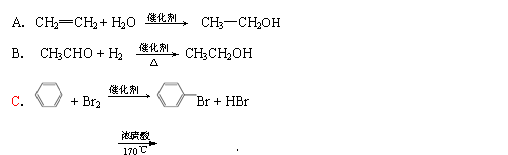
12�����з�Ӧ�У�����ȡ����Ӧ���ǡ�
13�����з�Ӧ�У�������������ԭ��Ӧ����
A��2FeCl3 + Fe ==��3FeCl2
B��2NaOH + Cl2 == NaCl + NaClO + H2O
C��Na2O + H2O��===��2NaOH
D��CuSO4 + Fe��== FeSO4 + Cu
14�����������У�ֻ�����ۼ�����
����A��NH4Cl���������� B. Na2O2������������ C��HCl ������������D��NaCl
15���������ʲ��ܷ���ˮ�ⷴӦ����
����A�������ʡ������� B�����ۡ��������� C�����ǡ����������� D��������
16�������ε�ˮ��Һ�� pHС��7����
A��Na2CO3������ �� B��NH4NO3���� ���� C��Na2SO4���������� D��KCl
17��ij�л�����������Ӧ�IJ�����CH3��CH2��CHO��ԭ�л�����
A���Ҵ���ͬϵ� B����ȩ��ͬϵ�C�������ͬ���칹�� D����ȩ��ͬ���칹��
18������˵����ȷ����
A�����ô���������ϸ��ƿʢ��NaOH��Һ
B��������ͨ��������ú������ܱ��������Ȼ�̼��
C�����Ӳ���մ��Ƥ���ϣ�����������������Һϴ��
D����NaOH����ֱ�ӷ�������ƿ�У���ˮ���̶��߾����һ�����ʵ���Ũ�ȵ�NaOH��Һ���������������������������������� ��ѧ�Ծ���������2ҳ����3ҳ��
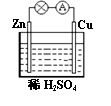 19������п��ͭ��ϡ������ɵ�ԭ��أ�����ͼ���������й�˵����ȷ����
19������п��ͭ��ϡ������ɵ�ԭ��أ�����ͼ���������й�˵����ȷ����
������ ��Zn�Ǹ��������������� ��Cu������
��Zn -2e-==Zn2+ �������� ��Cu2+ +2e-== Cu
A���٢ڡ������������������� B���٢ڢۡ���
C���ڢۢ� ������������������������D���٢ڢۢܡ�
20���������ӷ���ʽ�У���д��ȷ����
A�� CO32�� �� 2H2O === H2CO3 �� 2OH��
B��Na �� H2O === H2�� �� OH��������
C�� Al3+�� �� 3H2O ![]() Al(OH)3���� 3H+����
Al(OH)3���� 3H+����
D�� Cl2 + H2O = 2H+ + Cl- + ClO-
21�����и������ʵ����ʱȽϣ���ȷ����
A�����ԣ�HClO4��H3PO4��H2SO4������ B���⻯���ȶ��ԣ�HF��H2O ��H2S
C�����ԣ�NaOH��Mg(OH)2��Ca(OH)2�� D��ԭ�Ӱ뾶��F�� Cl�� Br �� I
22�����м������ʵ���;˵����ȷ����
A��������������������ʳ��ˮ������
B����������ϡ��Һ�����ڸ���ˮ��Ʒ����
C�����������������Ư��ijЩ��ɫ���ʣ����ò��ָ�ԭ����ɫ���ʵ���ɫ����
D������������������ά����Ҫԭ��
23�����и������ӣ���ǿ������Һ�п��Դ����������
A��Cl-��CO32-��K+�������������������� B��Na+��NH4+��NO3-
C��Na+��NO3-��Al3+�������������������� D��Ba2+��Fe3+��Cl-
24����һ�������£������ܱ������н��еĿ��淴Ӧ��N2 (g) + 3H2(g) ![]() 2NH3(g)
2NH3(g)
����˵���У��ܳ��˵����һ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬����
A��N2��H2��NH3�����ʵ���֮��Ϊ1�U3�U2
B��N2��H2��NH3��Ũ�����
C�������淴Ӧ��������Ҳ�������
D����Ӧֹͣ�������淴Ӧ���ʶ�������
|
A��CH3COH������������������������������ B��
C��CH3= CH��CH3������������������������ D��CH3COOC2H5
������������������������������������������
��ѧ�Ծ���������3ҳ����3ҳ��
��������������������������������������������������
�� �� Ϊ �� �� ֽ
�����г�����2008����ͨ���б�ҵ�ῼģ�⿼�ԣ�һ��
���� ѧ�� �ԡ� ��
�ڢ�����ǻ���������50�֣�
| �� �� �� ֪ | 1������Ҫ������д�ܷ����ڵ����ء�ѧУ�������������š������ź���λ��š� 2���ڢ�������������⣬��4ҳ������ǰҪ�������⣬������ĿҪ��Ҫ���������� 3����������ú�ɫ�ּ���ǩ�ֱʣ��ּ�Ҫ����������Ҫ���ࡣ |
| �⡡�� | һ | �� | �� | �ܡ� �� |
| �֡��� | ||||
| �ľ��� | ||||
| ������ |
�����õ������ԭ��������
H��1��C��12��N��14��O��16��Na��23�� Al��27��Cl��35.5��Fe��56��Mg��24
| �÷� | �ľ��� | һ������⣨��22�֣� |
1����3�֣���2H2SO4��Ũ����C ![]() CO2����2SO2����2H2O�ķ�Ӧ�С���Ϊ����������������������
���ѧʽ������Ϊ��ԭ������������������
���ѧʽ��������Ӧ��������
1mol SO2������������������
mol H2SO4��
CO2����2SO2����2H2O�ķ�Ӧ�С���Ϊ����������������������
���ѧʽ������Ϊ��ԭ������������������
���ѧʽ��������Ӧ��������
1mol SO2������������������
mol H2SO4��
2����3�֣��ڢ���ϩ�������ᡡ�����������������У�����Br2�����ӳɷ�Ӧ����������
������ţ���ͬ�����ܷ���������Ӧ������������ ������̼�����Ʒ�Ӧ���ɶ�����̼�����������������
��ѧ�Ծ��ڢ����1ҳ����4ҳ��
3����4�֣�ij�����ĩ���ܺ�����Cu2����Al3����K+��Cl����SO42����CO32����ɵ�һ�ֻ������ʣ��ֽ�������ʵ�飺
��ȡ�������壬����ϡ�������裬����ȫ���ܽ⣬û������ų���
�����������Һ�м���Ba(NO3)2��Һ���������ɣ��ٵ���AgNO3��Һ���а�ɫ�������ɣ�
����ȡ�������������������ˮ���������ȫ���ܽ⣬�õ���ɫ������Һ��
�����������Һ�м��백ˮ��ʹ��Һ�ʼ��ԣ��г������ɣ����ˡ���������ó����м����������������Һ������ȫ���ܽ⡣
��ɹ����ĩ�������У������е��������������������� ���϶����е����������������� �����ܿ϶����������������� ������������������ʵ�鷽�������м�����
4����4�֣��ڻ�ѧ���ϣ�Χ�ƽ������ܷ���Ũ���ᷴӦ������������ʵ��̽������һ֧�Թ��з���һС����Ƭ������Ũ���ᣬ�������ϴ����ܵĽ�������������ͨ����һ֧ʢ��NaOH��Һ���Թ��С���ش�
��1�������£��Թ���û�����Ա仯��������Ϊ��Ũ���������ı��汻 ���������������˼�����ܵ�����Ĥ������ֹ��Ӧ�ļ������С�
��2�����Թܼ��ȣ����ҷ�Ӧ��������һ�ֺ���ɫ���������������� ���ѧʽ��������������Ļ�ѧ����ʽ���������������������������������������������� ��
��3����������ʵ����������������������� ������ţ���
�����ԡ����� �ڲ��ȶ��ԡ�������ǿ�����ԡ�����
5����8�֣�����ԭ���������������A��B��C��D��E����ͬ���ڵĶ�����Ԫ�ء���֪A��C��D����Ԫ��ԭ�ӵ�������Ӳ������֮��Ϊ10��������Ԫ�ص�����������ˮ����֮�䣬�������ܷ�Ӧ�Ҿ������κ�ˮ����ش�
��1��CԪ����Ԫ�����ڱ��е�λ���������������������� ��
��2��D��E��Ԫ�ص�����������ˮ�����У����Խ�ǿ���������������� ���ѧʽ����
��3��д��A��C��Ԫ�ص�����������ˮ����֮�䷴Ӧ�����ӷ���ʽ��
�������������������������������������������������������� ��
��4����AԪ�صĹ�������19.5 g������������̼��ȫ��Ӧ���������������� mol ���ӷ���ת�ơ�
��ѧ�Ծ��ڢ����2ҳ����4ҳ��
| �÷� | �ľ��� | ����ʵ���⣨��20�֣� |
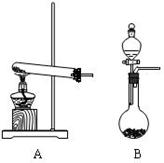 6����4�֣�ʵ������ȡ����������������������
6����4�֣�ʵ������ȡ����������������������
��1�����ù���NH4Cl��Ca(OH)2����ȡ����ʱӦѡ����ͼװ���е�������
������ţ���ͬ�����䷴Ӧ�Ļ�ѧ����ʽΪ��
������������������������������������������������ ��
(2) �ռ�����ʱӦѡ��____��A�������ſ����� B�������ſ�����
(3)Ϊ�˵õ������NH3��Ӧѡ��________���������
A����ʯ�ҡ��� B��ŨH2SO4������C��P2O5
7����8�֣�����ȥ�±����й������е��������ʣ��������õ��Լ�����Ҫ�������裨����ţ���
��ѡ�õ��Լ��У���a����ˮ����b�����Ը��������Һ����c�����
��d��NaOH��Һ�� ��e������Na2CO3��Һ��
��ѡ�õIJ����У��ٹ��ˣ� ������ �۷�Һ����ͨ������ܣ���ͨ��ϴ��ƿ��
| ѡ���Լ� | ��Ҫ���� | |
| ��1��SiO2���Al2O3 | ||
| ��2�����������л�����ϩ���� | ||
| ��3��C2H4���SO2���� | ||
| ��4����������������� |
8����8�֣�ijͬѧ�����и�װ�����һ��ʵ�飬��֤���������ʡ�
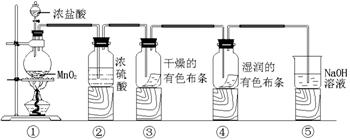
��ش�
��1�����������Ļ�ѧ����ʽ�������������������������������������������� ��
��2������Ũ�����������_____________��
��3�����е�ʵ��������_____________�����е�ʵ��������____________������ʵ������˵����Ư�����õ���__________���ѧʽ����������
��4������NaOH��Һ�����������ն������������ֹ��Ⱦ��������Ӧ�����ӷ���ʽ�� _____________������������������ ______��
��ѧ�Ծ��ڢ����3ҳ����4ҳ��
| �÷� | �ľ��� | ���������⣨��8�֣� |
9����4�֣�ʹ0.23 g�����Ƹ�������ˮ��Ӧ����Ӧ��������Һ�����Ϊ100 mL���Լ��㣺
������
��1����Ӧ���ɵ������ڱ�״���µ��������
��2����Ӧ��������Һ��NaOH�����ʵ���Ũ�ȡ�
10����4�֣�þ������������Ҫ�Ľ������ڹ�ҵ��������;�㷺��
��1����������������Һ��Ӧ�����ӷ���ʽΪ������������������������������������ ��
��2�������������������ȷ�Ӧ�Ļ�ѧ����ʽΪ�������������������������������� ��
��3����11.9 g Mg-Al-Fe��ɵĺϽ���������NaOH��Һ�У��Ͻ���������2.7 g ����ȡ�������ĺϽ����ڹ�����ϡ�����У�����6.72 L����״����NO����Ӧ�����Һ�м���������NaOH��Һǡ��ʹMg2+��Al3+��Fe3+��ȫת��Ϊ�����������������Ϊ�������� g��
�����г�����2008����ͨ���б�ҵ�ῼģ�⿼�ԣ�һ��
��ѧ�Ծ��𰸼����ֲο��� 2008��5
�ڢ��������������50�֣�
ѡ���⣨ÿС��2�֣���50�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| �� | C | B | B | B | C | C | A | D | B | D |
| ��� | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| �� | D | C | C | C | D | B | A | B | B | C |
| ��� | 21 | 22 | 23 | 24 | 25 | |||||
| �� | B | D | A | C | D |
�ڢ�����ǻ���������50�֣�
һ������⣨��22�֣�
1����3�֣� H2SO4���������� ����������������������������������������������������1��
�������������� C���������� ������������������������������������������������������1��
�������������� 1������������ ����������������������������������������������������1��
2����3�֣����١����������� ����������������������������������������������������1��
�������������� �ۡ������� ��������������������������������������������������������1��
���� �ڡ����������� ����������������������������������������������������1��
3����4�֣� CO32-��SO42-��Cu2+�������� ����������������������������������������1��
Cl-��Al3+������������ ����������������������������������������������1��
K+���������� ������������������������������������������������������1��
�� �������� ��ɫ��Ӧ���������� ��������������������������������������������������1��
4����4�֣���1���ۻ������������������������������������������������������������� 1��
����2��NO2���������� ��������������������������������������������������1��
��������![]() ������ ����������������1��
������ ����������������1��
��˵����û����ƽ��û�м��ȷ��Ų����֣�
��3���� �ۡ���û����ȫѡ����֣��������������������������������� 1��
5����8�֣���1��![]() ������������������������������������������������2��
������������������������������������������������2��
��2��HClO4������������������������������ ����������������������������2��
��3��Al(OH)3 + OH- == AlO2- + 2H2O ��������������������������������������2��
��4��0.25�������������������������� ����������������������������������2��
����ʵ���⣨��20�֣�
6����4�֣���1��A�������������������������������� ������������������������������1��
![]() ��������������������1��
��������������������1��
��2��B�������������� ������������������������������������������������1��
��3��A���������������� ������������������������������������������������1��
7����8�֣���1�� c���١������������������������� ��������������������������������2��
��2�� a���ݡ����������� ����������������������������������������������2��
��3�� d���ݡ����������� ����������������������������������������������2��
��4�� e���ۡ����������� ����������������������������������������������2��
8����8�֣���1��![]() ��������������������2��
��������������������2��
���������� ��2����ˮ��������������������������������������� ������������������1��
���������� ��3����ɫ��������ɫ�� ��ɫ������ɫ������ HClO�������� ����������ÿ��1��
��4��Cl2 + 2OH-== Cl- + ClO- + H2O������������ ��������������������������2��
���������⣨��8�֣�
9����4�֣��⣺����0.23 gNa��Ӧ���ɵ��������Ƶ����ʵ���Ϊx������H2�ڱ�״���µ����Ϊy
��������������������������
2Na + 2H2O = 2NaOH + H2����������
��������������������1��
�������� 23 g��2��������2 mol��22400 mL
0.23 g���������� x���� y���������� ��������������������1��
��1��������������![]() ��������������������������������1��
��������������������������������1��
![]()
��2��NaOH��Һ��NaOH�����ʵ���Ũ��Ϊ��![]() ����������������1��
����������������1��
�𣺣��ԣ�
10����4�֣���1��2Al + 2OH- + 2H2O == 2AlO2- + 3 H2����������������������������������1��
(2)![]() ����������
����������������������������1��
����������
����������������������������1��
��3��27.2������������ ����������������������������������������������2��
��ѧ�Ծ��ڢ����4ҳ����4ҳ��