高二化学 《烃的含氧衍生物》考试
相对原子质量:H-1 C-12 O-16 Ag-108
第Ⅰ卷(选择题 共46分)
一.选择题(本题包括8小题,每小题2分,共16分。每小题只有一个选项符合题意)
1.下列各组液体混和物,用分液漏斗不能分开的是
A.苯和水 B.乙醛和水 C.乙酸乙酯和水 D.溴苯和水
2.实验室制备下列物质时,不用加入浓H2SO4的是
A.由苯制取硝基苯 B.用乙酸和乙醇制备乙酸乙酯
C.由溴乙烷制乙烯 D.由乙醇制乙烯
3.营养学家研究发现,大脑的生长发育与不饱和脂肪酸密切相关,深海鱼油中提取的“DHA”就是一种不饱和程度很高的脂肪酸,被称为“脑黄金”,它的分子中含有6个碳碳双键,学名为二十 六碳六烯酸,它的化学式应是
A.C25H49COOH B.C26H39COOH C.C25H39COOH D.C26H41COOH
4.某有机物的结构简式为: 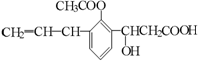 ,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚 ⑧中和
,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚 ⑧中和
A.①②④⑤⑥⑦⑧ B.②③④⑤⑥⑧
C.②③④⑤⑥⑦⑧ D.①②③④⑤⑥⑦⑧
5.分子中含5个碳原子的饱和一元醇,有多种同分异构体,其中催化氧化生成醛的醇有
A.2种 B.3种 C.4种 D.5种
6.分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下
能转化成C。则有机物A的可能结构有
A.1种 B.2种 C.3种 D.4种
7.某物质由甲酸、乙酸、乙醇和甲酸乙酯四种物质中的一种或几种组成。在鉴定时有下列现象:①有银镜反应;②加入新制氢氧化铜悬浊液沉淀不溶;③与含酚酞的氢氧化钠溶液共热,溶液中红色逐渐变浅直至变为无色。据此判断
A.几种物质都有
B.有甲酸乙酯,可能有乙醇,一定没有乙酸
C.有甲酸乙酯、甲酸和乙酸,可能有乙醇
D.有甲酸和乙醇,可能有甲酸乙酯
8.生活中的一些问题常涉及到化学知识,下列叙述中正确的是
①氟氯代烷化学性质稳定,排放到大气中不会对环境造成危害;②体积分数为75%的酒精可用来消毒;③苯酚有毒,所以日常所用的药皂中不可能掺入苯酚;④各种水果之所以有果香味,是因为水果中含有一定的酯类物质;⑤2,4,6-三硝基甲苯又叫TNT,是一种烈性炸药,可用于开矿;⑥福尔马林是混合物,可用来制作生物标本
A.①②③ B.④⑤⑥ C.①③⑤⑥ D.②④⑤⑥
二.选择题(本题包括10小题。每小题3分,共30分。每小题有一个或两个选项符合题意)
9.下列物质中,可一次性鉴别乙酸、苯、氢氧化钙溶液、乙醇的是
A.水 B. 碳酸钠溶液 C. 溴水 D. 紫色石蕊试液
10.甲苯分子的一氯取代物的同分异构体共有
A.3种 B. 4种 C. 8种 D. 10种
11.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实能说明上述观点的是
A.甲苯能使酸性高锰酸钾溶液褪色,甲烷不能使酸性高锰酸钾溶液褪色
B.乙烯能发生加成反应,乙烷不能发生加成反应
C.乙醛能发生银镜反应而乙醇却不能
 D.苯酚与浓溴水直接就可反应,苯与液溴反应则需要铁作催化剂
D.苯酚与浓溴水直接就可反应,苯与液溴反应则需要铁作催化剂
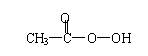
12.过氧乙酸 是一种高效消毒剂,具有很强的氧化性和腐蚀性,它可用
冰醋酸和过氧化氢在一定条件下制得;它可以迅速杀灭多种微生物,包括多种病毒、细菌、真菌及芽孢。有关过氧乙酸的叙述正确的是
A.过氧乙酸可与苯酚混合使用
B. 过氧乙酸分子中有酯的结构
C. 过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
D. 过氧乙酸分子结构中有羧基
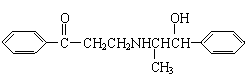 13.心酮胺是治疗冠心病的药物,它具有如下结构简式:下列关于心酮胺的描述错误的是
13.心酮胺是治疗冠心病的药物,它具有如下结构简式:下列关于心酮胺的描述错误的是
A.该物质是芳香族化合物 B.可以在催化剂作用下和溴反应
C.可以发生银镜反应 D.不能发生酯化反应
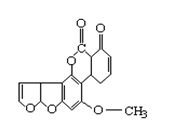 14.黄曲霉素的结构如下,1 mol 该化合物分别与H2、NaOH溶液反应最多消耗H2和NaOH分别为
14.黄曲霉素的结构如下,1 mol 该化合物分别与H2、NaOH溶液反应最多消耗H2和NaOH分别为
A.6 mol 2 mol
B.7 mol 2 mol
C.6 mol 1 mol
D.7 mol 1 mol
![]() 15.从柑橘中可提取得萜二烯-1,8,结构如右图所示。有关萜二烯-1,8的说法正确的是
15.从柑橘中可提取得萜二烯-1,8,结构如右图所示。有关萜二烯-1,8的说法正确的是
A.萜二烯-1,8的分子式为C10H16
B.萜二烯-1,8与足量的H2反应后,产物的分子式为C10H22
C.萜二烯-1,8与1mol的HBr发生加成反应,可以得到2种不同的产物
D.萜二烯-1,8能发生加聚反应
16.荣获2001年诺贝尔化学奖的科学家科研的成果,不仅具有巨大的理论意义,而且已经成功地运用于生产实际,取得了良好的经济效益。例如,美国科学家的成果被应用于工业合成重要的治疗帕金森症(震颤麻痹症)的药物左旋多巴(C)。下面是它们的结构式以及美国科学家发明的合成路线。
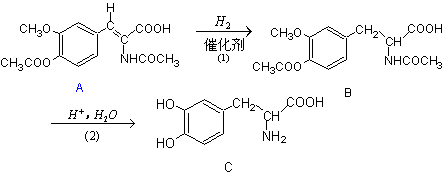 |
在上述反应中,关于 ⑴、⑵ 两步的反应类型,全部正确的是
A.化合反应,分解反应 B.加成反应,水解反应
C.还原反应,分解反应 D.氧化反应,水解反应
17.某芳香族有机物的分子式为C8H6O2,它的分子(除苯环外不含其他环)中不可能有
A. 两个羟基 B. 一个醛基 C. 两个醛基 D. 一个羧基
18.胆固醇是人体必需的生物活性物质,分子式为C27H46O,一种胆固醇酯是液晶材料,分子式为C34H50O2,合成这种胆固醇酯的酸是
A.C6H13COOH B. C6H5COOH C. C7H15COOH D. C6H5CH2COOH
第Ⅱ卷(非选择题 共54分)
三.填空题
19.核磁共振谱(NMR)是研究有机化合物结构的最有力手段之一。在所研究化合物的分子中,每一种结构类型的等价(或称为等性)H原子,在NMR谱中都给出相应的峰(信号).谱中峰的强度是与分子中给定类型的H原子数成比例的.例如,乙醇的NMR谱中有三个信号,其强度比为3:2:1。
(1)在常温下测得的某烃C8H10(不能与溴水反应)的NMR谱上,观察到两种类型的H原子给出的信号,其强度之比为2:3,试确定该烃的结构简式为 ;该烃在光照下生成的一氯代物在NMR谱中可产生几种信号 ,试确定强度比为 。
(2)在常温下测定相对分子质量为128的某烃的NMR,观察到两种类型的H原子给出的信号,其强度之比为9:1,若为链烃,则该烃的结构简式为 ;观察到两种类型的H原子给出的信号,其强度之比为1:1,若为芳香烃,则该烃的结构简式为 。
20.(1)A、B、C三种物质分子式都是C7H8O,若滴入FeCl3溶液,只有C呈紫色;若投入金属钠,只有B没有变化。在A、B中分别加入溴水,溴水不褪色。
写出A、B、C的结构简式:A_________,B_________,C(只写一个)_________。
|
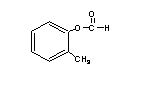
① ②
|
③ 、④ 、⑤ 、⑥ 。
 21.有三个只含C、H、O的有机化合物A1、A2、A3,它们互为同分异构体,M=60,室温时均为液态,分子中C与H的质量分数之和是46.7%。A1、A2均可与新制取的碱性氢氧化铜悬浊液反应生成砖红色沉淀,其产物分别为B1、B2;A3能与氢氧化铜反应形成蓝色溶液。 A1难溶于水而A2、A3易溶于水。上述关系也可以表示如下图,
21.有三个只含C、H、O的有机化合物A1、A2、A3,它们互为同分异构体,M=60,室温时均为液态,分子中C与H的质量分数之和是46.7%。A1、A2均可与新制取的碱性氢氧化铜悬浊液反应生成砖红色沉淀,其产物分别为B1、B2;A3能与氢氧化铜反应形成蓝色溶液。 A1难溶于水而A2、A3易溶于水。上述关系也可以表示如下图,
请用计算、推理,确定A1 、 A2 、 A3 、 B1 、 B2的结构简式。
A1 、 A2 、 A3 、
B1 、 B2 。
22.已知①一元羧酸在一定条件下可以脱水生成羧酸的酸酐,如:
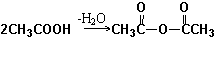 |
②烯键碳原子上若结合羟基时不稳定,自动转化为醛,
如:R—CH=CH—OH → RCH2—CHO
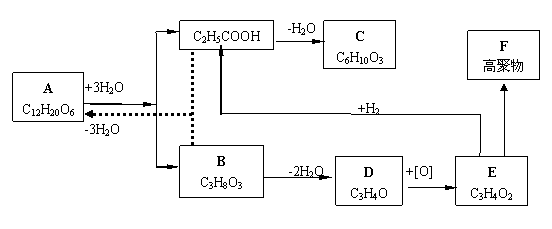 现有有机化合物A~F,它们之间在一定条件下可发生如图所示的一系列变化。分析图示,完成下列问题:
现有有机化合物A~F,它们之间在一定条件下可发生如图所示的一系列变化。分析图示,完成下列问题:
(1)写出下列物质的结构简式 A ;B ; C
(2)写出下列反应的化学方程式:
E→F 。
四.实验题
23.下列有关实验的说法正确的是_____________。
A.制乙烯时,温度计应插入反应混合液中
B.实验室用溴和苯在铁粉存在下反应,得到的溴苯显橙红色,原因是溴苯在空气中被氧化
C.检验C2H5Cl中氯元素时,将C2H5Cl和NaOH水溶液混合加热,然后用稀硫酸酸化,再加入AgNO3溶液
D.做过银镜反应的试管用氨水洗涤,做过苯酚的试管用酒精洗涤
E.将一定量CuSO4和NaOH溶液混合后加入甲醛溶液,加热至沸腾,产生黑色沉淀,原因可能是NaOH量太少
F.用3mL乙醇、2mLH2SO4、2mL冰醋酸制乙酸乙酯,为增大反应速率,现改用6mL乙醇、4mLH2SO4、4mL冰醋酸
24.一氯甲烷也叫甲基氯,常温下是无色气体,密度为0.9159g/cm3,熔点为-97.73℃,沸点为-24.2℃,18℃时在水中的溶解度为280 mL/L水,与乙醚、丙酮或苯互溶,能溶于乙醇。在实验室里可用如图装置制取一氯甲烷;制备装置的分液漏斗中盛有甲醇,烧瓶中盛有浓盐酸和无水氯化锌,甲醇和浓盐酸在氯化锌存在下可生成一氯甲烷。
|
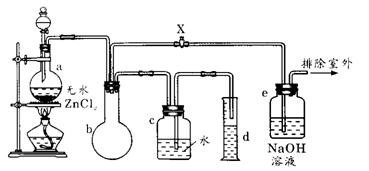
试填写下列空白:
(1) 制备一氯甲烷的化学方程式_____________________,其反应类型属于_____反应;
(2) 装置b的作用是_____________________;
(3) 若打开活塞X,装置e中可能发生的反应方程式为____________________________;
(4) 实验中将甲醇和浓盐酸按1∶2(物质的量之比)进行反应的理由是______________;
(5) 某学生在关闭活塞X的情况下做此实验时发现,收集一定体积的气体产物所消耗的甲醇-浓盐酸的混合液的量比正常情况下多(装置的气密性没有问题),其原因是___________;
(6)实验结束后,d中收集到的液体中含有______________________。
五.计算题
25.取46.0g乙醇,加入适量浓硫酸后,再加入30.0g乙酸,加热后制得的乙酸乙酯的质量为33.0g求此时该反应的产率。
26.将含有C.H、O的有机物3.24 g,装入元素分析装置,通入足量的O2使它完全燃烧,将生成的气体依次通过氯化钙干燥管A和碱石灰干燥管B。测得A管质量增加了2.16g,B管增加了9.24g。已知该有机物的相对分子质量为108。
⑴求此化合物的分子式?
⑵燃烧此化合物3.24g,须消耗氧气的质量是多少?
⑶该化合物1分子中存在1个苯环和1个羟基,试写出它的同分异构体的结构简式。
高二化学 《烃的含氧衍生物》考试答卷纸
班级 姓名 学号
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| 答案 | ||||||||||
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 |
三.填空题
19. ⑴ ; , 。
⑵ , 。
20.
⑴ A________ ,B ,C 。
⑵ ③_________________ 、④_________________ 、⑤ 、
⑥ _____________ 。
21. A1 、A2 、A3 、
B1 、B2 。
22.(1)结构简式 A ;B ; C 。
(2)化学方程式: E→F 。
四.实验题
23.正确的是_____________ 。
24.(1) 化学方程式________________________, 反应类型_____ 反应;
(2) b作用是_____________________ ;
(3) 反应方程式为______________________________ ;
(4) 理由是________________ ;
(5) 原因是_________________________________________ ;
(6) 液体中含有______________________。
五.计算题
25.
26、