高二年级化学第二学期期中试卷
化 学 试 题
提示:第21至25题、第30、31、33题均分文科,理科两类,请注意不要做错。
本试卷可能用到的相对原子质量:H―1 C―12 O―16 Na―23 S―32 Ba―137
第Ⅰ卷(共25小题,共55分)
一、选择题(每小题只有一个正确选项,共20题,计40分。)
1.下列物质中,不属于高分子化合物的是 ( )
A.酶 B.天然橡胶 C.淀粉 D.硬脂酸甘油酯
2.下列过程不发生化学变化的是 ( )
A.裂解 B.裂化 C.分馏 D.干馏
3.下列变化必须加入氧化剂才能实现的是 ( )
A.Na2O→NaOH B.Cl―→Cl2 C.Na2O2→O2 D.Cl―→NaCl
4.将p%浓硫酸和同体积水混合后得到q%稀硫酸,则p、q关系正确的是 ( )
A.p≤2q B.p=2q C.p<2q D.p>2q
5.有关淀粉和纤维素的说法,不正确的是 ( )
A.均为多糖,是天然高分子化合物
B.它们水解产物都是葡萄糖
C.结构不同,互为同分异构体
D.都是葡萄糖以不同方式缩小得到的产物
6.若9.6×10―3mol的XO4―在溶液中还原为较低价态,需要24mL 0.4mol/L的Na2SO3,则
X元素的最终价态为 ( )
A.+7价 B.0价 C.+5价 D.+4价
![]() 7.体积相同的甲、乙两个容器,分别都充有等物质的量的SO2和O2,在相同温度发生反应2SO2(g)+O2(g)
2SO3(g),并达到平衡,在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为P%,则乙容器中的SO2的转化率为
7.体积相同的甲、乙两个容器,分别都充有等物质的量的SO2和O2,在相同温度发生反应2SO2(g)+O2(g)
2SO3(g),并达到平衡,在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为P%,则乙容器中的SO2的转化率为
( )
A.等于P% B.大于P% C.小于P% D.无法判断
8.铁棒和石墨用导线连接后浸入0.01mol/L的食盐溶液中,可能出现的现象是 ( ) A.铁棒附近产生OH― B.铁棒被腐蚀
C.石墨棒上放出Cl2 D.石墨棒上放出O2
9.在180℃,101Kpa下,1L稀轻与炔烃的混合气体与相同状态下11L氧气混合,点火充分
燃烧后,恢复到原来状况,测知仍有12L气体,则混合烃不可能是 ( )
A.C2H2,C3H6 B.C2H2,C4H8 C.C2H4,C3H4 D.C3H4,C3H6
10.下列分子中的各原子不处于同一平面的是 ( )
A.苯 B.乙炔 C.乙烯 D.乙烷
11.关于丙烯醛(CH2=CH―CHO)的化学性质叙述中错误的是 ( )
A.能起银镜反应,表现氧化性 B.能使溴水褪色,发生加成反应
C.能与新制Cu(OH)2发生反应 D.一定条件下,能发生加聚反应
12.下列物质属于强电解质的是 ( )
①NaHS ②BaSO4 ③Al(OH)3 ④CO2 ⑤HCl ⑥Na
A.①⑤⑥ B.②③⑤ C.①②⑤ D.③④⑥
13.下列混合物中,只要总质量一定,不论以何种比例混合完全燃烧产生的二氧化碳和水均为一恒量的是 ( )
A.甲烷和乙烷 B.乙酸和葡萄糖
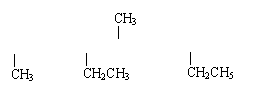 C.甲醛和乙酸乙酯 D.硬脂酸甘油酯和油酸甘油酯
C.甲醛和乙酸乙酯 D.硬脂酸甘油酯和油酸甘油酯
14.结构简式为CH3―CH―CH2―CH―CH―CH2―CH―CH3的烃的名称为 ( )
A.3,5,8―三甲基―6―乙基壬烷 B.2,5,7―三甲基―4―乙基壬烷
C.4,7―二甲基―2,5―二乙基辛烷 D.2,5―二甲基―4,7―二乙基辛烷
15.现有两种短周期元素的简单离子,aXm+、bYn―,若两者的电子层结构相同,则下列关系式正确的是 ( )
A.b-a=m+n B.a-b=m+n C.b-a=m-n D.a-b=m-n
16.物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液,其pH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是 ( )
A.HX、HZ、HY B.HZ、HY、HX C.HX、HY、HZ D.HY、HZ、HX
![]() 17.可逆反应A+3B 2C+2D在四种情况下,反应速率分别为 :
17.可逆反应A+3B 2C+2D在四种情况下,反应速率分别为 :
①VA=0.15mol/(L・S),②VB=0.6mol/(L・S),③VC=0.4mol/(L・S),④VD=0.45mol/(L・S),则以上四种反应速率的大小排列正确的是 ( )
A.④>②=③>① B.②>④>③>①
C.②>③=④>① D.④>③>②>①
18.下列说法正确的是 ( )
A.原电池是把电能思化为化学能的装置
B.原电池中电子流出的一极是正极,发生氧化反应
C.原电池的两极发生的反应均为氧化还原反应
D.形成原电池,原电池中的阳离子向正极移动
19.VmL浓度为C mol/L的HA溶液中,含mg HA溶质,则A的相对原子质量为 ( )
A.![]() B.
B.![]() -1 C.
-1 C.![]() -1 D.
-1 D.![]() -1
-1
20.不能用来比较非金属性相对强弱的条件是 ( )
A.最高价氧化物对应水化物的酸性强弱
B.气态氢化物的稳定性
C.非金属间的相互置换
D.单质的熔、沸点高低
二、选择题(每小题只有一个正确选项,共5题,共15分)
21.(文科)下列物质中,不属于合成材料的是 ( )
A.塑料 B.合成纤维 C.陶瓷 D.合成橡胶
22.(文科)下列说法不正确的是 ( )
A.分子是为C3H8和分子是为C5H12的两种有机物一定是互为同系物
B.具有相同通式的两种有机物不一定互为同系物
C.两个相邻同系物的相对分子质量数值一定相差14
D.分子组成相差一个或几个CH2原子团,必定互为同系物
23.(文科)乙烯发生的下列反应,不属于加成反应的是 ( )
A.与氢气反应,生成乙烷 B.与水反应生成乙醇
C.与溴水反应使之褪色 D.与酸性高锰酸钾溶液反应使之褪色
24.(文科)下列物质中属于同素异形体的是 ( ) A.D和T B.乙烯和丙烯
C.正丁烷和异丁烷 D.C60和金刚石
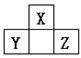
|
则X、Y、Z的元素符号为( )
A.O、P、Cl B.Cl、P、O
C.O、S、Cl D.P、S、Cl
21.(理科)一定质量的某有机物和足量的金属钠反应,可得到气体Va L,等质量的该有机物如果与足量的纯碱溶液反应,可得到气体Vb L。若同温同压下Va>Vb,那么该有机物可能是 ( )
A.CH3COOH B.HOOC―COOH
C.HOCH2CH2CHO D.HOCH2CH2COOH
22.(理科)在标准状况下,V L氨气溶于1 L水中,形成密度为ρg/cm3氨水,该氨水的物质的量浓度为 ( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
![]() 23.(理科)一定量含A、B、C的混合气体,在密闭容器中反应,m A(g)+n B(g)
23.(理科)一定量含A、B、C的混合气体,在密闭容器中反应,m A(g)+n B(g)
p C(g)。在一定温度下达到平衡。若气体体积缩小到原来的1/2,则C的浓度为原来的1.9倍。下列说法正确的是 ( )
A.m+n>p B.A的转化率降低
C.平衡向正反应方向移动 D.C的体积百分含量增加
24.(理科)常温常压下,将16mL CH4和C2H2的混合气体与足量氧气混合后,点燃使之充分燃烧,冷却到常温常压下,发现总体积比反应前减少26mL,则混合物气体中甲烷的体积为 ( )A.4mL B.8 mL C.10 mL D.12 mL
25.(理科)在一定温度下,向容积固定不变的容器里充入a mol NO2,发生如下反应:
![]() 2NO2 N2O4(g),达到平衡后,再向该容器中充入1mol NO2,达到平衡后与原平衡比较,错误的是 ( )
2NO2 N2O4(g),达到平衡后,再向该容器中充入1mol NO2,达到平衡后与原平衡比较,错误的是 ( )
A.平均相对分子质量增大 B.NO2的转化率提高
C.压强比原来的2倍要小 D.颜色变浅
第Ⅱ卷(共8小题,共45分)
三、填空题(共6题,共33分)
26.短周期元素的四种离子A3+、B+、C―、D2―,均具有相同的电子层结构:
它们的原子半径由大到小的顺序为 ;
它们的原子序数由大到小的顺序为 。
27.用乙醇制取乙二醇(HOCH2―CH2OH),需要经过3个阶段,依次写出反应的化学方程式,并注明反应类型:
(1)反应方程式 ,反应类型 。
(2)反应方程式 ,反应类型 。
(3)反应方程式 ,反应类型 。
28.乙二酸(HOOC―COOH)和乙二醇(HOCH2―CH2OH)在不同条件下反应,会生成三种不同的酯,其中普通酯是一个乙醇分子和一个乙二酸分子反应生成的,分子式为C4H6O5,另一种分子式为C4H4O4的环状酯,还有一种高分子酯,试写出它们的结构简式:
(1)普通酯 ;
(2)环状酯 ;
(3)高分子酯 。
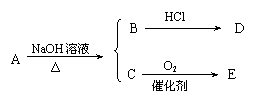 29.有机物A~E有以下转化:
29.有机物A~E有以下转化:
(1)若A的分子式为C4H8O2,且D不能发生银镜反应,则A的结构简式为
(2)若A的分子式为C4H8O2,且D不能发生银镜反应,而E不能被氧化,则A的结构简式为 。
(3)若C不能发生消去反应,且D不能发生银镜反应,则有机物A分子中碳原子数至少应有 个。
30.(文科)二氯化铁溶液显 性,原因是(用离子方程式表示) 。
将该溶液蒸干强热后,即得固体,主要成分是 。
![]() 31.(文科)在下列几种有机物中(用编号填写)
31.(文科)在下列几种有机物中(用编号填写)
![]() A.NH2 B.CH3―CH―COOH C.C12H22O11(麦芽糖)
A.NH2 B.CH3―CH―COOH C.C12H22O11(麦芽糖)
D.CH2OH(CHOH)4CHO E.CH3COOCH2CH2CH3
(1)既能发生银镜反应,又能发生水解反应的是 。
(2)既能与酸反应,又能与碱反应的是 。
(3)既能发生酯化反应,又能发生消去反应的是 。
|
30.(理科)有机物A俗称水杨酸,其结构简式为:
(1)将A跟下列编号为 的物质的溶液反应,可得到一种钠盐(该盐化学工为C7H5O3Na)
A.NaOH B.NaHCO3 C.NaCl
(2)水杨酸的同分异构体中,属于酚类,同时还属于酯类的化合物有 种,这种有机物1mol与足量氢氧化钠溶液反应,消耗NaOH的物质的量为 mol。
(3)水杨酸的同分异构体中,属于酚类,但不属于酯类或羧酸类的化合物,必定含有
基。
31.(理科)(1)把pH=2的醋酸溶液与pH=12的苛性钠溶液等体积混合后,溶液pH (填“>”“=”或“<”),把同体积同物质的量浓度的醋酸和苛性钠溶液混合后,溶液pH
7(填“>”“=”或“<”)。用NaOH溶液去滴定醋酸溶液,应用 作指示剂。
(2)pH=2的强酸溶液V1 mL与pH=13的某碱溶液V2 mL,混合后溶液的pH=11,则V1、V2的关系为 。
(3)已知100℃时,KW=1×10―12。此温度下,将pH=3的稀硫酸与pH=10的NaOH溶液混合后,溶液pH=7,则稀硫酸和氢氧化钠溶液的体积比为 。(假设两溶液混合后体积不变)
四、计算题(共2题,共12分)
32.取100mL Na2CO3和Na2SO4的混合溶液,加入过量的BaCl2溶液充分反应后得29.02g白
色沉淀,用过量稀HNO3处理后,沉淀减少到9.32g,并有气体产生。
(1)原溶液中Na2CO3和Na2SO4的物质的量浓度是多少?
(2)产生的气体在标准状况下的体积是多少?
33.(文科)将某饱和一元醇与足量钠反应,生成标准状况下的氢气560mL,若取等质量的醇完全燃烧,生成3.36L标准状况下的CO2和3.6g水,通过计处确定该醇的化学式,并写出可能的同分异构体的结构简式。
33.(理科)某有机物在气态时,其密度是相同条件下氢气的38倍,若将它完全燃烧,只生成水蒸气和二氧化碳,且二者的体积比为(同温同压下)4:3,另取该有机化合物3.8g,充分燃烧后将其产物全部通过干燥的碱石灰,碱石灰增重10.2g,再取同质量的该有机物与足量的金属钠反应,可生成标况下的氢气1.12L。
求:(1)该有机物的分子式。
(2)该有机物属于哪一类有机物,写出可能的结构简式。
参考答案
第Ⅰ卷(共25小题,共55分)
一、二、选择题(共25小题,共55分)
1.D 2.C 3.B 4.C 5.C 6.C 7.B 8.B 9.D 10.D 11.A 12.C 13.B 14.B 15.B
16.C 17.A 18.D 19.D 20.D 21.文C 理D 22.文D 理B 23.文D 理B
24.文D 理A 25.文A 理D
第Ⅱ卷(共8小题,共45分)
三、填空题(共6小题,共33分)
|
27.(1)CH3CH2OH CH2 CH2+H2O,消去
(2)CH2=CH2+Br2→CH2Br―CH2Br,加成
(3)CH2Br―CH2Br+2NaOH→HOCH2―CH2OH+2NaBr,取代
28.(1)普通酯HOOC―COOCH2―CH2OH;
| |
| |
|
![]()
![]() (3)高分子酯 [ CO―COOCH2―CH2―O ]n。
(3)高分子酯 [ CO―COOCH2―CH2―O ]n。
29.(1)CH3COOC2H5,CH3CH2COOCH3 (2)HCOOCH(CH3)2 (3)3个
![]() 30.(文科)呈酸性,原因是(离子方程式)Fe2++2H2O Fe(OH)2+2H+
30.(文科)呈酸性,原因是(离子方程式)Fe2++2H2O Fe(OH)2+2H+
主要成分是Fe2O3
31.(文科)(填编号)(1)C (2)A (3)B (4)CE
30.(理科)(1)B; (2)3种,3mol (3)醛基
31.(理科)(1)pH<7, pH>7, 酚酞作指示剂。
(2)V1、V2的关系为V1 : V2≥9∶1
(30体积比为999∶101
四、计算题(共2小题,共12分)
32.(1)c(Na2SO4)=0.4mol/L, c(Na2CO3)=1.0mol/L (2)V(CO2)=2.24L
33.(文)(1)C3H8O; (2)CH3CH2CH2OH,CH3CHOHCH3
33.(理)(1)C3H8O2;(2)该有机物为醇,结构式HOCH2CH2OH,HOCH2CHOHCH3