高二年级化学下学期期中试题
高二化学
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分
试题总分值:100分 考试时间:100分钟
可能用到的原子量:H 1 C 12 N 14 O 16 C1 35.5 Na 23 Cu 64
第I卷(选择题 共46分)
一、单项选择题(本题包括8小题,每题2分,共16分。每题只有一个选项符合题意)
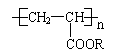 1.聚丙烯酸酯的结构为
,下列有关它的说法中,不正确的是( )
1.聚丙烯酸酯的结构为
,下列有关它的说法中,不正确的是( )
A.它可由CH2=CH―COOR经加成聚合反应得到
B.聚丙烯酸酯材料是一种混合物
C.在一定条件下能发生水解反应
D.在一定条件下能发生加成反应
2.下列物质互为同系物的是( )
![]() A.HCOOH 和 C17H35COOH
B.
和
A.HCOOH 和 C17H35COOH
B.
和
![]() C. -OH和 -CH2OH D.CH3CH2CH2CH2OH 和 CH3CH(OH)CH2CH3
C. -OH和 -CH2OH D.CH3CH2CH2CH2OH 和 CH3CH(OH)CH2CH3
3.x 、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知( )
A.x的原子半径大于y的原子半径。
B.x的电负性大于y的电负性。
C.x阴离子的半径小于y阳离子的半径
D.x的第一电离能小于y 的第一电离能。
4.已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
A.X与Y形成化合物是,X可以显负价,Y显正价
B.在元素周期表中X可能位于Y的右面
C.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性
D.Y的气态氢化物的稳定性小于X的气态氢化物的稳定性
5.使蛋白质从水中析出并保持其生理活性,可以加入下列溶液中的( )
A.乙酸铅溶液 B.氢氧化钠溶液 C.福尔马林 D.饱和硫酸铵溶液
6.下列说法中,错误的是( )
A.纤维素和淀粉的化学式都可以写作(C6H10O5)n,它们并不是同分异构体
B.有机物分子中,碳原子总是和4个原子或原子团直接连接
C.煤是由有机物和无机物组成的复杂的混合物
D.石油的分馏产品经过裂解可以得到乙烯、丙烯等气态短链烃
7.下列关于电子云的说法中,正确的是( )
A.电子云表示电子在原子核外运动的轨迹
B.电子云表示电子在核外单位体积的空间出现的机会多少
C.电子云界面图中的小黑点密表示该核外空间的电子多
D.电子云可表示电子在核外运动的方向
8.当乙醇发生下列反应时,所断裂的键是O-H的是 ( )
A.和金属钠反应生成乙醇钠和氢气
B.和氢溴酸反应生成溴乙烷和水
C.在催化剂作用下生成乙烯和水
D.与灼热的氧化铜作用生成乙醛、铜和水
二、选择题(本题包括10小题,每小题3分,共30分。每小题有一个选项符合题意。)
9.能证明某有机物分子中含有羧基的是( )
A.分子式可写作CnH2nO2,且与钠反应生成氢气
B.一定条件下能与硝酸发生酯化反应
C.分子式可写作CnH2nO2,且与碳酸氢钠反应生成CO2
D.分子式可写作CnH2nO2,能与氢氧化钠反应,生成物中有CH3COONa
10.皮肤的黑白与皮肤中黑色素的多少有关,而酪氨酸是黑色素合成的基础物质,酪氨酸的结构简式为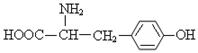 ,下列有关酪氨酸的说法不正确的是( )
,下列有关酪氨酸的说法不正确的是( )
A. 酪氨酸分子是手性分子
B. 酪氨酸在碱性条件下,主要以阴离子的形态存在
C.水解能生成酪氨酸的蛋白质遇浓酸变黄
D.酪氨酸不能发生缩聚反应形成高分子化合物
11.某学生设计了如下实验方案用以检验淀粉水解的情况:
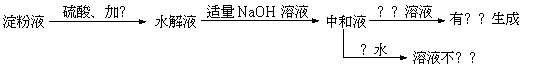 |
下列结论正确的是( )
A.淀粉尚有部分未水解 B.淀粉已完全水解
![]()
![]() C.淀粉没有水解
D.淀粉已发生水解,但不知是否完全水解12.用丙醛(CH3-CH2-CHO)制取聚丙烯 [ CH2-CH(CH3)]n的过程中发生的反应类型为( ) ①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原
C.淀粉没有水解
D.淀粉已发生水解,但不知是否完全水解12.用丙醛(CH3-CH2-CHO)制取聚丙烯 [ CH2-CH(CH3)]n的过程中发生的反应类型为( ) ①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原
A.①④⑥ B.⑤②③ C.⑥②③ D.②④⑤
13.具有下列电子层结构的原子,其对应的元素一定属于同一周期的是( )
A.两种元素原子的电子层上全部都是s电子
B.3p能级上只有1个空轨道的原子和3p能级上只有1个未成对电子的原子
C.最外层电子排布为2s22p6的原子和最外层电子排布为2s22p6的离子
D.原子核外的M层上的s、p能级上都填满了电子而d轨道未排电子的两种原子
14.乙醛能够发生银镜反应,还能在碱性条件下被新制的氢氧化铜氧化,这是因为其分子结构中存在醛基,下列说法错误的是 ( )
A.乙醛在反应中被氧化为羧酸后,羧酸能与碱反应形成羧酸盐
B.醛类物质都含有醛基,上述两个反应是醛类的特征反应
C.在一定条件下,醛和氢气起加成反应生成醇,此时醛被还原
D.甲醛和乙醛都有刺激性气味,通常状况下它们都是易溶于水的液体
15.有机物A和B,只由C、H、O两种或三种元素组成,相同物质的量的A和B完全燃烧时,消耗氧气的物质的量相等,下列对A、B的判断错误的是( )
A.A与B互为同分异构体 B.A与B的分子组成相差n个“CH2”
C.A与B的分子组成相差n个“CO2” D.A与B的分子组成相差n个“H2O”
16.据最近的美国《农业研究》杂志报道,美国的科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式为![]() ,则下列说法错误的是( )
,则下列说法错误的是( )
A.半胱氨酸,属于a-氨基酸
B.半胱氨酸是一种两性物质
C.两分子半胱氨酸,脱水形成的二肽结构简式为:
|
|
|
D.HS―CH2―CH2―COONH4可与NaOH溶液反应放出一种碱性气体
17.下列有关认识正确的是( )
A.各能级的原子轨道数按s、p、d、f的顺序分别为1、3、5、7
B.各能层的能级都是从s能级开始至f能级结束
C.各能层含有的能级数为n―1
D.各能层含有的电子数为2n2
![]() 18. 将
和C3H5(OH)3(甘油)以一定比例混合,测得混合物含碳51.3%,那么氧元素的质量分数是( )
18. 将
和C3H5(OH)3(甘油)以一定比例混合,测得混合物含碳51.3%,那么氧元素的质量分数是( )
A.40% B.35% C.30% D.无法计算
第II卷 (非选择题 共54分)
三、(本题包括2小题,共19分)
|
(1)写出下列元素的符号:甲 丁 戊
(2)用电子式表示甲和乙元素组成化合物的形成过程
(3)乙和戊元素气态氢化物沸点高低关系是 > (填化学式)
(4)丙元素原子价电子层电子排布式为
(5)戊和丁形成化合物的电子式
(6)丙的硫酸盐与少量氨水反应的离子方程式
20.(8分)有机化学反应因反应条件不同,可生成不同的有机产物。例如:
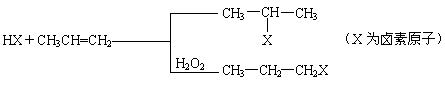 |
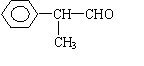 工业上按下列路线合成结构简式为
的物质,该物质是一种香料。
工业上按下列路线合成结构简式为
的物质,该物质是一种香料。
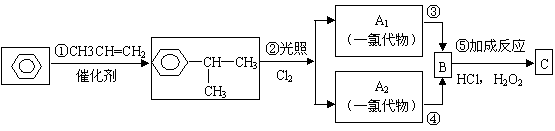 | |||
 | |||
请回答下列问题:
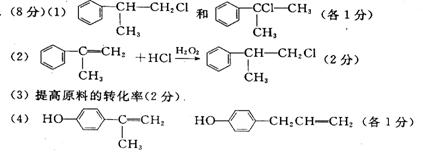
(1)写出A1、A2可能的结构简式:A1 ;A2______________。
(2)反应⑤的化学方程式为
(3)工业生产中,中间产物经反应③④⑤⑥得D,而不是由A1或A2直接转化为D。其优越性主要是__________。
(4)这种香料有多种同分异构体,写出2种符合下列条件的有机物的结构简式:
a.其水溶液遇FeCl3溶液变紫色;
b.分子中有苯环,且苯环上的一溴代物只有2种。
_____________________,___________________________。
四、(本题包括2小题,共14分)
![]() 21.(6分)常见有机化合物A、B、C(分子中的碳原子数都不超过4)在氧气中充分燃烧都只生成CO2和H2O,它们中的大多数在有机合成中有重要作用。X是气体单质,在一定条件下,它们有如下转化关系:
。
21.(6分)常见有机化合物A、B、C(分子中的碳原子数都不超过4)在氧气中充分燃烧都只生成CO2和H2O,它们中的大多数在有机合成中有重要作用。X是气体单质,在一定条件下,它们有如下转化关系:
。
请回答下列问题:
(1)X可以是 。
(2)若A、B都能发生加聚反应,则A、B的加聚产物分别是
、 。
(3)若等物质的量的A、B、C在氧气中充分燃烧,其耗氧量逐渐减小,又A和C反应,既可以生成六元环状化合物,也可以生成高分子化合物,则该高分子化合物的结构简式为 。
22.(8分)医药阿斯匹林的结构简式如下,试根据阿斯匹林的结构回答:
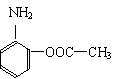 |
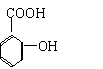 ⑴阿斯匹林看成酯类物质,口服后,在胃肠酶的作用下,阿斯匹林发生水解反应,
⑴阿斯匹林看成酯类物质,口服后,在胃肠酶的作用下,阿斯匹林发生水解反应,
生成A和B 两种物质。其中A的结构简式为 ,则B的结构简式
为 ;B中含有的官能团是(填名称) 。
⑵阿斯匹林跟小苏打同时服用,可使上述水解产物A与小苏打反应,生成可溶性盐随尿液排出,该反应的化学方程式为: 。
⑶上述水解产物A与氢氧化钠溶液反应的化学方程式为:
;
⑷上述水解产物B与乙醇、浓硫酸共热反应的化学方程式为
。
五、(本题共13分)
23(13分)按照下图所示装置进行有关实验,拔掉分液漏斗玻璃塞,将A逐滴加入B中。
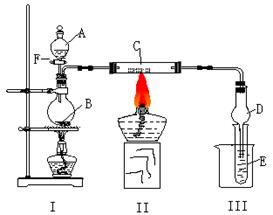
(1)若A是乙醇,B是生石灰,实验中观察到C中黑色固体逐渐变红。当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁出现了光亮的银镜。则C是 ,在反应作 剂(填“氧化”或“还原”),写出硬质玻璃管C中所发生的反应方程式 。试管E中所发生反应的离子方程式 。
(2)若A是能发生银镜反应且只含一个碳的一种液态有机物,B为浓硫酸,E为苯酚钠溶液,C不变。实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管E中溶液变浑浊,则A是(写名称) 。然后往烧杯中加入沸水,则试管E中的现象是 。此实验中浓硫酸的作用是 。写出硬质玻璃管C中所发生的反应方程式
。
写出乙醇和⑵题中A这二种物质在浓硫酸存在时所发生的反应方程式
。
六、(本题共8分)
24.(8分)0.2mol某有机物和0.4molO2,在密闭容器中燃烧后,产物为CO2、CO和H2O,产物经过浓硫酸后,浓硫酸增重10.8g,通过灼热的CuO充分反应后,使CuO失重3.2g,最后通过碱石灰,碱石灰增重17.6g,若同量该有机物与9.2g钠恰好反应。计算并回答有机物的结构简式及名称。
高二化学试题参考答案和评分标准
一、共16分。每小题2分。
1. D 2. A 3. B 4. C 5. D 6. B 7.B 8.A
二、共30分。每小题3分。
9. C 10. D 11. B 12. C 13. B 14. D 15. B 16.C 17.A 18.A
三、共19分。第19题11分。第20题8分。
19.(11分)(1)C K O(3分) (2)CS2的形成过程(略,2分)
(3)H2O H2S (2分) (4)3d104s1 (1分) (5)K2O的电子式(略)1分
(6)Cu2++2NH3・H2O=Cu(OH)2 +2NH4+ (2分)
20.
四、共14分。第21题6分,每小题2分。第22题8分。



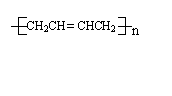 21. (1) H2或O2
21. (1) H2或O2
 (2)
、
、
、
(2)
、
、
、
或 (其他合理答案均可)
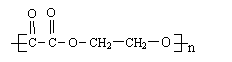 |
(3)
22.略(第1题每空1分,其余每空2分,共8分)
五、共13分。
23.(1)CuO (1分)氧化剂(1分) CuO+CH3CH2OH → CH3CHO+Cu+H2O (2分)
CH3CHO + 2[Ag(NH3)2]+ + 2OH- → CH3COO- + NH4+ + 2Ag↓+ 3NH3 + H2O (2分)
|
![]() CO+CuO =Cu+CO2(2分)
CO+CuO =Cu+CO2(2分)
HCOOH+C2H5OH HCOOC2H5+H2O (2分)
六、共8分。
24. 则有机物的分子式为C2H6O2(4分)
所以结构简式HOCH2CH2OH,名称为乙二醇。(4分)