�߶���ѧ�ڶ�ѧ�ڵڶ����¿�����
���Ծ��־���;���������,����100�֡�����ʱ��Ϊ90���ӡ�
���Խ���������ֽ�ʹ��һ�����ء�
���ԭ��������H 1��C 12��N 14��O 16��Na 23��Mg 24��Al 27��K 39�� S 32
������ѡ���⣬��48�֣�
һ��ѡ���⣨ÿС��ֻ��һ��ѡ��������⡣ÿС��3�֣���48�֣�
1�������ġ�ˮ��������Water Cube���DZ������˻���Ӿ�ݡ��������������л�ϸ������Ȼͼ���Լ������ݵ��γɡ���������ĵ���ɫ����ǽ֮�ڣ��ֽṹ�Ļ�����λ��һ����12��������κ�2��������������ɵļ���ϸ�������������ܵ��ǰ��������ݣ���ΪPTFEĤ�����ķ���ϩ��������Ϊ���ݴ����������Ȼ�⡣����˵������ȷ����
A. PTFE����ʹ��ˮ��ɫ������������ B. PTFE��ͨ���Ӿ۷�Ӧ�ϳɵ�
C. PTFE�ĵ�����CF2=CF2���������� D. PTFE��ѧ�ȶ��ԡ���ĥ������
2�����������У����ܷ���������������
A����������Һ������ B��������Һ�������� C��������Һ������ D��Ӳ֬������Һ
3����������������
| A�� | B�� |
| ��H��I�����ܴ���H��Cl������ | ��HI��HCI�ȶ� |
| ��H��I������С��H��C1������ | ��HCl��HI�ȶ� |
| ��HI���Ӽ�����������HF���Ӽ������� | ��HI�е��HF�� |
| ����HI���Ӽ�������С��HCl���Ӽ������� | ��HI�е��HCl�� |
B����������ȷ��������A�����������ȷ���͵���
A.��١������������� B����ڡ����������� C����ۡ������������� D������
4���ؽ�������ʹ�����ж�������������ʹ�����ڵĵ�����
A��������ˮ������ B���������������á�C�������˱������á�D�������˷ֽⷴӦ
5��ˮ��״̬��������Һ��̬�⣬���в���̬��������Һ̬ˮ������ȴ��165Kʱ�γɵģ�����̬��ˮ�̶���״�������ھ���ṹ�����ܶ�����ͨҺ̬ˮ���ܶ���ͬ���йز���̬ˮ��������ȷ����
A��ˮ��Һ̬��Ϊ����̬�������С������ B��ˮ��Һ̬��Ϊ����̬���������
C������̬��ˮ��һ������״̬���������� D������̬ˮ�Ƿ��Ӿ���
6�������۽��͵���ø�Ļ������벣��ֽ���У����ã�������������ˮ�У��൱һ��ʱ���ȡ������Һ��ֱ����ˮ������Cu(OH)2�����ȣ���ŨHNO3���ȣ����ã�������������
A������ɫ���������Ի�ɫ������������ B������ɫ����ɫ������������
C���������������Ի�ɫ������������ D��������ɫ�������Ի�ɫ
7�������ǡ����ᡢ������Ҵ�����һ���Լ����Լ��������Լ���
A. ������Һ�������� B. Na2CO3��Һ�� ���� C. ˮ��������D. ����Cu(OH)2����Һ
8�������������£�����ˮ��������Է���������ͬ���������ʵ��л�����
�������ǡ������ǡ�����ѿ�ǡ��ܼ����������һ�ȱ��顡��������
A.�٢ڢݢޡ����� B.�ڢۢݡ����� C.�ڢޡ�������D.�ڢۢܢ�
9�������Ӿ����в����ڵ��������
A�����Ӽ��������� B�����Լ��������� C���Ǽ��Լ��������� D�������߶�˹��
10����������������֬����
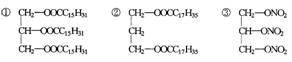 �������͡��ݻ����� ��ʯ��
�������͡��ݻ����� ��ʯ��
A.�٢ڡ��������� B.�٢ݡ������������� C.�ܢݡ����������� D.�٢�
11��������������ȷ����
A. �ܷ���������Ӧ���һ�������ᡡB.���ۡ���ά�ء���֬�����ڸ߷��ӻ�����
C. ��Ȼ������ˮ������ղ�����a-�����ᡡD. ��֬ˮ���õ��Ĵ��DZ�����
12������3.42g�����3.24g��ϲ���ȫˮ�⣬������mg�����Ǻ�ng���ǣ���m��nΪ
�������ã��������£����ã��������ã����ã��������ģ����ã�
13�����и�������У��������ȳ������ܽ�����Ϊ
����Na2CO3��Һ��ͨ�������CO2����Fe(OH)3��������μ��������ϡ�������AgI��������μ��������ϡ�������ʯ��ˮ��ͨ�������CO2�����������Һ����ε������������
A���٢ڢۡ� B���ڢۢݡ���C���٢ڢۢݡ���D���٢ۢ�
14�����о��壬ÿ��ԭ�Ӷ������ڵ�4��ԭ�Ӱ�Χ���Թ��ۼ������γ���������ṹ������ռ䷢չ������״�ṹ����
A�����龧�塡����B������衡������C��ʯī�������� D��ˮ��
15�����������С����� (NH4)2S�� �� H2S�� �� Al(OH)3�� �� AgNO3�� �ݸʰ��ᣬ���������ᷴӦ�������백ˮ��Ӧ����
A.�٢� ������ B.�ڢۡ����������� C.�ܢݡ� ������������D.�٢ܢ�
 16��SF6��һ����ɫ���壬���к�ǿ���ȶ��ԣ����������SF6
16��SF6��һ����ɫ���壬���к�ǿ���ȶ��ԣ����������SF6
�ķ��ӽṹ��ͼ��ʾ�������������͡����FԪ����������
����ͬλ�أ���SF6�IJ�ͬ��������Ϊ
A��6�֡� B��7�֡���C��10�֡���D��12��
��������ѡ���⣬��52�֣�
��������⣨��3�⣬��26�֣�
17����6�֣���1��ij�ָ�ǿ�ȵ���ά�����ֵ�����ɣ���ṹΪ��
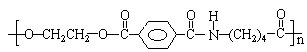
�������ֵ���Ľṹ��ʽ�ֱ�Ϊ_____________��______________��_____________���ϳ����ָ߷��Ӳ��ϵķ�Ӧ����Ϊ�������������� ��
![]() ��2���ϳɽṹ��ʽΪ
��2���ϳɽṹ��ʽΪ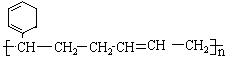 �ĸ߾���䵥��Ľṹ��ʽӦ����������������������������
������������������������
��
�ĸ߾���䵥��Ľṹ��ʽӦ����������������������������
������������������������
��
18����4�֣�Pt (NH3)2 Cl2��ƽ���ı��νṹ���������γ����ֹ��壬һ��Ϊ����ɫ����ˮ���ܽ�Ƚ�С����һ��Ϊ����ɫ����ˮ���ܽ�Ƚϴ�
(1)���������ֹ�����ӵļ��ι���ͼ������������������������������������������ ��
(2)����ɫ�����ܽ�ȴ��ԭ���ǣ��������������������������������������������� ��
19����8�֣�X��Y��Z�����ֳ����Ķ�����Ԫ�أ����ǿ����γ�XY2��XY3��Z2X��Z2Y��Z2Y2�Ȼ������֪Xԭ�ӱ�Yԭ�Ӷ�һ�����Ӳ㣬Y�õ����Ӵﵽ8�����ȶ��ṹʱ��Z��������ͬ�ĵ��Ӳ�ṹ��
��1��X������������ ��Y������������ ����Ԫ�ط��ţ���
��2��Z�ĵ��������������� ���壬д��Z2Y2�ĵ���ʽ�������� ��
20��(8��)��֪�Ȼ������۵�Ϊ190�棨2.202��105Pa����������180�漴��ʼ������
��1���Ȼ��������������������������������� ��������ӻ���������ۻ��������
��2����500K��1.01��105Paʱ�����������ܶȣ�����Ϊ��״��ʱ��Ϊ11.92g��L��1����ȷ���Ȼ���������״̬ʱ�Ļ�ѧʽΪ������������ �������������������������� ��
��3����ˮ�Ȼ����ڳ�ʪ�Ŀ�����ǿ�ҵط����̡�����ԭ��������������������������������
��4�����֤���Ȼ��������ӻ����ﻹ�ǹ��ۻ�����������������
�����ƶ��⣨��2�⣬��16�֣�
21����8�֣���������������HNO2��Ӧ�æ����ǻ��ᣬ�磺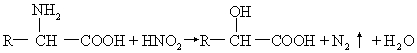
��д�����и��仯�У�a��b��c��d�����л���Ľṹ��ʽ��
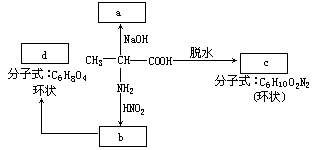 �ش�a________��b________��
�ش�a________��b________��
c________��d________��
22����8�֣��л���A�ķ���ʽΪ��3��7��2�Σ��л���µķ���ʽΪ��3��9��2�Σ��������л���ķ��ӽṹ�ж���һ����̼ԭ�������ļ������Ƕ�����NaOH��Һ��Ӧ��Ҳ������H2SO4��Ӧ������д���¿ո�
�������л���A��B�Ľṹ��ʽ���������������������������� ��B�������������������� ��
������A�����ᷴӦ�Ļ�ѧ����ʽ���������������������������������� ��
B��NaOH��Ӧ�Ļ�ѧ����ʽ���������������������������������� ��
�ġ������⣨10�֣�
23����4�֣�1986�꣬��ʿ��λ��ѧ�ҷ���һ���������õĽ��������ﳬ���壬ʹ��������ȡ��ͻ���Խ�չ��Ϊ����λ��ѧ�һ����1987���Nobel����ѧ�����侧���ṹ��ͼ��
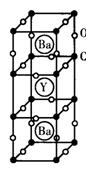 (1)����ͼʾ�����ṹ�����㾧����Y��Cu��Ba��Oԭ�Ӹ�����Ϊ ������������
(1)����ͼʾ�����ṹ�����㾧����Y��Cu��Ba��Oԭ�Ӹ�����Ϊ ������������
(2)�û������и�Ԫ�صĻ��ϼ�ΪYΪ+3�ۣ�BaΪ+2�ۣ�CuΪ+2��+3�ۣ����ݻ��������ɣ����㻯������+2��Cu��+3��Cuԭ�Ӹ�����Ϊ�������� ��
25����6�֣�ʯ�ͻ����ǽ���ʡ��֧����ҵ֮һ��������ϩ����;ʮ�ֹ㷺��ʯ�ͻ�����Ʒ��ij���������������й�������������ϩ�ĵ�������ϩ��
��CH2��CH2��Cl2��CH2Cl��CH2Cl ��CH2Cl��CH2Cl��CH2��CHCl��HCl
��ش��������⣺
(1)��֪��Ӧ���ж�������IJ��ʣ�����=ʵ�ʲ���/���۲���´100%��Ϊ98%����Ӧ��������ϩ���Ȼ���IJ��ʾ�Ϊ95%����2.8t��ϩ���Ƶ�����ϩ�� t��ͬʱ�õ��������Ȼ���������t������������1λС������
(2)Ϊ������ø������Ȼ��⣬�ù������������з�Ӧ������������
����2CH2��CH2��4HCl��O2��2CH2Cl��CH2Cl��2H2O
�ɷ�Ӧ�١��ۻ�ö������飬�ٽ���������ͨ����Ӧ�ڵõ�����ϩ�������Ȼ��⣬�������Ȼ����Ӧ��ʹ�ã��γ����µĹ��ա�
���ڸ���Ӧ�Ĵ��ڣ�������Ͷ�����ϩȫ��������ʱ����Ӧ�١����ж�������IJ�������Ϊa%��c%����������ȫ��������ʱ����Ӧ�����Ȼ���IJ���Ϊb%���Լ��㣺��Ӧ�١�������ϩ��Ͷ�ϱ�Ϊ����ʱ���¹��ռȲ���Ҫ�����Ȼ���Ϊԭ�ϣ���û�и������Ȼ���ʣ�ࣨ�����ڷ����ĸ���Ӧ�мȲ������Ȼ��⣬Ҳ�������Ȼ��⣩��
�߶���ѧ����
������ѡ���⣬��48�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| ѡ�� |
|
|
|
|
|
|
|
|
|
|
| ��� | 11 | 12 | 13 | 14 | 15 | 16 |
|
|
|
|
| ѡ�� |
|
|
|
|
|
|
|
|
|
|
��������ѡ���⣬��52�֣�
��������⣨��3�⣬��22�֣�
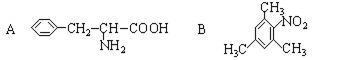 17����4�֣�
17����4�֣�
18����4�֣�(1)����ɫ�ܽ��С���ǡ�����������ɫ�����ܽ�ȴ����
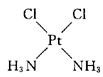

(2)��Ϊ���ӽṹ���Գƣ����Է����м��ԣ������ˮ���ܽ�ȴ�
19����6�֣�
��1��X������ S���������� ��Y��������O���������� ��Z������ Na�������� ��
��2��Z�ĵ��������������� ���壬Z��Y�γ�Z2Y�Ĺ��̿��õ���ʽ��ʾΪ �ԡ����� ��
20��(8��)
��1���Ȼ��������ۻ����� ��2����ѧʽΪ��Al2Cl6����
��3����ˮ�Ȼ����ڿ�����ǿ�ҵķ����̡�����ԭ����������ˮ����
��4�����һ���ɿ���ʵ�飬�ж��Ȼ��������ӻ����ﻹ�ǹ��ۻ����� ����ʱ�Ƿ硡�����ƶ��⣨��3�⣬��20�֣�
21����4�֣�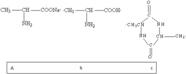
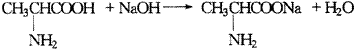 22����8�֣�����������������£������
22����8�֣�����������������£������
�����������Σ�ϣȣ�
�£��Σ�ϣȣ��ã�3�ã�2�ãϣϣΣ�4���Σ�ϣ�![]() �ã�3�ã�2�ãϣϣΣᣫ�Σ�3������2��
�ã�3�ã�2�ãϣϣΣᣫ�Σ�3������2��
23����8�֣�
(1) A��B��������ķ���ʽ�� C5H9O4N��������
(2) ��A�Ľṹ��ʽΪ���Ȱ��ᡡ �������� ��
(3) ��B�Ľṹ��ʽ�� OHC-��CH2��4-NO2���� ��
�ġ������⣨10�֣�
24����4�֣�(1)��ѧʽ:YBa2Cu3O7�� (2)Cu2+:Cu3+=2:1
25����6�֣�(1)2.8t��ϩ���Ƶ�����ϩ 5.8��t��ͬʱ�õ��������Ȼ����� 3.4�� t������������1λС������
(2)��200c��bc����ab ע�⣨2���𰸣����ڢ۵ĸ���Ӧ�Ȳ������Ȼ���Ҳ�������Ȼ��⣬���ԣ�����ȥ2mol CH2��CH2������2c%mol CH2Cl��CH2Clʱ���ĵ�HCl�����ʵ�������4mol����4c%mol��