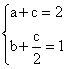高二化学气体等效平衡练习题 气体等效平衡专题讲练 命题:岳全国
一、可逆反应在恒温、恒容条件下建立等效平衡
结论:等温等容,只要对应物起始量等物质的量,平衡时对应物就能同浓度、同百分含量、同转化率、同反应速率。记为:等温等容等摩。
![]() 若 aA(g) + bB(g)
cC(g)
若 aA(g) + bB(g)
cC(g)
Ⅰ a mol b mol 0
Ⅱ x y z
Ⅰ、Ⅱ要达成相同平衡必须满足的条件是x + z![]()
![]() = a 和 y + z
= a 和 y + z![]() = b
= b
【例】在一个体积固定的密闭容器中加入2 mol A和1 mol B,发生反应:
2A(g)+B(g)![]() 3C(g)+D(g),达到平衡时C的浓度为a
mol・L-1。若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为a mol・L-1的是( D )
3C(g)+D(g),达到平衡时C的浓度为a
mol・L-1。若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为a mol・L-1的是( D )
A.4molA+2molB B.2molA+1molB+3molC+1molD
C.3molC+1molD+1molB D.3molC+1molD
二、可逆反应在恒温、恒压条件下建立等效平衡
结论:等温等压,只要对应物起始量等物质的量之比,平衡时对应物就能同浓度、同百分含量、同转化率、同反应速率。记为:等温等压等摩尔比。
若 aA(g) + bB(g) ![]() cC(g)
cC(g)
Ⅰ a mol b mol 0
Ⅱ x y z
Ⅰ、Ⅱ要达成相同平衡必须满足的条件是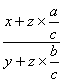 =
= ![]()
【例】.某恒温恒压下,向可变容积的密闭容器中充入3升A和2升B,发生如下反应: 3A(气)+2B(气)=xC(气)+yD(气) 达到平衡时C的体积百分比为m %,若维持温度,压强不变,将0.6升A,0.4升B、4升C、0.8升D作为起始物质充入密闭容器内,则达到平衡时C的体积百分比仍为m%,则x= 5n ,y= n 。(n为自然数)
三、反应前后气体体积不变的可逆反应在恒温、恒容条件下建立等效平衡
结论:若对应物起始量等物质的量之比而不等物质的量,平衡时对应物只能同百分含量,而浓度、转化率、反应速率均不等。
【例1】可逆反应A(g)+B(g)![]() 2C(g)在固定容积的容器中进行,a. 如果向容器中充入1mol A和1mol B,在某温度下达到平衡;b. 若向容器中充入1mol C,在同样的温度下达到平衡:(1)C物质平衡浓度 a > b (2) C物质体积分数 a = b
2C(g)在固定容积的容器中进行,a. 如果向容器中充入1mol A和1mol B,在某温度下达到平衡;b. 若向容器中充入1mol C,在同样的温度下达到平衡:(1)C物质平衡浓度 a > b (2) C物质体积分数 a = b
(3) A物质的转化率 a = b (4)平衡时的反应速率 a > b
【例2】在一密闭的容器中充入2mol A和1mol B发生反应:
2A(g)+B(g)![]() xC(g),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为w%,则x的值为( C )
xC(g),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为w%,则x的值为( C )
A. 只能为2 B.只能为3 C. 可能为2,也可能为3 D. 无法确定
四、通过建立等效平衡中间状态,比较反应物转化率的大小以及平衡时某物质体积分数、浓度的大小
【规律总结】对于气体参加的可逆反应,在温度恒定的条件下,涉及体积与压强以及平衡移动有关判断的问题时,可设计一些等效平衡的中间状态来进行求解。这样能降低思维难度,具有变难为易、变抽象为直观的作用。
【例1】在相同温度下,有相同体积的甲、乙两容器,甲容器中充入1g N2和1g H2,乙容器中充入2g N2和2g H2。下列叙述中,错误的是( D )
A.化学反应速率:乙>甲 B.平衡后N2的浓度:乙>甲
C.H2的转化率:乙>甲 D.平衡混合气中H2的体积分数:乙>甲
【例2】 甲、乙两容器,甲的容积固定,乙的容积可变。在一定温度下,向甲中通入3mol N2和4mol H2,反应达到平衡时,生成NH3的物质的量为amol。
(1)相同温度下,向乙中通入2molNH3,且保持容积与甲相同,当反应达到平衡时,各物质的浓度与甲平衡中相同。起始时乙中还通入了____mol N2和____mol H2。
(2)相同温度下,若向乙中通入6mol N2和8mol H2,且保持压强与甲相等,当反应达到平衡时,生成氨的物质的量为b mol,则a∶b______1∶2;若乙与甲的容积始终相等,达到平衡时,生成氨的物质的量为c mol,则a∶c_____1∶2 (填“>”、“<”或“=”)。
答案:(1)2mol N2和1mol H2
(2)平衡氨的物质的量物质的量b=2a,所以a∶b=1∶2
平衡时氨的物质的量物质的量c>2a,即a∶c<1∶2。
【例3】 当温度一定时分别往下列容器中充入氢气和氮气,发生如下反应:
![]()
![]()
![]() 。A.
。A. ![]() B.
B. ![]()
(1)在恒容容器中
(2)在恒压容器中
充分反应达到平衡时,这两种情形下,氮气的转化率、各物质平衡浓度、平均相对分子质量怎样变化?
答案:(1) 氮气转化率B > A 各物质平衡浓度B > A 平均相对分子质量B > A
(2)氮气转化率B = A 各物质平衡浓度B = A 平均相对分子质量B = A
气体等效平衡练习 命题:岳全国
班 姓名 学号
选择题(每题有1~2个正确答案)
1.在一定温度下的固定容积的密闭容器中,当下列物理量不再变化时,表明反应:A(s)+2B(g) ![]() C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的总物质的量
2.在温度不变下,在恒压容器a与恒容容器b中,分别充入体积比为1∶3的N2和H2。若开始时两容器的体积相等,且在相同条件下达到平衡时,两容器中N2的转化率应当是
A.a中大 B.b中大 C.a、b中一样大 D.无法判断
3.恒温条件下,将NO2装入带活塞的密闭容器中,当反应2NO2(g) ![]() N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是
N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是
A.若体积减小一半,则压强为原来的两倍
B.平衡向右移动,混合气体颜色一定会变浅
C.若体积减小一半,压强增大,但小于原来的两倍
D.平衡向右移动,混合气体密度增大
4.在一定温度下,容器中加入CO和H2O(g)各1mol,发生反应:
CO+H2O![]() CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件不变,一开始就加入4mol H2O(g),则达到平衡可能生成的CO2是
CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件不变,一开始就加入4mol H2O(g),则达到平衡可能生成的CO2是
A.0.6mol B.0.95mol C.1mol D.1.5mol
5.可逆反应A(g)+B![]() C(g)+D 达到平衡时,下列说法不正确的是
C(g)+D 达到平衡时,下列说法不正确的是
A.若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体
B.增大压强,平衡不移动,说明B、D必定是气体
C.升高温度,C的百分含量减少,说明正反应是放热反应
D.若B是气体,增大A的浓度会使B的转化率增大
6.在一密闭容器中充入1mol
NO2,建立如下平衡:2NO2![]() N2O4,此时NO2的转化率为x%,在其他不变的情况下,再充入1mol NO2,待新平衡建立时测得NO2的转化率为y%,则下列大小关系正确的是
N2O4,此时NO2的转化率为x%,在其他不变的情况下,再充入1mol NO2,待新平衡建立时测得NO2的转化率为y%,则下列大小关系正确的是
A.x>y B.x=y C.x<y D.不能确定
7.将2molSO2和2molSO3气体混合于容积一定的密闭容器中,在一定条件下发生反应:2SO2+O2![]() 2SO3,达平衡时SO3为n mol。在相同温度下,按下列配比在该容器中放入起始物质,达平衡时,SO3的物质的量将大于n mol的是
2SO3,达平衡时SO3为n mol。在相同温度下,按下列配比在该容器中放入起始物质,达平衡时,SO3的物质的量将大于n mol的是
A.2molSO2和1molO2 B.2molSO2、1molO2和2molSO3
C.4molSO2和1molO2 D.3molSO2、1molO2和1molSO3
8.在四个同样密闭容器中发生反应:A(g)+3B(g) ![]() 2C(g),在同一时间内测得容器内的反应速率:甲为:v (A)=3 mol/(L・min);乙为v (B)=4.5 mol/(L・min);
2C(g),在同一时间内测得容器内的反应速率:甲为:v (A)=3 mol/(L・min);乙为v (B)=4.5 mol/(L・min);
丙为v (C)=4 mol/(L・min);丁为v (A)=0.75mol/(L・s)。若其它条件相同,温度不同,则温度由低到高的顺序是__________ _______。
9.一定温度下,在一个固定容积的密闭容器中,可逆反应:A(g)+2B(g) ![]() C(g)达到平衡时,
C(g)达到平衡时,![]() (A)=2mol・L-1,
(A)=2mol・L-1,![]() (B)=7mol・L-1,
(B)=7mol・L-1,![]() (C)=3mol・L-1。试确定B的起始浓度
(C)=3mol・L-1。试确定B的起始浓度![]() (B)的取值范围是______________;若往容器中继续注入一定量的氦气(不参加反应),足够长的时间后,体系中B的物质的量浓度_________(填“增大”、“减小”或“不变”,下同),混合气体的密度_________。
(B)的取值范围是______________;若往容器中继续注入一定量的氦气(不参加反应),足够长的时间后,体系中B的物质的量浓度_________(填“增大”、“减小”或“不变”,下同),混合气体的密度_________。
10.在一定条件下,x A+y B![]() z C的反应达到平衡。
z C的反应达到平衡。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是__________________;
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则平衡一定向_____________移动;
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不发生移动,则A是_____________态物质。
(4)若加热后C的质量分数减少,则正反应是_________(填“放热”或“吸热” )反应。
11.有两只密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等物质的量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等(如下图所示)。在保持400℃的条件下使之发生如下反应:2SO2+O2![]() 2SO3。试填写下列空格:
2SO3。试填写下列空格:
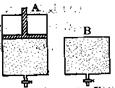
(1)A容器达到平衡时所需的时间比B容器__________;平衡时A容器中SO2的转化率比B容器_______;
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等物质的量的氩气,A容器中化学平衡_________移动,B容器中化学平衡__________;
(3)达到(1)所述平衡后,若向两容器中通入等物质的量的原反应气体,达到平衡时,A容器的混合气体中SO3的体积分数_________(填“增大”、“减小”或“不变”,下同);B容器的混合气体中SO3的体积分数_________。
12.在一容积固定的容器中通入2 mol SO2和1mol O2发生反应:
2SO2+O2![]() 2SO3,当此反应进行到一定程度时,就达到了化学平衡状态。若该容器中维持温度不变,令a、b、c分别代表起始的SO2、O2和SO3的物质的量,如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保持达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时完全相同。试填写下列空白:
2SO3,当此反应进行到一定程度时,就达到了化学平衡状态。若该容器中维持温度不变,令a、b、c分别代表起始的SO2、O2和SO3的物质的量,如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保持达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时完全相同。试填写下列空白:
(1)若a=0,b=0,则c=______;
(2)若a=0.5mol,则b=________,c=_________;
(3)a、b、c取值必须满足的一般条件是(请用两个不同的式子表示)____________
_______________________________________。
【答案】
1.BC 2.A 3.CD 4.B 5.B 6.C 7.BD
8.乙<丙<甲<丁(提示:温度越高,化学反应速率越快)。
9.3mol・L-1~13mol・L-1;不变;增大。
10.(1)x+y>z;(2)逆反应方向;(3)固态或液态;(4)放热。
11.(1)短;大;(2)向逆反应方向;不移动;(3)不变;增大。
12.(1)2;(2)0.25,1.5;(3)![]() ;
;