第一学期第三次阶段测试
高二化学试题
时间:100分钟 总分:120分
注意:
①可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cl 35.5 Fe 56 Br 80
②请将第I卷答案填入选择题答题栏
第Ⅰ卷(选择题 共60分)
一、选择题(本题包括7小题,每小题4分,共28分。每小题只是一个选项符合题意)
1. 既能发生水解反应,又能发生氢化反应的是
A.油酸甘油酯 B.软脂酸甘油酯 C.油酸 D.苯酚
2. 生活中的一些问题常涉及到化学知识,下列叙述不正确的是
A.糯米中的淀粉一经发生水解反应,就酿造成酒
B.福尔马林是一种良好的杀菌剂,但不可用来消毒饮用水
C.棉花和木材都富含纤维素
D.室内装饰材料中缓慢释放出的甲醛、甲苯等有机物会污染空气
3. 新兴的大脑营养学研究发现,大脑的生长发育与不饱和脂肪酸有密切关系。被称为脑黄金的DHA就是一种不饱和程度很高的脂肪酸,它的分子中有6个C═C键,学名二十六碳六烯酸,它的分子组成是
A.C25H50COOH B.C25H39COOH C.C26H41COOH D.C26H47COOH
4.
下列物质中最难电离出![]() 的是
的是
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
5.
国家食品卫生标准规定,酱油中3-氯丙醇![]() 含量不超过
含量不超过![]() 。相对分子质量为94.5的氯丙醇(不含
。相对分子质量为94.5的氯丙醇(不含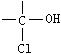 结构)共有
结构)共有
A.2种 B.3种 C4种 D.5种
6.
由—![]() 、—OH、
、—OH、![]() 、—COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有
、—COOH四种基团两两组合而成的化合物中,其水溶液显酸性的有
A.5种 B.4种 C.3种 D.2种
7. 等质量的铜片,在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是
A.硝酸 B.无水乙醇 C.石灰水 D.盐酸
二、选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
8.
化合物![]() 中的—OH被卤原子取代所得的化合物称为酰卤,下列化合物中可以看做酰卤的是
中的—OH被卤原子取代所得的化合物称为酰卤,下列化合物中可以看做酰卤的是
A.HCOF B.![]() C.
C.![]() D.
D.![]()
9.
将![]() 和
和![]() (甘油)以一定比例混合,测得混合物含碳51.3%,那么氧元素的质量分数是
(甘油)以一定比例混合,测得混合物含碳51.3%,那么氧元素的质量分数是
A.40% B.35% C.30% D.无法计算
10.
胆固醇是人体必需的生物活性物质,分子式为![]() ,一种胆固醇脂是液晶材料,分子式为
,一种胆固醇脂是液晶材料,分子式为![]() ,合成这种胆固醇脂的酸是
,合成这种胆固醇脂的酸是
A.![]() B.
B.![]()
C.![]() D.
D.![]()
11. 可以判断油脂皂化反应基本完成的现象是
A.反应液使红色石蕊试纸变蓝色 B.反应液使蓝色石蕊试纸变红色
C.反应后静置,反应液分为两层 D.反应后静置,反应液不分层
12. 人类在地球上的活动致使一年内产生的CO2(主要是煤和石油的利用)约达200亿吨,若植物将这些CO2全部转化为淀粉,那么最终由此而生成的淀粉质量最接近
A.1200亿吨 B.120亿吨 C.200亿吨 D.400亿吨
13.
已知乙烯醇(![]() )不稳定,可自动转化为乙醛;二元醇可脱水生成环状化合物,现有1 mol乙二醇在一定条件下脱去1mol
)不稳定,可自动转化为乙醛;二元醇可脱水生成环状化合物,现有1 mol乙二醇在一定条件下脱去1mol
![]() ,所得产物的结构简式有下列几种,其中不可能的是
,所得产物的结构简式有下列几种,其中不可能的是
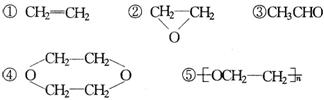
A.只有① B.只有①④ C.只有①⑤ D.只有①⑤⑥
14.
最近,媒体报道不法商贩销售“致癌大米”,已验证这种大米中含有黄曲霉毒素(AFTB),其分子结构式为如图所示,人体的特殊基因在黄曲霉素的作用下会发生突变,有转变为肝癌的可能。一般条件下跟1mol AFTB起反应的![]() 或NaOH的最大量分别是
或NaOH的最大量分别是
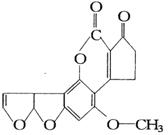
A.6mol;1mol B.5mol;1mol
C.6mol;2mol D.5mol;2mol
15.
化合物![]() 与NaOH溶液、碘水三者混和后可发生如下反应:
与NaOH溶液、碘水三者混和后可发生如下反应:
①I2+2NaOH=NaI+NaIO+H2O
![]()
![]()
此反应称为碘仿反应,根据上述反应方程式,推断下列物质中能发生碘仿反应的有A.![]() B.
B.![]()
C.![]() D.
D.![]()
第Ⅰ卷 选择题(共60分)
答题栏
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 |
|
|
|
|
|
|
|
|
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
|
| 答案 |
|
|
|
|
|
|
|
|
第Ⅱ卷 非选择题 (共60分)
三、(本题包括2小题,共15分)
16.
(6分)醛类易被氧化成羧酸,向乙醛中滴入酸性![]() 溶液,可观察到的现象是_____________________。现已知柠檬醛的结构式为:
溶液,可观察到的现象是_____________________。现已知柠檬醛的结构式为:
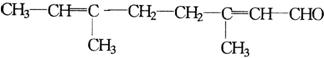
(1)柠檬醛中存在的官能团的名称是__________________________________。
(2)若要检验柠檬醛中的“C=C”,其实验方法是_______ ______
______________ __。
17. (9分)已知:卤代烃和醇在不同条件下可发生转化:为验证乙醇分子中含有氧原子,现采用以下装置进行实验。
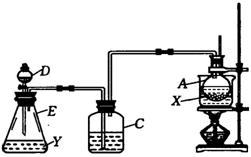
Ⅰ.装置中所装试剂:A瓶装不含水的乙醇及无水盐X;C和D中都装浓硫酸;E瓶中装试剂Y
Ⅱ.实验操作及现象是:水浴加热A瓶,将D中浓硫酸缓缓滴入E中与试剂Y作用,发现C中导管有大量气泡放出;A瓶内X逐渐变色。请回答下列各问题:
(l)E瓶里所装的试剂Y是以下物质中的_______________。
A.饱和食盐水 B.MnO2和NaCI的混合物 C.浓盐酸
C瓶中浓硫酸所起的作用是______________________________________________。
(2)无水盐X可选用________________,请用化学方程式表示此实验能证明乙醇分子中含有氧原子的原理_________________________________________________________。
(3)某同学按上图装配好仪器,然后因事离开了一段时间,当他回到实验室时,发现A瓶内X已经变色,这是因为___________________________________________________,请对上图装置作简单的改进以避免此因素干扰实验,其方法是______________________。
四、(本题包括2小题,共17分)
18. (6分)据报道,某省又发生一起毒鼠强多人中毒案,控制毒鼠强的使用及寻找新的安全鼠药已成为热点问题。已知毒鼠强由C、H、O、N、S五种元素组成,其原子个数之比为2:4:2:2:1,其分子结构如图1所示。试回答:
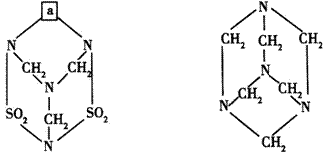

图1 图2
(1)毒鼠强的分子式是________________________________。
(2)在毒鼠强的分子结构中的方框内a为______________原子团。
(3)已知在医药上用作抗流感和抗风湿的药物乌洛托品的分子结构如图2所示,则下列关于乌洛品与毒鼠强的关系正确的是____________________。
A.两者属同系物 B.两者均有剧毒
C.两者都属烃的衍生物 D.两者都是高分子化合物
19. (11分)乙醛是重要的化工原料和化学试剂。实验室可用乙醇制乙醛,工业上目前使用两种方法制取乙醛:①乙炔水化法 ② 乙烯氧化法。两种制法制乙醛的有关信息见下表:
| 物质 项目 | 乙炔水化法 | 乙烯氧化法 |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4、100℃~125℃ | PdCl2~CuCl2 100℃~125℃ |
| 平衡转化率 | 乙炔转化率 90% | 乙烯转化率 80% |
| 日产量 | 2.5t(某设备条件下) | 3.6t(相同设备条件下) |
| 原料来源生产工艺 | CaCO3 CaC2 | 石油裂解气 |
(1)写出下列化学方程式:
实验室乙醇制乙醛__________________________________________________
乙炔水化法制乙醛__________________________________________________
(2)将乙醛滴入新制的氢氧化铜悬浊液并加热,其现象是______________,反应的化学方程式为_____________________________________________。
(3)比较两种乙醛的工业制法,从化学反应速率的角度分析,在相同的条件下,较快的是__________(填字母)
A.乙炔水化法 B.乙烯氧化法
(4)现代工业上乙烯氧化法有逐步取代乙炔水化法的趋势,试通过表中提供的信息,说出其中的两个原因:_______________________________、__________________ _ _______
五、(本题包括2小题,共16分)
20. (8分)请根据下面的反应路线及所给的信息,用中学化学知识回答问题:
![]()
已知A是一种直链一溴代物,1molA最多与2molH2反应生成1molG,F是环状化合物,环上有5个原子,其化学式为C4H6O2。
(1)化合物F的结构简式是______________,化合物C的结构简式是_____________。
(2)化合物A含有的官能团是溴原子、碳碳双键、__________________________。
(3)1molA与2molH2的化学方程式是__________________________________________。
21. (8分)乙酸苯甲酯常用于食品和化妆品工业,可以用下列方法进行合成:
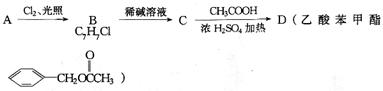
(1) 写出A、C的结构简式
A___________________________;C_______________________________。
(2)D有多种同分异构体,含有酯基的一取代苯结构的同分异构体还有五个,其中三个的结构简式是:
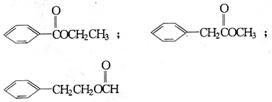
请写出另外两个同分异构体的结构简式:
____________________________;__________________________________。
六、(本题包括2小题,共12分)
22. (6分)有三种饱和一元醇A、B、C,其相对分子质量之比为8:15:22。按其物质的量之比为1:2:1混合,取该混合液12g与足量钠反应,生成氢气2.24L(标准状况),求A、B、C的分子式。
23.
(6分)某晶体A的水溶液呈中性,燃烧0.2molA物质可得到26.88L(标准状况)![]() ,生成水21.6g,又知A的相对分子质量为甲醛的6倍,A能发生银镜反应,当与乙酸发生酯化反应时,A与乙酸的质量比为3:5,求A的分子式并写出其结构简式
,生成水21.6g,又知A的相对分子质量为甲醛的6倍,A能发生银镜反应,当与乙酸发生酯化反应时,A与乙酸的质量比为3:5,求A的分子式并写出其结构简式
高二化学试题参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | A | A | B | B | B | B | C | AC |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
|
| 答案 | A | B | D | B | A | C | BC |
|
16.(6分)褪色 (1)烯键、醛基 (2)先加入新制![]() 悬浊液,加热,过滤后,酸化(控制pH≤7),再滴入溴水出现褪色
悬浊液,加热,过滤后,酸化(控制pH≤7),再滴入溴水出现褪色
17、(9分)(l)C(1分) 干燥HCI气体(1分)
(2)无水硫酸铜(1分) ![]() (2分)
(2分)
![]() (2分)
(2分)
(3)比空气轻的水蒸气进入了A装置(1分)在A装置的竖直导管上加干燥器(1分)
18.(6分)(1)C4H8O4N4S2 (2)![]() (3)C(各2分)
(3)C(各2分)
19(11分).(1)2CH3CH2OH+O2
![]() 2CH3CHO+2H2O ;CH≡CH+H2O
2CH3CHO+2H2O ;CH≡CH+H2O![]() CH3CHO
CH3CHO
(2) 有红色沉淀生成(1分);CH3CHO+2Cu(OH)2 ![]() CH3COOH +Cu2O ↓+2H2O
CH3COOH +Cu2O ↓+2H2O
(3)B
(4) 乙炔水化法使用HgSO4 作催化剂,毒性大;乙烯氧化法日产量高,反应快;原料气乙炔要经过多步反应制得,且消耗大量的电能,热能,较难获得;原料乙烯来源于石油裂解气,消耗总能量 比乙炔少,且易获得。(只要答出其中的两点就给2分)
20、(8分)(各2分) (1)
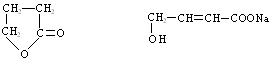

(2)醛基(或—CHO)
(3)CH2Br—CH=CH—CHO+2H2![]() CH2Br—CH2—CH2—CH2OH
CH2Br—CH2—CH2—CH2OH
21、答:(各2分)
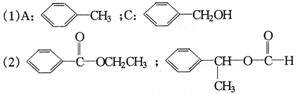
22.(6分)A:![]() ;B:
;B:![]() ;C:
;C:![]()
23、(6分)![]()
![]()