�߶��꼶�ϲ���ĩ���Ի�ѧģ������(��)
�ڢ����ѡ���⣩
һ��ѡ����(ÿ��ֻ��һ����ȷѡ�ÿ��3�֣���24�֡�)
1����֪25 �� ʱ��AgCl ���ܶȻ�Ksp=1.8��10-10��������˵����ȷ���ǣ�
A����AgClˮ��Һ�м������ᣬKspֵ���
B��AgNO3��Һ��NaCl��Һ��Ϻ����Һ�У���һ����c(Ag+)=c(Cl-)
C���¶�һ��ʱ������Һ��c(Ag+)��c(Cl-)=Kspʱ������ҺΪAgCl�ı�����Һ
D��������AgCl���뵽��Ũ��KI��Һ�У��в���AgClת��ΪAgI��˵��AgCl�ܽ��С��AgI
2�������£�ij��ɫ����Һ����ˮ���������H+��OH��Ũ�ȵij˻�Ϊ1��10��24�������Һ�п��ܴ��������������Ϊ
A��HCO3����Al3+��Na+��SO42������ ������B��I����NO3����K+��NH4+
C��MnO4����Cl����SO42����K+�� �������� D��SiO32����SO32����Na+��Cl��
3����ֲ�ﻨ�п���ȡһ�ּ�дΪHIn���л������ˮ��Һ�����������ƽ�⣺
HIn(��Һ����ɫ)![]() H+(��Һ)+In��(��Һ����ɫ) ���������ָʾ����������Һ�м���Na2O2��ĩ������Һ��ɫΪ��
H+(��Һ)+In��(��Һ����ɫ) ���������ָʾ����������Һ�м���Na2O2��ĩ������Һ��ɫΪ��
A����ɫ������� B����ɫ��dz ���� C����ɫ��� ����D����Ϊ��ɫ
4����10mL pH=12��ij����Һ�м���10mL pH=2�����ᣬ��ַ�Ӧ������̪��Һ����Һ��죬��˼�һ���ǣ�
A�����������B��һԪǿ��� C����Ԫǿ�������D���κμ�
 5�����ܱ������н������з�Ӧ��M��g����N��g��
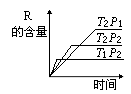
5�����ܱ������н������з�Ӧ��M��g����N��g��![]() R��g����2 L�������˷�Ӧ��������ͼ������������ȷ���ǣ�
R��g����2 L�������˷�Ӧ��������ͼ������������ȷ���ǣ�
A.����Ӧ���ȣ�L�����塡����B.����Ӧ���ȣ�L�ǹ���
C.����Ӧ���ȣ�L��Һ�塡����D.����Ӧ���ȣ�L������
6�����й���ͭ�缫��������ȷ���ǣ�������������������������������������
A��ͭһпԭ����У�ͭ��ԭ��صĸ��� �� B���õ�ⷨ������ͭʱ����ͭ������
C���ڶƼ��ϵ��ͭʱ�����ý���ͭ��������D�����ϡ������H2��O2ʱ��ͭ������
7��һ������ȼ�ϵ�أ����������Ϊ�缫����KOH��Һ�У�Ȼ��ֱ���������ͨ������������缫��Ӧʽ��C2H6 +18OH����14e��= 2CO32��+ 12H2O��7H2O+��7/2��O2+14e��=14OH�����йش˵�ص��ƶ���ȷ���ǣ�������������������
��A���������Һ�е����������ƶ���B���ŵ�һ��ʱ���KOH�����ʵ���Ũ�Ȳ���
��C��ͨ����ĵ缫Ϊ������������ D���μӷ�Ӧ��O2��C2H6�����ʵ���֮��Ϊ2��7
8����һ���ݻ�ΪV L���ܱ������з���2 L A��g����1 L B��g������һ�������·������з�Ӧ3A(g)ʮB(g)![]() nC(g)+2D(g)
�ﵽƽ���A���ʵ���Ũ�ȼ�С1/2����������ƽ��Ħ����������1/8����÷�Ӧ�Ļ�ѧ����ʽ��n��ֵ��
nC(g)+2D(g)
�ﵽƽ���A���ʵ���Ũ�ȼ�С1/2����������ƽ��Ħ����������1/8����÷�Ӧ�Ļ�ѧ����ʽ��n��ֵ��
A��1��������B��2 ���� C��3��������D��4
����ѡ���⣨ÿ����1��2����ȷѡ�ÿС��3�֣���30�֣�
9������ѪҺ������pHԼΪ7.35��7.45�������������������ͻȻ�����ı�ͻ��������ж������ж���������������Σ�ա�����������Һ�Ļ���ϵͳ�д�������ƽ�⣺
![]()
![]()
![]()
![]() H����HCO3������ H2CO3���� CO2��H2O H����PO43������HPO42������ H����HPO42������ H2PO4��
H����HCO3������ H2CO3���� CO2��H2O H����PO43������HPO42������ H����HPO42������ H2PO4��
����ά��ѪҺpH������ȶ����Ա�֤���������������˵���в��������ǣ�
A����ǿ�������ʽ����������Һ����������ϵͳ��ƽ�������ƣ��Ӷ�ά��pH�ȶ�
B����ǿ�������ʽ����������Һ����������ϵͳ��ƽ�������ƣ��Ӷ�ά��pH�ȶ�
C��ij�����ھ�����ע�Ĵ���������ˮ��ѪҺ��ϡ�ͣ��ᵼ��c(H+)�������٣�pHֵ���������ܻ�������ж�
D����������к����ʱ�����CO2����ѪҺ����ʹƽ�������ƶ���c(H+)����pHֵ�Լ�С��
10���������ӷ���ʽ��д��ȷ���ǣ�
A��̼��������ˮ��![]()
B����![]() ��ĩ�м�������HI��Һ��
��ĩ�м�������HI��Һ��![]()
C����![]() ��Һ�м���������
��Һ�м���������![]()
D����Mg�ۼ���![]() ��Һ�У�
��Һ�У�![]()
11�����ⶨij��Һ��ֻ��NH4+��Cl-��H+��OH-�������ӣ�����˵����ȷ���ǣ�
A����Һ����������֮�䲻�������㣺c(Cl-)��c(H+)��c(NH4+)��c(OH-)
B������Һ�����ԣ���һ�����㣺c(Cl-)��c(NH4+)��c(H+)��c(OH-)
C������Һ�ʼ��ԣ���һ�����㣺c(NH4+)��c(Cl-)
D������Һ�����ԣ���һ�����㣺c(NH4+)��c(Cl-)
12��25��ʱ����ϡ��ˮ��μ��뵽ϡ�����У�����Һ��pH=7ʱ�����й�ϵ��ȷ����
A��c(NH4+)��c(SO42��)�������������������� B��2c(NH4+)��c(SO42��)
C��c(NH4+)��c(SO42��)������������������ D��c(OH��)+c(SO42��) = c(NH4+)+c(H+)
13.![]() ��һ�ܱ������У���ӦmM(��) ����nN(��)�ﵽƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��M��Ũ��Ϊԭ����80%,��
��һ�ܱ������У���ӦmM(��) ����nN(��)�ﵽƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��M��Ũ��Ϊԭ����80%,��
A��ƽ�������ƶ������������������� B������M��ת��������
C��n > m���� ����������������������D������N��������������
14�����з����п���˵��2HI(g)![]() H2(g)+I2(g)�Ѵﵽƽ����ǣ��ٵ�λʱ��������n mol H2��ͬʱ����n mol HI����һ��H�CH�����ѵ�ͬʱ������H�CI�����ѣ��۰ٷ���ɦ�(HI)=��(I2)���ܷ�Ӧ���ʦ�(H2)=��(I2)=1/2��(HI)ʱ���� c(HI):c(H2):c(I2)=2:1:1ʱ�����¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯�����¶Ⱥ����һ��ʱ��ijһ������Ũ�Ȳ��ٱ仯��������һ������������ƽ����Է����������ٱ仯�����¶Ⱥ����һ��ʱ������������ɫ���ٱ仯�����¶Ⱥ�ѹǿһ��ʱ�����������ܶȲ��ٱ仯��
H2(g)+I2(g)�Ѵﵽƽ����ǣ��ٵ�λʱ��������n mol H2��ͬʱ����n mol HI����һ��H�CH�����ѵ�ͬʱ������H�CI�����ѣ��۰ٷ���ɦ�(HI)=��(I2)���ܷ�Ӧ���ʦ�(H2)=��(I2)=1/2��(HI)ʱ���� c(HI):c(H2):c(I2)=2:1:1ʱ�����¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯�����¶Ⱥ����һ��ʱ��ijһ������Ũ�Ȳ��ٱ仯��������һ������������ƽ����Է����������ٱ仯�����¶Ⱥ����һ��ʱ������������ɫ���ٱ仯�����¶Ⱥ�ѹǿһ��ʱ�����������ܶȲ��ٱ仯��
A���ڢۢݡ�������B���٢ܢߡ��� C���ڢߢᡡ���������� ����D������
15������ͼ��ʾ�������ݻ���ͬ�������٢ڢ��н������·�Ӧ��3A(g)+B(g)![]() 2C(g)����H<0������ʼ�¶���ͬ���ֱ�������������ͨ��3molA��1mol B����ﵽƽ��ʱ��������C���ʵ���������ɴ�С��˳��Ϊ���� ��
2C(g)����H<0������ʼ�¶���ͬ���ֱ�������������ͨ��3molA��1mol B����ﵽƽ��ʱ��������C���ʵ���������ɴ�С��˳��Ϊ���� ��
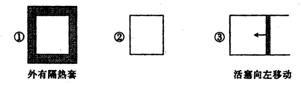
����A�� �ۢڢ١� B���ڢ٢ۡ� ������C���٢ڢ� �������� D���ۢ٢�
16.�ڳ�����100mLpH��10��KOH��Һ�У�����pH��4��һԪ��HA��Һ��pH�պõ���7����Է�Ӧ����Һ��������ȷ����
A��V�����Һ����200mL������������������������ B��V�����Һ����200mL
C��c��H������ c��OH����< c��K����< c��A���������� D��c��A������ c��K����
17.��һԪ��HA����Һ��һԪ��BOH����Һ�������ϣ���������Һ�����ԣ������й��ж���ȷ����
A�������ǰ�ᡢ��pH֮�͵���14,��HA�϶�������
B�������ǰ�ᡢ�����ʵ���Ũ����ͬ����HA�϶�������
C����Һ��ˮ�ĵ���̶ȣ������Һ>��ˮ>BOH��Һ
D�������Һ������Ũ��һ�����㣺c��B����> c��A����> c��H����> c��OH����
18��������Ӧ��ͼ��ͼ�������һһ��Ӧ�����ж��������˵����ȷ���ǣ�����
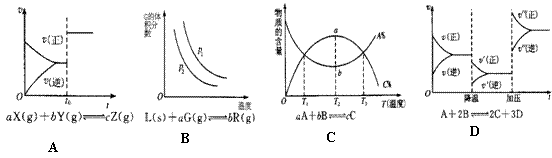
A���ܱ������з�Ӧ�ﵽƽ�⣬t0ʱ�ı�ijһ��������ͼ��ʾ����ı������һ���Ǽ������
B����Ӧ��ƽ��ʱ�����������ƽ��Ӱ���ϵ��ͼ��ʾ��������ӦΪ���ȷ�Ӧ����a��b
C�����ʵİٷֺ������¶ȹ�ϵ��ͼ��ʾ����÷�Ӧ������ӦΪ���ȷ�Ӧ
D����Ӧ���ʺͷ�Ӧ�����仯��ϵ��ͼ��ʾ����÷�Ӧ������ӦΪ���ȷ�Ӧ��A��B��C�����塢DΪ�����Һ��
�ڢ������ѡ���⣩
����ʵ�������������������С�⣬��12�֣�
19����6�֣�ʵ����Ϊ�ⶨһ�����ϡ�����ȷŨ�ȡ�ͨ���ô�����Na2CO3����ˮ����ɱ���Һ���еζ�����������ǣ���ȡW�˴�����ˮNa2CO3װ����ƿ�У�������������ˮ�ܽ⡣����ʽ�ζ����м����������ζ���
��1������CO2������Һ�л�Ӱ��pHֵ��Ϊȷ�ζ����յ���ѡ��pHֵ4��5֮�䣬��ô��ʯ����ȡ���̪����ָʾ����Ӧѡ�����������������������������ζ�����Һ��������������������������ɫ��Ϊ������������������ʱ������ʾ�����յ㡣
��2�����ﵽ�ζ��յ�ʱ���к�W��Na2CO3��������V����������������ʵ�����Ũ��Ϊ���������������������� mol/L��
��3��������ȡ��Na2CO3���������������Ũ�ȾͲ�ȷ�����������ȷŨ��ΪC1 mol/L���ò�����Na2CO3�궨���������Ũ��ΪC2 mol/L������������£�C1��C2�Ĺ�ϵ�ǣ��>����<����=������
�ٵ�Na2CO3�к���NaHCO3ʱ����C1���������������������� C2��
�ڵ�Na2CO3�к���NaOHʱ����C1��������������������C2��
20����6�֣����к�FeCl2���ʵ��Ȼ�ͭ���壨CuCl2��2H2O����Ϊ��ȡ������CuCl2��2H2O�����Ƚ����Ƴ�ˮ��Һ��Ȼ����ͼ��ʾ��������ᴿ��
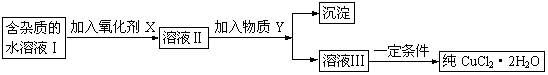
��֪H2O2��KMnO4��NaClO��K2Cr2O7������ǿ�����ԣ�Ҫ����Һ�е�Cu2����Fe2����Fe3������Ϊ�����������Һ��pH�ֱ�Ϊ6.4��6.4��3.7��
��ش��������⣺
��1����ʵ�����ʺϵ�������X��__________��
A��K2Cr2O7��������B��NaClO��������C��H2O2���������� D��KMnO4
��2������Y��������___________��
A��CuO���� ���� B��CuCl2�������� C��Cu��OH��2���������� D��CuCO3
��3����ȥFe3�����й����ӷ���ʽ�ǣ�����Y�ڣ�2����ѡ����ʵ�ѡ�����������
��4��������������Ŀ����________________________________________��
��5������ܲ���ֱ�������ᾧ�õ�CuCl2��2H2O��__________����ܡ����ܡ������粻�ܣ�Ӧ��β����������ܣ��˿ղ��________________________________��
�ġ�����⣨�����������С�⣬��40�֣�
21����12�֣���1����AlCl3��ҺΪԭ����ȡ��ˮAlCl3�����Ƶ�AlCl3��6H2O���壬��Ҫ���������������������������� ���ڸ����HCl�����м���AlCl3��6H2O���壬�ܽ�һ����ȡ��ˮAlCl3����ԭ���ǣ���ϻ�ѧ����ʽ��Ҫ˵���������������������������� ��
��2����������( H2O2)��һ����ɫճ��Һ��,����ˮ��Һ�׳�˫��ˮ,��������,ҽ�������������������H2O2��һ�ֶ�Ԫ����,��д�����ĵڶ������뷽��ʽ ���������������������� ,��H2O2��Һ�м������Ba(OH)2��Һ, ��Ӧ�Ļ�ѧ����ʽ________________________����
��3����֪ij��ɫ��Һ��ֻ���а���Na+��CH3COO-���ڵ��������ӣ���ش��������⣺
��������Һ��ֻ����һ�����ʣ������Һ������������ �ԡ���ص����ӷ���ʽΪ���������� ��
�� ��������Һ�����ԣ�����Һ�е�����Ϊ���������� ��
�� ������Һ�к����������ʣ�����Һ�ʼ��ԣ������Һ�в����ܳ��ֵ�����Ũ�ȴ�С��ϵ������������ ����ѡ������ĸ��
A��c��Na+��>c��CH3COO-����������B��c��CH3COO-��> c��Na+��
C��c��OH-��> c��Na+���� ������������D��c��Na+��> c��OH-��
E��c��OH-��>c��CH3COO-����������F�� c��CH3COO-��> c��OH-��
22.��8�֣���ĭ������dz��õ����������ṹ����Ͳ����Ͳ����ͲΪ����Ͳ����ͲΪ��Ͳ��ʹ�õ�ҩƷΪ��������Һ��̼��������Һ����ʢ��������Ͳ�С�ʹ��ʱ����������þͻ���������Ķ�����̼������������һ������ĭ����ʽ�����
��1����Ͳ��ʢ��ҩƷ�� �������� ��Ϊʲô����ʢ������Ͳ�У��������������� ��
��2��������ĭ��ԭ����ʲô���������ӷ���ʽ��ʾ�������������������������� ��
��3��������̼�����ƾ����������Һ������Ϊ�Ƿ������Ϊʲô��
���������������������������������������������������������������������� ��
��4��������̼������Һ����̼��������Һ������Ϊ�Ƿ������Ϊʲô��
�������������������������� ����������������������������������������������
23����12�֣������Ϊ 2L �Ĺ̶��ܱ�������ͨ�� 3molX ���� , ��һ���¶��·� �����·�Ӧ��2X (g) ![]() y (g) +3Z (g)
y (g) +3Z (g)
(1)�� 5min ��Ӧ�ﵽƽ�� , ��ʱ��������ڵ�ׯǿΪ��ʼʱ�� 1.2 �� , ���� Y ��ʾ������Ϊ���������� mol/L��min��
(2)��������Ӧ�ڼס��ҡ��������ĸ�ͬ�����ܱ������н��� , ��ͬһ��ʱ���ڲ�������ڵķ�Ӧ���ʷֱ�Ϊ : �ס� v (X) =3. 5 mol/L��min; �ҡ� v (Y) =2 mol/L��min; ���� v (Z) =4. 5 mol/L��min; ���� v (X) =0. 075 mol/L��s ��������������ͬ , �¶Ȳ�ͬ , ���¶��ɸߵ��͵�˳���� ( ����š�����������������������������������������������������
(3)����ﵽ (1) ��ƽ����ϵ�г��뵪�� , ��ƽ���������� ( ��"��"��"��"��"��)�ƶ��� ����ﵽ (1) ��ƽ����ϵ�����߲��ֻ������ , ��ƽ��������( �� " �� " �� " �� " �� " �� ") �ƶ���
(4)������ͬ��������ﵽ (1) ������ƽ����ϵ���ٳ��� 0.5molX ���� , ��ƽ��� X ��ת������(1) ��ƽ���е� X ��ת������Ƚ�
A����ȷ����B��ǰ��һ�����ں��ߡ�c��ǰ��һ�����ں��ߡ�D��ǰ��һ��С�ں���
(5)�������¶Ⱥ�ѹǿ���� , ��ʼʱ���� X �� Y �� Z ���ʵ����ֱ�Ϊ amol �� bmol �� cmol, �ﵽƽ��ʱ���� (1) ��ƽ���Ч , �� : a �� b �� C Ӧ������Ĺ�ϵΪ������������������������
(6)�������¶Ⱥ�������� , ��ʼʱ���� X �� Y �� Z ���ʵ����ֱ�Ϊ amol �� bmol �� cmol, �ﵽƽ��ʱ���� (1) ��ƽ���Ч , ����ʼʱά�ֻ�ѧ��Ӧ���淴Ӧ������� , �� C ��ȡֵ��ΧӦ�� Ϊ������������������������������������
24����8�֣���Ԫ�����ڱ��У����ڽ���Ԫ���ڽṹ������������������֮�����ڶ����ڵ�̼�������������������γ��⻯���Ԫ�ص��⻯���H2O�⣬����H2O2��̼Ԫ�ص��⻯���CH4�⣬����C2H6�ȣ���֮���Ƶĵ�Ԫ�ص��⻯���NH3�⣬����N2H4�ȡ�
(1)̼ԭ�Ӽ�����γ���״�ṹ����ԭ�Ӽ�Ҳ���γ���״�ṹ�����赪����ԭ�Ӽ�ֻ��N��N����N��H����ʽ���ӣ����γ��⻯����ϵ���⻯���ͨʽΪ���������������� ��
(2)��ϵ���е�NH3��ũҵ����ѧ������ҵ������Ҫ���塣��ϳ�ԭ���ǣ�
![]() N2(g)��3H2(g)��������2NH3(g)����H����92kJ/mol��
N2(g)��3H2(g)��������2NH3(g)����H����92kJ/mol��
����һ���¶��£���1molN2��4molH2����ͨ�뵽һ���̶��ݻ����ܱ������У�����Ӧ�ﵽƽ��ʱ�������ڵ�ѹǿΪ��ʼʱ��80������ʱ��Ӧ�ų�������Ϊ������������������ ��
�ڱ����¶Ȳ��䣬����ͬ�������У�����ʼʱ�����ʵ�����ΪamolN2��bmolH2��cmolNH3����ʹƽ��ʱNH3�����ʵ�������Ϊ25������
�� I���ﵽƽ��ʱ������ڷų����������������� ������ĸ��
A��һ����ȡ��������������� B��ǰ��һ��С�ں��ߡ�
C��ǰ�ߵ��ڻ�С�ں��ߡ����� D��ǰ�ߵ��ڻ���ں���
II�����÷�Ӧ������У���a��ȡֵ��Χ�������������� ��
�塢������ �������������С�⣬��14�֣�
25����9�֣��Ÿ�¯�����з����Ļ�����Ӧ֮һΪ��FeO(s)+CO(g)![]() Fe(s)+CO2(g)����H>0����ƽ�ⳣ���ɱ�ʾΪK=c(CO2)/c(CO)����֪1373KʱK=0.263��
Fe(s)+CO2(g)����H>0����ƽ�ⳣ���ɱ�ʾΪK=c(CO2)/c(CO)����֪1373KʱK=0.263��
���¶����ߣ���ѧƽ���ƶ���ƽ�ⳣ��Kֵ������ ������������١����䡱��
��1373Kʱ��ø�¯��c(CO2)=0.025mol/L��c(CO)=0.1mol/L������������£��÷�Ӧ�Ƿ��ڻ�ѧƽ��״̬���� ����ǡ�������ʱ����ѧ��Ӧ����v����������v���棩������ڡ��������ڡ���С�ڡ�������ԭ�������������������������������� ��
�Ƴ��̶������к����̲ݲ���ȫȼ�ղ�����һ����̼�����������ѪҺ�е�Ѫ�쵰�ף���Hb��ʾ�����ϣ�����������ӦCO(g)+Hb•O2(g)![]() O2(g)+Hb•CO(g)��ʵ�������Hb •��CO��Ũ�ȼ�ʹֻ��Hb•O2Ũ�ȵ�2%��������ʹ�˵����������Իش�
O2(g)+Hb•CO(g)��ʵ�������Hb •��CO��Ũ�ȼ�ʹֻ��Hb•O2Ũ�ȵ�2%��������ʹ�˵����������Իش�
��������Ӧ��ƽ�ⳣ������ʽΪ��K=���������� ��
����֪37��ʱ��ƽ�ⳣ��K=220�����̺������β��Ŀ����е�CO��O2��Ũ�ȷֱ�Ϊ1��10-6mol/L��1��10-2mol/L���ܷ�ʹ�˵������������������� ����ܡ����� ���������������������������������� ��
26. ��5�֣������£�FeS��Ksp=6.25��10-18(�豥����Һ���ܶ�Ϊ1g/mL)������֪H2S������Һ�ڳ����£�c��H+����c��S2-��֮��������¹�ϵ��c2��H+����c��S2-��=1.0��10-22���ڸ��¶��£�������FeSͶ��H2S������Һ�У���ʹ��Һ��c��Fe 2+���ﵽ1mol/L��Ӧ������Һ��pHΪ���٣�
�߶��꼶��ĩ���Ի�ѧģ������(��)
1��C 2��D 3��D 4��A 5��D 6��C 7��C 8��A
9��C 10��C 11��C 12��C 13��A 14��C 15��A 16��BD 17��A 18��CD
19����1�����ȡ��ơ��ȡ�������2��1000W/53��V
������3����ʾ����Na2CO3����2HCl
������������������ 106g������ 2mol
����������NaHCO3����HCl�������� ���� NaOH����HCl
����������84g������ 1mol��������������40g�� ��2mol
�������Ե�����ʱ��NaHCO3����HCl��������١�NaOH����Hcl�������ࡣ
�����پ�CHCl![]() ����֪��
����֪��![]() ����Խ�࣬CHClԽС��
����Խ�࣬CHClԽС��
�����ʢ�C1 < C2������������C1 > C2
20.��1��C�� ��2��B������3��Fe3++3H2O![]() Fe(OH)3+3H+�� CuO+2H+=Cu2++H2O
Fe(OH)3+3H+�� CuO+2H+=Cu2++H2O
�� ��4����Fe3+������Fe2+���������ɳ�������Cu2+����
�� ��5�����ܡ���Ӧ��HCl����������
21. (1)����Ũ������ȴ�ᾧ�����ˣ�Al3+ + 3H2O![]() Al(OH)3 + 3H+���ڸ����HCl�����У�������AlCl3��ˮ�⣬�Ҵ���AlCl3��6H2O�������Ȳ�����ˮ���������ܵõ���ˮAlCl3��
Al(OH)3 + 3H+���ڸ����HCl�����У�������AlCl3��ˮ�⣬�Ҵ���AlCl3��6H2O�������Ȳ�����ˮ���������ܵõ���ˮAlCl3��![]()
![]() ��3���٣�1�����ԡ�������CH3COO-+H2O��������CH3COOH+OH-
��3���٣�1�����ԡ�������CH3COO-+H2O��������CH3COOH+OH-
�� ��CH3COOH��CH3COONa���� ��B��C
22����1����������Һ���� ������ˮ����Һ�����Իḯʴ��Ͳ�����Բ���ʢ���ڸ�Ͳ��
��2��Al3++3HCO3-=Al(OH)3��+3CO2��
��3���������� ����̼��������ˮ���ܽ�Ȳ���ˮ��ʱ������Al(OH)3�Ḳ���ھ�����棬ʹ��Ӧֹͣ
��4���������� ��̼��������ȣ�������ͬ����CO2��̼���ƺ�����Ҳ���CO2����������������һ���������£���̼������Һ����̼��������Һ��ʹ������CO2���٣��������������ĭ
23��(1)0��03 (2). �����ң��ף���(3)������ (4)D�� (5) C=3b��a��0(6)0.9��a��4.5
24����8�֣�(1)NmHm+2��mΪ�������� (2) �� 46kJ����I��D��II��0.5��a��1
25���Ţ����� �ڷ��ڣ���ʱc(CO2)/c(CO)=0.25<k����Ӧ���ҽ���
�Ƣ�c(O2)• c(Hb• CO)/C(CO)• c(Hb• O2)��������c(Hb• CO)/ c(Hb• O2)=2.2%��2%��
26��2.4