高二化学学业水平测试模拟试题(1)
可能用到的原子量:H :1 O:16 S:32 Cu:64 Na:23 C:12 N: 14 Ca:40
K:39 Li:7 Na:23 I: 127 Mg:24 Al:27,Cr:52 Ag:108 Cl:35.5
第I卷(选择题,共69分)
一、选择题(本题共23小题,每题只有1个正确答案,每小题3分,共69分)
1.为了使天空更蓝,空气更清新,目前江苏的各城市对没有申领到“绿色”通行证的高污染车实行限行。高污染车排出的尾气中所含的污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有
A、 二氧化碳 B、氮氧化物
C、 水蒸汽 D、 氮气
2、![]() 、
、![]() 、
、![]() 、H+、H2是
、H+、H2是
A、氢的五种同位素 B、五种氢元素
C、氢的五种同素异形体 D、氢元素的五种不同粒子
3.地 壳 中 化 学 元 素 含 量 前 四 位 排 序 正 确 的是:
A .氧、硅、铁、铝, B. 铁、氧、铝、镁,
C. 氧、硅、铝、铁, D .硅、氧、铝、铁,
4.下列玻璃仪器:①烧杯 ②烧瓶 ③试管 ④容量瓶 ⑤量筒。能直接加热的是:
A.①③ B. ②③ C. ③ D. ④⑤
5.下列叙述中正确的是
A.摩尔是物质的质量的单位
B.碳的摩尔质量为12g
C.阿伏加德罗常数约为6.02×1023mol-1
D.一个碳原子的质量为12g
6.![]() 剧毒,致死量为0.3g,万一不慎误服,应大量吞服鸡蛋清及适量解毒剂,此解毒剂应是( )。
剧毒,致死量为0.3g,万一不慎误服,应大量吞服鸡蛋清及适量解毒剂,此解毒剂应是( )。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
7.下列物质中含有自由移动的Cl-是
A.KClO3溶液 B.KCl溶液
C.液态HCl D.NaCl固体
8.澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”, 他外形类似海绵,比重极小,并具有磁性。纳米泡沫碳与金刚石的关系是
A.同系物 B.同分异构体 C.同位素 D.同素异形体
9.下列物质转化需要加入还原剂才能实现的是
A.SO32-→SO2 B.HCl→Cl2
C.Na→Na+ D.SO2→S
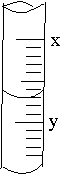 10. 右图是
10ml 量筒的一部分,数字XY之间相差 1ml
10. 右图是
10ml 量筒的一部分,数字XY之间相差 1ml
若 X=5,则量筒所盛液体的体积是
A. 5.7 ml B. 4.4 ml C. 4.3 ml D. 6.3 ml
11.下列离子方程式书写正确的是
A.钠和冷水反应 Na+2H2O=Na++2OH-+H2↑
B.铁粉投入到硫酸铜溶液中:Fe +Cu2+=Fe2+ +Cu
C.AlCl3溶液中加入足量的氨水:Al3++ 3OH- = Al(OH)3↓
D.澄清石 灰 水 跟 稀 硝 酸 反 应: Ca(OH)2+2H+=Ca2++2H2O
12.下列离子在溶液中能大量共存的是
A.Ba2+、SO42- 、K+、 OH- B.![]()
C.Al3+、HCO3- 、K+、 OH- D.![]()
13.下列对硫酸的叙述正确的是
A.因浓硫酸具有强氧化性,故不可用它来干燥氢气
B.浓硫酸不活泼,可用铁铝容器存放
C.浓硫酸有强氧化性,稀硫酸不具有氧化性
D.浓硫酸具有腐蚀性,取用时要小心
14.下列操作不能用于检验![]() 的是
的是
A.气体使湿润的酚酞试纸变红
B.气体能使湿润的红色石蕊试纸变蓝
C.气体与浓H2SO4靠近
D.气体与浓盐酸产生白烟
15、1820年德贝莱纳用MnO2催化KClO3分解制氧,发现制得氧气有异常的气味,使该气体通过KI淀粉溶液,溶液变蓝。则该氧气中可能混有
A.Cl2 B.Br2 C.HCl D.CO2
16.下列装置能够组成原电池的是
![]()
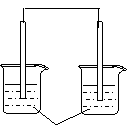

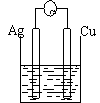

稀硫酸 AgNO3(aq) 蔗糖 稀硫酸
A B C D
17、可以用分液漏斗进行分离的混合物是
A、酒精和碘水 B、苯和水
C、乙酸和乙酸乙酯 D、乙酸和水
18、下述关于烃的说法中,正确的是
A.烃是指仅含有碳和氢两种元素的有机物
B.烃是指分子里含碳元素的化合物
C.烃是指燃烧反应后生成二氧化碳和水的有机物
D.烃是指含有碳和氢元素的化合物
19、除去乙烷中乙烯的办法是
A.点燃 B.通过溴水 C.通过浓硫酸 D.通过石灰水
20.下列关于食品添加剂的说法不正确的是( )
A.亚硝酸钠可以致癌 B.我们应该禁止使用防腐剂
C.苯甲酸钠可以作雪碧饮料的防腐剂
D.绝大多数食品添加剂在过量使用时对人体有害的
21.下列关于药物的使用说法正确的是( )
A.虽然药物能治病,但大部份药物有毒副作用
B.使用青霉素时,不用进行试验直接静脉注射
C.长期大量使用阿司匹林可预防疾病,没有副作用
D.我们生病了都可以到药店自己买药吃,不用到医院
22.阿司匹林又名乙酰水杨酸,推断它不应具有的性质( )
A.与NaOH溶液反应 B.与金属钠反应
C.与乙酸发生酯化反应 D.与乙醇发生酯化反应
23.变质的油脂有难闻的哈喇味,这是因为发生了( )。
A.氧化反应 B.加成反应 C.取代反应 D.水解反应
班级 学号 姓名 得分
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | ||||||||||||
| 题号 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | |
| 答案 |
第Ⅱ卷(非选择题,共31分)
二、填空题(本大题包括3小题,共20分)
24.(3分)在新疆与青海两省交界处有一狭长山谷,当地牧民经常遇到在风和日丽的晴天顷刻间电闪雷鸣,狂风大作,人畜皆遭雷击而倒毙。奇怪的是这里牧草茂盛,四季长青。被当地牧民称为“魔鬼谷”。请用化学方程式表示“魔鬼谷” 牧草茂盛,四季长青的原因:
(1)___
(2)
(3)
25、( 8分)下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
|
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
![]() ⑴在这些元素中,化学性质最不活泼的原子的原子结构示意图为
⑴在这些元素中,化学性质最不活泼的原子的原子结构示意图为
![]() ⑵地壳中含量最多的金属元素是
⑵地壳中含量最多的金属元素是
⑶用电子式表示②与④形成化合物的过程 。
⑷这些元素中的最高价氧化物对应的水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 。
⑸写出⑤与氢氧化钠反应的化学方程式: 。
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式: 。
26. (9分)
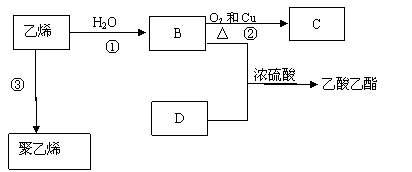 |
(1)乙烯的结构式为: 。
(2)写出化合物官能团的化学式及名称:
B中含官能团名称 ;D中含官能团名称 ;
(3)写出反应的化学方程式
①: 反应类型:
②: 反应类型:
③: 反应类型:
三、(本题包括2小题,共11分)
27.(5分)糖尿病是“富贵病”,请你设计实验检验病人尿液中的葡萄糖,并与正常人作对比,设计要求:
⑴(2分)写出实验所用化学药品
⑵(3分)写出实验现象并作出结论。
28.(6分)在25℃时,向100 mL含氯化氢14.6 g的盐酸溶液里放入5.60 g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min末,收集到1.12 L(标准状况)氢气。在此之后,又经过4 min,铁粉完全溶解。则:
(1)在前2 min内用FeCl2表示的平均反应速率是 。
(2)在后4 min内用HCl表示的平均反应速率是 。
(3) 前2 min与后4 min相比,反应速率较快的是 ,其原因是 。
参考答案:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | B | D | C | C | C | D | B | D | D | C | B | B |
| 题号 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | |
| 答案 | D | C | A | B | B | A | C | B | A | C | A |
24. N2 + O2 ==== NO 2NO+ O2 ====NO2
3NO2 + H2O ==== 2HNO3 + NO
25、(共8分,每空1分,)
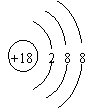 (1)Ar
(1)Ar
![]() (2)Al (3)
(2)Al (3)
(4)HClO4 KOH Al(OH)3
(5)2Al + 2NaOH + 2H2O =2 NaAlO2+ 3H2↑
Al (OH)3+ OH- = AlO2-+ 2H2O
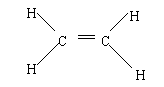 26、(1)
26、(1)
(1分)
(2)羟基;羧基
(3)
①CH2=CH2 + H2O![]() CH3CH2OH
(加成反应)
CH3CH2OH
(加成反应)
②2CH3CH2OH + O2![]() 2CH3CHO + 2H2O (氧化反应)
2CH3CHO + 2H2O (氧化反应)
![]() ③nCH2=CH2
③nCH2=CH2 ![]() (聚合反应)
(聚合反应)
27.⑴(3分)10%NaOH溶液、CuSO4溶液和两种尿液样品。(用其他合理药品也可以)
⑵(3分)加热时出现砖红色沉淀,正常人尿液无现象,证明糖尿病人尿液中含有葡萄糖。
28.(1)0.25 mol・L-1・min-1 (2)0.25 mol・L-1・min-1
(3)前2 min ;随着反应的进行,反应物浓度减小,反应速率减慢
 族
族