高二化学学业水平测试模拟试题(3)
2007-2-16
可能用到的原子量:H :1 O:16 S:32 Cu:64 Na:23 C:12 N: 14 Ca:40
K:39 Li:7 Na:23 I: 127 Mg:24 Al:27,Cr:52 Ag:108 Cl:35.5
第I卷(选择题,共69分)
一、选择题(本题共23小题,每题只有1个正确答案,每小题3分,共69分)
1、.我国的“神舟五号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的![]() ,每百吨
,每百吨![]() 核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以![]() 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是
A.![]() 原子核内含有4个质子
原子核内含有4个质子
B.![]() 和
和![]() 互为同位素
互为同位素
C.![]() 原子核内含有3个中子
原子核内含有3个中子
D.![]() 的最外层电子数为2,所以
的最外层电子数为2,所以![]() 具有较强的金属性
具有较强的金属性
2.蛋白质在胃蛋白酶和胰蛋白酶的作用下变成氨基酸的反应属于( )。
(A)消去反应 (B)聚合反应 (C)水解反应 (D)酯化反应
3、环境污染已成为人类社会面临的重大威胁,各种污染数不胜数。下列名词与环境污染无关的是
①白色垃圾;②潮汐;③酸雨;④光化学烟雾;⑤臭氧空洞;⑥可吸入颗粒物
⑦赤潮;⑧绿色化学
A.①⑦ B.②⑤ C.②⑧ D.⑦⑧
4.按照HCl、( )、Ca(ClO)2、Cl2O5、HClO4的排列规律,选出一种适当的物质填入括号
A.NaCl B.NaClO C.Cl2O7 D.Cl2
5.已知下列溶液的溶质都是强电解质,这些溶液中的Cl-浓度与
50mL 1mol・L-1 MgCl2溶液中的Cl-浓度相等的是
A.150 mL 1 mol・L-1 NaCl溶液
B.75 mL 2 mol・L-1 CaCl2溶液
C.150 mL 2 mol・L-1 KCl溶液
D.75 mL 1 mol ・L-1 AlCl3溶液
6.NO2被水吸收的过程中,发生了氧化还原反应3NO2+H2O=2HNO3+NO,其中被氧化的N原子和被还原的N原子,其物质的量之比是
A.3:1 B.1:3 C.1:2 D.2:1
7. 市场上有一种加酶洗衣粉,它是在洗衣粉中加入少量的碱与蛋白酶制成的。蛋白酶的催化活性很强,衣物的汗渍、血迹及人体排放的蛋白质、油渍遇到它,都能水解而除去。下列衣料中,不能用加酶洗衣粉洗涤的是
①棉织品 ②毛织品 ③腈纶织品 ④丝织品
A.① B.②③ C.①③ D.②④
8.若在试管中加入2-3mL液体再加热,正确的操作顺序是 ( )
①点燃酒精灯进行加热; ②在试管中加入2-3mL液体;
③用试管夹夹持在试管的中上部; ④将试剂瓶的瓶盖盖好,放在原处。
A.②③④① B.③②④① C.②④③① D.③②①④
9.很多化学物质名称中含有“水”,“水”通常有三种含义:①表示水这种物质;②表示水溶液;③表示物质处于液态。下列物质名称中的“水”不属于以上三种含义的是 ( )
A.水晶 B.水银 C.溴水 D.重水
10.下列反应的离子方程式书写正确的是
A.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu
B.稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑
C.氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓
D.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
11、下列关于氯气的叙述中,不正确的是
A.氯气是一种黄绿色、有刺激性气味的气体
B.氯气、液氯和氯水是同一种物质
C.氯气能溶于水
D.氯气是一种有毒的气体
12.铝制品不宜长期盛放酸性食品和碱性食品是因为铝制品表层属于( )
A.金属铝 B.碱性氧化物 C.酸性氧化物 D.两性氧化物
13.据统计,世界上的古建筑在20世纪所遭受的腐蚀比过去几百年甚至几千年所遭受的腐蚀还要严重,这是因为( )
A.古建筑的腐蚀是可逆过程,在前几百年甚至几千年前处于化学平衡状态,而近几十年来腐蚀向正反应方向移动
B.由于近几十年来大量使用矿石燃料,造成酸雨,加速了古建筑的腐蚀
C.由于近几十年来参观的人数急剧增多,加速了古建筑的磨损
D.由于近几十年来温室效应加剧,加速了古建筑的风化
14.酸雨形成的主要原因是( )
A.汽车排出大量尾气 B.自然界中硫化物分解
C.工业上大量燃烧含硫燃料 D.可燃冰燃烧.
15.我国三峡工程所提供的清洁.廉价.大功率可再生的水电,相当于每年燃烧3×107吨原煤的火力发电厂产生的电能。因此三峡工程有助于控制( )
A.温室效应 B.氮的氧化物的排放
C.白色污染 D.碳氢化合物的排放
16、下列属于氮的固定的是
A、植物从土壤中吸收氮肥
B、大豆的根瘤菌将含氮的化合物转变为植物蛋白质
C、将空气中的氮气转变为氮的化合物
D、硝酸和氨气反应生成氮肥
17、下列各对物质中,互为同系物的是
A.CH4、C2H4 B.CH4、C2H5OH
C.C2H6、C3H8 D.CH3COOH、C3H8
18、下列有关甲烷性质的叙述,正确的是
A、甲烷是一种无色,有臭味的气体 B、甲烷易溶于水
C、甲烷与氯气发生的化学反应类型属于取代反应 D、甲烷是一种混合物
19、下列物质中,属于合成高分子化合物的是
A.纤维素 B.蛋白质 C.酶 D.塑料
20.用石灰水保存鲜蛋是一种化学保鲜法。石灰水能保存鲜蛋的原理是( )。
①石灰具有强碱性,杀菌能力强;
②![]() 能与鲜蛋呼出的
能与鲜蛋呼出的![]() 反应,生成碳酸钙薄膜,起保护作用;
反应,生成碳酸钙薄膜,起保护作用;
③石灰水是电解质溶液,能使蛋白质凝聚;
④石灰水能渗入蛋内中和酸性物质。
A.①② B.③④ C.②④ D.①③
21. 火星探测器发回的信息表明,火星上存在针铁矿[Goethite,化学式:FeO(OH)]和黄钾铁矾[Jarosite],从而证明火星表面曾经存在过水。这一发现被《人民日报》评为2004世界十大新闻之首。已知两种矿物中铁的价态相同,则黄钾铁矾{化学式记为:KFe3(SO4)2(OH)n}中n值为:( )
A.4 B.5 C.6 D.7
22.下面不是污水处理方法的是:
A.过滤法 B.混凝法 C.中和法 D. 沉淀法
23.“白色污染”的主要危害是:
①破坏土壤结构 ②降低土壤肥效 ③污染地下水 ④危及海洋生物的生存
A.①② B.②③ C. ①②③④ D. ②④
班级 学号 姓名 得分
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | ||||||||||||
| 题号 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | |
| 答案 |
第Ⅱ卷(非选择题,共31分)
二、填空题(本大题包括5小题,共27分)
24. (2分)干电池是一种的 装置。干电池外围的锌皮是电池的 极,发生 反应;中间的碳棒是______极,该极发生______反应。
25. (4 分)分别除去下列混合物中的杂质。在空白处写出所选试剂。和化学方程式。
⑴MgCl2 混有少量MgCO3 。
⑵SiO2混有少量CaO 。
⑶FeCl2混有少量CuCl2 。
⑷铜粉中混有少量铁粉 。
26、(3分)某药品标签上贴有OTC,它表示 ,若是R标记则表示 ,我们平时能自己到药店买到的药如阿司匹林属于哪类药
27.(8分)把某黑色固体A加热至红热,投入到一种无色溶液B中,产生由两种气体组成的混合气体X,将X作如下图所示实验:
 白色沉淀
白色沉淀
无色气体C
无色气体E
蓝色溶液G
无色溶液D
无色气体E
由此可判断:A的名称是_________,B的名称是________;C是_______、
D是_________、R是________、E是________、G是________、X是________。
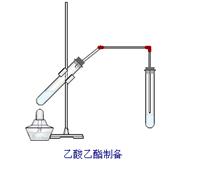 28.(10分)如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2 mL乙酸,充分摇匀。在右试管中加入5mL饱和Na2CO3溶液。按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
(1)写出左试管中主要反应的方程式:
;
(2)加入浓硫酸的作用:_______________________________________________;
28.(10分)如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2 mL乙酸,充分摇匀。在右试管中加入5mL饱和Na2CO3溶液。按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
(1)写出左试管中主要反应的方程式:
;
(2)加入浓硫酸的作用:_______________________________________________;
(3)饱和Na2CO3的作用是: _____________________________________________;
(4)反应开始时用酒精灯对左试管小火加热的原因是:
_________________________ ______;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)后改用大火加热的目的是 。
(5)分离右试管中所得乙酸乙酯和Na2CO3溶液的操作为(只填名称) ,所需主要仪器为 。
(6)实验生成的乙酸乙酯,其密度比水 ,有 气味。
三、计算题
29.(4分)取一定量的Na2CO3和Na2SO4混合物溶液与过量盐酸反应,生成2.016 L CO2(标准状况),然后加入足量的Ba(OH)2溶液,得到沉淀的质量为2.33 g。试计算混合物中Na2CO3和Na2SO4的物质的量分别为多少。
参考答案:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | B | C | C | B | C | D | D | C | A | A | B | D |
| 题号 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | |
| 答案 | B | C | A | C | D | C | D | A | C | A | C |
24.将化学能转化成电能的装置 ;负,氧化;正,还原。
25. ⑴盐酸 MgCO3 + 2HCl = MgCl2 + CO2↑ + H2O
⑵盐酸 CaO + 2HCl = CaCl2 + H2O
⑶铁粉 CuCl2 + Fe = FeCl2+ Cu
⑷盐酸 Fe+2HCl=FeCl2+H2↑
26、非处方药,处方药,OTC
27. 木炭,浓硝酸;CO2和NO、稀HNO3、Cu、NO、Cu(NO3)2、CO2和NO2
28.(1)
![]()
(2)催化剂、吸水剂。(3)中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度。
(4)加快反应速率,同时又防止了反应物未来得及反应而挥发损失;蒸出生成的乙酸乙酯,使可逆反应向右进行。
(5)分液;分液漏斗。
(6)小;芳香。
29 0.9mol 0.01mol