高二化学学业水平测试模拟试题(4)
可能用到的原子量:H :1 O:16 S:32 Cu:64 Na:23 C:12 N: 14 Ca:40
K:39 Li:7 Na:23 I: 127 Mg:24 Al:27,Cr:52 Ag:108 Cl:35.5
第I卷(选择题,共69分)
一、选择题(本题共23小题,每题只有1个正确答案,每小题3分,共69分)
1.“西气东输”是西部大开发的重大工程,“西气”指的是
A.石油气 B.天然气 C.水煤气 D.煤气
2. .下列不是室内污染物的是:
A.CO B.甲苯 C.尼古丁 D. 食品袋
3. 常温下可用铝制容器盛放的是:
A.浓盐酸 B.稀硝酸 C.浓硝酸 D.食用醋
4.以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是
 | |||||||
 |  | ||||||
 | |||||||
A B C D
![]() 5、下列表达方式错误的是
5、下列表达方式错误的是
A、氯化氢分子的电子式: H+ [: :]- B、S2-的结构示意图:
C、O―18的原子符号:![]() D、CO2分子的结构式:O=C=O
D、CO2分子的结构式:O=C=O
6.长期吸食或注射毒品会危及人体健康,下列各组中都属于毒品的是
A.冰毒、黄连素 B.海洛因、黄连素
C.大麻、摇头丸 D.黄曲霉素、尼古丁
7.青霉素是下面哪位科学家发现的
A、钱恩 B、弗莱明 C、诺贝尔 D、柯尔贝
8.天然皮革是( )
(A)纤维素制品 (B)酯类制品 (C)合成高分子制品 (D)变性的蛋白质
9、钙是人体必需的常量元素,成年人每天需要800毫克的钙,下列补钙的途径不正确的是
A、经常晒太阳 B、经常饮用钙离子含量高的硬水
C、经常饮用牛奶、豆奶 D、大量补充维生素D
10.有人分析一些小而可溶的有机分子的样品,发现它们含有碳.氢.氧.氮等元素,这些样品很可能是( )。
A.脂肪酸 B.氨基酸 C.②③葡萄糖 D.核糖
11. 测定下列溶液的pH测定结果错误的是:
A.柑橘汁pH: 3~4 B.食盐溶液pH= 7
C.氯化铝溶液pH= 4 D.纯碱溶液 pH =7
12. 在一个2升的容器中盛入2.0 mol某气态反应物,2 s后该气态物还剩余1 .6 mol。2 s内它的反应速率为:
A.0.1 mol/(L・s) B.0.2 mol /(L・s) C.0.3 mol /(L・s) D.0.4 mol /(L・s)
13.关于硝酸叙述正确的是:
A.硝酸不稳定,见光或受热就会分解
B.稀硝酸是弱酸,浓硝酸是强酸
C.铜与稀硝酸反应生成二氧化氮
D.稀硝酸是弱氧化剂,浓硝酸是强氧化剂
14.下列反应达到平衡后,增大压强或升高温度,平衡都向正反应方向移动的是:
A.2NO2 ![]() N2O4
(正反应为放热反应)
N2O4
(正反应为放热反应)
B.3O2![]() 2 O 3
(正反应为吸热反应)
2 O 3
(正反应为吸热反应)
C.H2(g)+I2(g)![]() 2HI(g)
(正反应为放热反应)
2HI(g)
(正反应为放热反应)
D.NH4HCO3(s) ![]() NH3 +
H2O +CO2 (正反应为吸热反应)
NH3 +
H2O +CO2 (正反应为吸热反应)
15. 下列说法错误的是:
A.酸雨的pH小于5.6 B.医用酒精的体积分数是75%
C.煤和天燃气都是纯净物 D.汽油是C5~C11的烃的混合物
16、下列物质中加入金属钠不产生氢气的是
A.乙醇 B.乙酸
C.水 D.苯
17、下列海洋资源中属于可再生资源的是( )
A、 海底石油、天然气 B、潮汐能
C、 滨海砂矿 D、锰结核
18、下列物质不互为同分异构体的是
A. 葡萄糖和果糖 B.蔗糖和麦芽糖
C.正丁烷和异丁烷 D.淀粉和纤维素
19. 钢铁发生吸氧腐蚀时,正极上发生的电极反应是:
A.2H+ + 2e- === H2↑ B.Fe2+ + 2e- == Fe
C.2H2O + O2 + 4e- === 4OH- D. Fe3+ + e- === Fe2+
20.以下微粒通常只具有氧化性的是
A. Fe B. Fe2+ C. Fe3+ D. H2
21.制造焊锡时,把铅加入锡的重要原因是:
A.增加强度 B.降低熔点 C.增加硬度 D. 增强抗腐蚀能力
22.既能与强酸又能与强碱反应的一组物质是
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3
A.只有① B.只有② C.只有③ D.①、②、③、④均可
23.鉴别两种食盐水和蔗糖水的方法有( )
①在两种溶液中分别加入少量稀硫酸,加热,再加入碱中和硫酸,再加入银氨溶液,微热;②测量溶液的导电性;③将溶液与溴水混合.振荡;④用舌头尝味道。
其中在实验室进行鉴别的正确方法是
A.①② B.①③ C.②③ D.③④
班级 学号 姓名 得分
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | ||||||||||||
| 题号 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | |
| 答案 |
第Ⅱ卷(非选择题,共31分)
二、填空题(本大题包括4小题,共20分)
24.(3分)化学式为C8Hm的烷烃,m值等于 ;CnH22的烷烃,n值等于 ;相对分子质量为212的烷烃的分子式为 。
25.(8分)某地有一池塘,生长着丰富的水生植物和多种鱼、虾。后来,由于化工厂将大量污水排入池塘中,使水质恶化,各种水生生物先后死亡。根据题意回答下列问题:
(1) 从生态平衡角度看,池塘的这种变化说明了
。
(2)造成这种变化的原因是 。
(3)经检测,污水中含有0.012 mol / L的游离溴,可用亚硫酸钠除去污水中的溴,请写出其化学方程式: 。
(4)处理5 L这种污水,需加入0.05mol / L的亚硫酸钠溶液 升才能将溴全部除去。
(5)要使池塘恢复本来面目,首先要解决的问题是 ,
首先要恢复的生物是 。
26、(5分)某同学欲检验抗酸药中是否含有Al(OH)3,操作如下.取药剂3-4片研碎,向样品中加入过量的盐酸,过滤,得澄清溶液,向澄清溶液中滴加NaOH溶液,观察到有白色沉淀,继续加过量NaOH溶液,白色沉淀又溶解.你能得出该抗酸药中是否含有Al(OH)3 (填含或不含),请写出有关反应的化学方程式:
①
②
③
27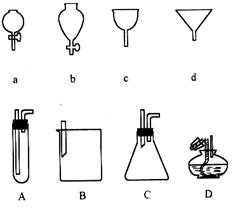 .(8分)如右图所示a、b、c、d分别是几种
.(8分)如右图所示a、b、c、d分别是几种
常见漏斗的上部,A、B、C、D是实际操作中各漏
斗的下部插入容器中的示意图,请指出A、B、C、
D分别与a、b、c、d相匹配的组合及其组合后装置
在实验中的应用,例如:C和a组合,用于制取气
体。
① A与 组合,用于 ,② B与 组合,用于 ,
③ B与 组合,用于 ,④ D与 组合,用于 ,
三、计算题
28.(7分)某抗酸药每片含碳酸钙534mg,氢氧化镁180mg,每片该药可中和多少克溶质质量分数为6 .2%的盐酸?
参考答案:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | B | D | C | D | A | C | B | D | B | B | D | A |
| 题号 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | |
| 答案 | A | B | C | C | B | D | C | C | B | D | A |
24.18 10 C15H32
25.(1)池塘的生态平衡遭到破坏 (2 )化工厂对池塘的污染超过了池塘的自动调节能力 (3)Na2SO3 + Br2 + H2O === Na2SO4 + 2 HBr
(4) 1.2 L (5)化工厂的污染问题;水生植物
26、含有,
①Al(OH)3 + 3HCl === AlCl3 + 3H2O
②AlCl3 + 3NaOH === Al(OH)3 + 3NaCl
③Al(OH)3 + NaOH ===NaAlO2 + 2H2O
27.① c,制备气体 ② b,分液 ③ d,过滤 ④ d 向酒精灯添加酒精(每小题2分)
28.10克