高二化学上学期第二章检测试卷
制卷人:杨学光
可能用到的相对原子质量:H:1 Na:23 Mg:24 Al:27 Fe:56 K:39 Cu:64 Ag:108 C:12 O:16 S:32 Cl:35.5 Br:80
| 得 分 | 评卷人 |
一、选择题(本题包括29小题,每小题2分,共58分,每小题有一个或两个正确答案)
1、反应4A(g)+3B(g)
![]() 2C(g)+D(g),经2 min, B的浓度减少了0.6 mol/L.此反应速率的表示正确的是( )
2C(g)+D(g),经2 min, B的浓度减少了0.6 mol/L.此反应速率的表示正确的是( )
A、用A表示的反应速率是0. 4 mol/(L・min)
B、用C表示的速率是0.2 mol/(L・min)
C、在2 min末的反应速率,用B表示是0. 3 mol/(L・mi
D、在2 min内用B和C表示的反应速率的值都是逐渐减小的
2、aX(g) +bY(g)![]() cZ(g)
+dW(g)在一定容积的密闭容器中反应5 min,测得X减少n mol/L,Y 减少了 n/3 mol/L,Z增加2n/3mol/L。并侧得反应前后容器内压强保持不变.则该反应的化学方程式正确的是( )
cZ(g)
+dW(g)在一定容积的密闭容器中反应5 min,测得X减少n mol/L,Y 减少了 n/3 mol/L,Z增加2n/3mol/L。并侧得反应前后容器内压强保持不变.则该反应的化学方程式正确的是( )
A、3X(g)+Y(g)![]() 2Z(g)+W(g)
2Z(g)+W(g)
B.、X(g)+3y(g) ![]() 2Z(g)+2W(g)
2Z(g)+2W(g)
C、 X(g)+3Y(g)![]() Z(g)十W(g)
Z(g)十W(g)
D.、3X(g)+Y(g) ![]() 2Z(g)+2W(g)
2Z(g)+2W(g)
3、在密闭容器中进行可逆反应,A与B反应生成C.其反应速率分别用V(A),V(B),V(C) mol/(L・min)表示,且V(A),V(B),V(C)之间有如下所示的关系v(B)=3v(A);3v(C)=2V(B):则此反应可表示为( )
A、2A+3B![]() 2C
B、A+3B
2C
B、A+3B![]() 2C
2C
C、3A+B![]() 2C
D.、A+B
2C
D.、A+B![]() C
C
4、可逆反应A(g)+2B(g)![]() C(g)+D(g),在四种不同情况下的反应速率如下.其中反应进行得最快的是( )
C(g)+D(g),在四种不同情况下的反应速率如下.其中反应进行得最快的是( )
A、v(A)=0. 15 mol/(L・min) B、v(B)=0.6 mol/(L・min)
C、v(C)=0. 4 mol/(L・min) D、v(C)=0. 02mol/(L・min)
5、在四个不同的容器中.在不同的条件下进行合成氨反应,根据在相同时间内测定的结果判断,生成氨的速率最快的是( )
A、v(H2)=0. l mol/(L・min) B、v(N2)=0. 2 mol/(L・min)
C、v(NH3)=0. l5 mol/(L・min) D、v(H2)=0. 3mol/(L・min)
6、反应4A(g) +5B(g)![]() 4C(g)+6D(g)在5L的密闭容器中进行,半分钟后,C的物质的量增加了0. 3mol。下列论述正确的是( )
4C(g)+6D(g)在5L的密闭容器中进行,半分钟后,C的物质的量增加了0. 3mol。下列论述正确的是( )
A.、A的平均反应速率是0.010 mol/(L・min)
B、容器中含D的物质的量至少为0. 45 mol
C、容器中A.B,C,D的物质的量比一定是4:5:4:6
D、容器中A的物质的量一定增加了0.30mol
7、下列四种X溶液.分别放人盛有10 ml: 2 mol/ L
HCI烧杯中,加水稀释至50 mL. X和HCI进行反应.其中反应速率最大的是( )
A.、20 mL 3 mol/ L X溶液 B、20 mL 2 mol/L.X溶液
C.、10 mL 4 mol/L X溶液 D.、10 ml.. 2 mol/L X溶液
8、对于反应N2+O2![]() 2NO,在密闭容器中进行.下列条件能加快反应速率的是( )
2NO,在密闭容器中进行.下列条件能加快反应速率的是( )
A、缩小体积使压强增大
B、体积不变充人N2,使压强增大
C、体积不变充人He,使气体压强增大
D、压强不变,充人气体Ne
9、反应3Fe(s)+4H2(g)![]() Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A、增加Fe的量 B、将容器体积缩小一半
C、保持体积不变充人N2使体系压强增大 D、压强不变充入N2使容器体积增大
10、20℃时.将0. 1 mol/L 的Na2S2O3溶液10 mL和0.1 mol/LH2SO4溶液10 mL混合,两分钟后溶液出现明显浑浊(发生的反应为:Na2S2O3+H2SO4==Na2SO4+S↓+SO2↑+H2O)。已知温度每升高10℃.该反应的化学反应速率增大到原来的2倍.那么50℃时,同样的反应要明显地出现浑蚀,所需时间是( )
A.、40 s B.、15 s C、48 s D.、20 s
11、工业上进行反应2SO2+O2![]() 2SO3(正反应为
2SO3(正反应为
放热反应),使用V2O5作催化剂.下列关于催化刘的叙述中,不正确的是( )
A、扩大反应物之间的接触面
B、降低了反应所需的能量增加了单位体积内的活化分子数
C、催化剂在反应中质量和化学性质均不变 D、催化剂在反应过程中不参与化学反应
12、NO和CO都是汽车尾气中的有害物质.它们能缓慢地起反应生成N2和CO2,对此反应的下列叙边中正确的是( )
A、使用催化剂不能加快反应速率 B、降低压强加快反应速率
C、升高温度能加快反应速率 D、改变压强对反应速率无影响
13、下列说法可以证明反应N2 +3 H2 ![]() 2NH3已达到化学平衡状态的是( )
2NH3已达到化学平衡状态的是( )
![]() A、一个N N键断裂的同时,有3个H―H键形成
A、一个N N键断裂的同时,有3个H―H键形成
B、N2、H2、NH3的分子数之比1:3:2
![]() C、一个N N键断裂的同时,有6个N―H键形成
C、一个N N键断裂的同时,有6个N―H键形成
D、N2、H2、NH3的浓度不再变化
14、可逆反应:2 NO2 ![]() 2NO+O2在体积固定的密闭容器中进行,达到平衡状态的标志是(A)①单位时间内生成nmol的O2同时生成2n mol NO2②单位时间内生成nmolO2时生成2nmol NO③用NO2与NO、O2表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的压强不再改变的状态⑦混合气体的平均相对分子质量不再改变的状态
2NO+O2在体积固定的密闭容器中进行,达到平衡状态的标志是(A)①单位时间内生成nmol的O2同时生成2n mol NO2②单位时间内生成nmolO2时生成2nmol NO③用NO2与NO、O2表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的压强不再改变的状态⑦混合气体的平均相对分子质量不再改变的状态
A、①④⑥⑦ B、②③⑤⑦ C、①③④⑤ D、全部
15、在1L密闭容器中,进行下列反应:X(g)+3Y(g)![]() 2Z(g),达到平衡后,其他条件不变,只增加X的量,下列叙述中正确的是( )
2Z(g),达到平衡后,其他条件不变,只增加X的量,下列叙述中正确的是( )
A、正反应速率增大.逆反应速率减小 B.、X的转化率变大
C、 Y的转化率变大 D、正、逆反应的速率都将增大
16、在一恒容的密闭容器中发生可逆反应C(s)+H2O(g)![]() CO(g)+H2(g)已达到平衡状态。现欲使平衡向正反应方向移动,且增大v(正).可进行的操作是( )
CO(g)+H2(g)已达到平衡状态。现欲使平衡向正反应方向移动,且增大v(正).可进行的操作是( )
A、再加人一些C B、移走一部分CO或H2
C.充入一些水蒸气 D、移走少量H2.并充人水蒸气
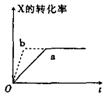 17、如右图所示, a曲线表示一定条件下可逆反应
17、如右图所示, a曲线表示一定条件下可逆反应
X(g)+Y (g)![]() 2Z(g)+W(s)(正反应是放热反应)的反应过程,若使a曲线变为b曲线,可采取的措施是( )
2Z(g)+W(s)(正反应是放热反应)的反应过程,若使a曲线变为b曲线,可采取的措施是( )
A、加人催化剂 B、增大Y的浓度 C、降低温度 D增大体系压强
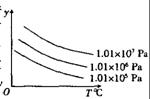 18、如右图表示外界条件,(温度、压强)的变化对下列反应的影响L (s)+G(g)
18、如右图表示外界条件,(温度、压强)的变化对下列反应的影响L (s)+G(g)![]() 2R(g)(正反应为吸热反应),在图象中,y轴是指( )
2R(g)(正反应为吸热反应),在图象中,y轴是指( )
A、平衡混合气体中R的百分含量
B、平衡混合气体中G的百分含量 C、G的转化率 D、 L的转化率
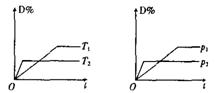
19、可逆反应mA(g)+nB(g)![]() pC(g)+qD(g)在反应过程中其他条件不变,D的百分含量和T或P关系如右图所示,下列叙述中正确的是( )
pC(g)+qD(g)在反应过程中其他条件不变,D的百分含量和T或P关系如右图所示,下列叙述中正确的是( )
 A、温度降低,化学平衡向正反应方向移动
A、温度降低,化学平衡向正反应方向移动
B、使用催化剂,D的物质的量分数增加
C、化学方程式系数m+n<p十q
D、加催化剂,有利于平衡向正反应方向移动
20、下列说法正确的是( )
A.合成氮工业中使用催化剂,使原来不能发生的反应变成可以发生了
B、且增大压强对溶液间的反应几乎无影响
C、温度升高,可以使吸热反应速率增大,也可使放热反应的速率增大
D、如果反应是放热的,则反应开始时不需加热
21、对于可逆反应N2(g)+3 H2(g)![]() 2NH3(正反应方向为放热反应),下列说法中正确的是( )
2NH3(正反应方向为放热反应),下列说法中正确的是( )
A、达到平衡后加人N2,当重新达到平衡时NH3的浓度比原平衡的大,H2的浓度比原平衡小
B、达到平衡后.升高温度,既加快了正、逆反应的速率,又提高了NH3的产率
C、达到平衡后,缩小容器的体积,既有利于加快正、过反应速率,又有利于提高氢气的转化率
D、加入催化剂可以缩短到达平衡的时间,是因为正反应速率增大了,逆反应速率减小了
22、合成氨生产过程中采用的措施与化学平衡移动原理无关的是( )
A、选择适应的温度 B、增大体系压强 C、使用催化剂 D、不断分离液氨
23、可逆反应X(g)十2Y(g)![]() 2Z(g)(正反应吸热).为了有利于Z的生成,应采取的反应条件是( )
2Z(g)(正反应吸热).为了有利于Z的生成,应采取的反应条件是( )
A、高温高压 B、高温低压 C、低温高压 D、低温低压
24、已知A+3B![]() 2C+D在某一时段内以A的浓度变化表示的化学反应速率为1 mol/L・min,则此段时间内以C浓度变化表示的化学反应速率为( )
2C+D在某一时段内以A的浓度变化表示的化学反应速率为1 mol/L・min,则此段时间内以C浓度变化表示的化学反应速率为( )
A、 0. 5 mol/ (L・min) B、1 mol/ (L・min)
C.、2 mol/ (L・min) D.、3 mol/ (L・min)
25、一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率且不形响生成H2的总量.可向盐酸中加人适量的( )
A、CaCO3(固) B、 Na2SO4溶液 C 、KNO3溶液 D.、CuSO4(固)
26、在一定温度下,向a L密闭容器中加人1mol X气体和2
molY气体,发生如下反应:X(g) +2Y(g)![]() 2Z(g),此反应达到平衡的标志是( )
2Z(g),此反应达到平衡的标志是( )
A、容器内压强不随时间变化
B、容器内各物质的浓度不随时间变化
C、容器内X、Y、Z的浓度之比为1:2:2
D、单位时间消耗0.1 mol X同时生成0.2 molZ
27、已知工业真空冶炼铷的原理如下(皆为熔融态)2RbCl+ Mg ![]() MgCI2 + 2Rb(g),对此反应的进行能给出正确解释的( )
MgCI2 + 2Rb(g),对此反应的进行能给出正确解释的( )
A.铷的金属活动性比镁弱
B、铷的沸点比镁低、把铷蒸气抽出.上述平衡向右移动
C、MgCI2的热稳定性不如RbCI强
D、铷单质比化合态更稳定
28、在恒温时,一固定容积的容器内发生如下反应2NO2(g)![]() N2O4(g)。达平衡时,再向容器内通人一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )
N2O4(g)。达平衡时,再向容器内通人一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )
A、不变 B、增大 C.、减小 D、无法判断
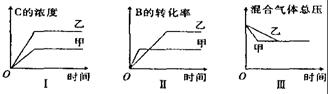 29、在容积固定的密闭容器中存在如下反应A (g)+3B(g)
29、在容积固定的密闭容器中存在如下反应A (g)+3B(g)![]() C(g); △H<0.某研究小组研条件不变时.改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是( )
C(g); △H<0.某研究小组研条件不变时.改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是( )
A、图I研究的是的不同催化剂对反应的影响,且乙使用的催化剂效率较高
B、图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C、图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D、图Ⅲ研究的是的不同催化剂对反应的影响,且甲使用的催化剂效率较高
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | ||||||||||
| 题号 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | |
| 答案 |
| 得 分 | 评卷人 |
二、填空题(本题共7小题,共51分)
30、(5分)在2 L的密闭容器中,加人1molN2和3mol的H2,发生 N2 +3 H2 ![]() 2NH3 ,在2s末时,测得容器中含有0.4 mol的NH3。
2NH3 ,在2s末时,测得容器中含有0.4 mol的NH3。
(1)求2s内用这三者分别表示该反应的速率各是 、 、 。
(2)三者速率之比是 。
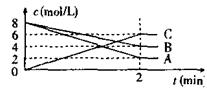 31、(5分)根据右图填空;
31、(5分)根据右图填空;
(1)、反应物是 ;生成物是 ;
(2)、在2分钟内A、B、C三者的反应速率值各是多少?
(3)、该反应化学方程式是 。
32、(5分)在一个容积为3 L的密闭容器内进行如下反应N2 +3 H2 ![]() 2NH3 。反应开始时n(N2)=1. 5 mol,n(H2)=4. 4 mol,2 min后、n(H2)=0.8 mol。试用H2、 N2、和NH3的浓度变化来表示该反应的反应速率是
, , 。2 min末的N2的浓度是
。
2NH3 。反应开始时n(N2)=1. 5 mol,n(H2)=4. 4 mol,2 min后、n(H2)=0.8 mol。试用H2、 N2、和NH3的浓度变化来表示该反应的反应速率是
, , 。2 min末的N2的浓度是
。
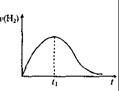 33、(6分)把除去氧化膜的镁条放人一定浓度的稀盐酸的试管中发现H2的生成速度v随时间t变化如图。其中t1之前速度变化的原因是
。
33、(6分)把除去氧化膜的镁条放人一定浓度的稀盐酸的试管中发现H2的生成速度v随时间t变化如图。其中t1之前速度变化的原因是
。
t1之后速度变化的原因是
。
34、(3分)发生火灾时,为什么在逃生和自救时应迅速有序地离开火灾现场,呼吸更多的新鲜空气,能够减轻或渭除CO的中毒?(血液中存在下列平衡:CO + Hb・O2![]() O2+Hb・CO)
O2+Hb・CO)
。
35、(4分)化学反应2A+B![]() 2C达到平衡时,回答下列问题:
2C达到平衡时,回答下列问题:
(1)如果A,B,C都是气体达到平衡时减小压强,那么 。
A、平衡不移动 B、平衡向正反应方向移动
C、平衡向逆反应方向移动 D.、C的浓度增大
(2)如果已知B是气体,增大压强时,化学平衡向逆反应方向移动,那么 。
A、A是气体.C是固体 B、 A,B,C都是气体
C、 A,C都是固体 D、A是固体、C是气体
36、(6分)在一个盛有催化剂的容积可变的密闭容器中,保持一定温度和压强,进行如下反应:N2 +3 H2 ![]() 2NH3 ,已知加人1molN2和4molH2时,达到平衡后生成a molNH3(见下表中的“已知”项),在相同的温度和压强下,保持平衡时各组分的体积分数不变,对下列编号①一③的状态.填写表中的空白。
2NH3 ,已知加人1molN2和4molH2时,达到平衡后生成a molNH3(见下表中的“已知”项),在相同的温度和压强下,保持平衡时各组分的体积分数不变,对下列编号①一③的状态.填写表中的空白。
| 编号 | 起始状态物质的量(mot) | 平衡时NH,的 物质的量(mot) | ||
| N2 | H2 | NH3 | ||
| 已知 | 1 | 4 | 0 | a |
| ① | 1.5 | 6 | 0 | |
| ② | 1 | 0. 5a | ||
| ③ | m | n(n≥4m) | ||
37、(6分)把N2和H2按物质的量之比1:2,置于V L密闭容器中合成氨,达到平衡时测得混合气体中含NH3的体积分数为20%,求:
(1)混合气体中含H2的体积百分数?
(2)反应前后容器内的压强比?
(3)N2和H2的转化率?
| 起始时各物质的物质的量(mol) | 平衡时NH3的物质的量(mol) | ||||
| 编号 | x(N2) | y(H2) | z(NH3) | ||
| 恒压 | (1) | 1 | 3 | 0 | a |
| (2) | 3 | 0 | |||
| (3) | 0.2 | 0.5a | |||
| x、y、,z取值必需满足的一般条件: | |||||
| 恒容 | (4) | 1 | 3 | 0 | b |
| (5) | 0 | 0 | b | ||
| (6) | 2.25 | b | |||
| x、y、,z取值必须满足的一般条件(一个只x、z.另一个只含y、z): 、 。 | |||||
| a与b的关系是a b(填>、<、=) | |||||
38、(11分)密闭容器中.保持一定温度.进行如下反应N2(g)+
3H2 (g)![]() 2NH3(g).已知加人1mol
N2和3mol H2,在恒压条件下,达到平衡时生成a mol NH3〔见下表中编号(1)的一行〕在恒容条件下,达到平衡时生成b mol NH3〔见下表中编号(4)的一行〕。若相同条件下,达到平衡时混合物中各组分的百分含量不变.请填空:
2NH3(g).已知加人1mol
N2和3mol H2,在恒压条件下,达到平衡时生成a mol NH3〔见下表中编号(1)的一行〕在恒容条件下,达到平衡时生成b mol NH3〔见下表中编号(4)的一行〕。若相同条件下,达到平衡时混合物中各组分的百分含量不变.请填空:
高二第二章化学检测试卷
答题卡
![]()
 一、选择题(本题包括29小题,每小题2分,共58分,每小题有一个或两个正确
一、选择题(本题包括29小题,每小题2分,共58分,每小题有一个或两个正确
答案)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | ||||||||||
| 题号 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | |
| 答案 |
二、填空题(本题共7小题,共51分
30、(5分)(1)求2s内用这三者分别表示该反应的速率各是 、 、 。
(2)三者速率之比是 。
31、(5分)(1)、反应物是 ;生成物是 ;
(2)、在2分钟内A、B、C三者的反应速率值各是多少?
(3)、该反应化学方程式是 。
32、(5分) 、 、 ; 。
33、(6)
、
。
34、(3分)
。
35、(4分)(1)、 ;(2)、 。
36、(6分)
| 编号 | 起始状态物质的量(mot) | 平衡时NH,的 物质的量(mot) | ||
| N2 | H2 | NH3 | ||
| 已知 | 1 | 4 | 0 | a |
| ① | 1.5 | 6 | 0 | |
| ② | 1 | 0. 5a | ||
| ③ | m | n(n≥4m) | ||
37、
| 起始时各物质的物质的量(mol) | 平衡时NH3的物质的量(mol) | ||||
| 编号 | x(N2) | y(H2) | z(NH3) | ||
| 恒压 | (1) | 1 | 3 | 0 | a |
| (2) | 3 | 0 | |||
| (3) | 0.2 | 0.5a | |||
| x、y、,z取值必需满足的一般条件: | |||||
| 恒容 | (4) | 1 | 3 | 0 | b |
| (5) | 0 | 0 | b | ||
| (6) | 2.25 | b | |||
| x、y、,z取值必须满足的一般条件(一个只x、z.另一个只含y、z): 、 。 | |||||
| a与b的关系是a b(填>、<、=) | |||||
参考答案
一、选择题(本题包括29小题,每小题2分,共58分,每小题有一个或两个正确
答案)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | A | D | B | C | B | B | A | AB | AC | B |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | A | C | AD | A | CD | CD | AD | B | AC | BC |
| 题号 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | |
| 答案 | AC | C | A | C | B | AB | B | C | AB |
| 起始时各物质的物质的量(mol) | 平衡时NH3的物质的量(mol) | ||||
| 编号 | x(N2) | y(H2) | z(NH3) | ||
| 恒压 | (1) | 1 | 3 | 0 | a |
| (2) | 3 | 9 | 0 | 3a | |
| (3) | 0.4 | 1.2 | 0.2 | 0.5a | |
| x、y、,z取值必需满足的一般条件:y≥3x(x≥0,z≥0) | |||||
| 恒容 | (4) | 1 | 3 | 0 | b |
| (5) | 0 | 0 | 2 | b | |
| (6) | 0.75 | 2.25 | 0.5 | b | |
| x、y、,z取值必须满足的一般条件(一个只x、z.另一个只含y、z): 2x+z=2 、 2y+3z=6 。 | |||||
| a与b的关系是a > b(填>、<、=) | |||||
30、(1)、0.05mol/l・s;0.15mol/l・s;0.1mol/l・s。(2)、1:3:2
31、(1)、A、B;C。(2)、3:2:3。(3)、3A+2B![]() 3C
3C
32、0.6mol/l・min;0.2mol/l・min、0.4mol/l・min;0.1mol/l。
33、反应开始温度低,反应速率慢,可反应为放热反应,随反应进行,温度升高,反应速率加快;随反应进行,反应物浓度逐渐减小,反应速率减小。
34、氧气的量增多,可使反应向逆向移动,使血液中的CO的含量减少。
35、(1)C、(2)D。
36、
| 编号 | 起始状态物质的量(mot) | 平衡时NH,的 物质的量(mot) | ||
| N2 | H2 | NH3 | ||
| 已知 | 1 | 4 | 0 | a |
| ① | 1.5 | 6 | 0 | 1.5a |
| ② | 0 | 0.5 | 1 | 0. 5a |
| ③ | m | n(n≥4m) | 2(n-4m) | (n-3m)a |
37、