绝密★启用前
高二化学下学期期末考试题
化 学 试 题
命题人:樊会武 审题人:孔松林
本试卷分第I卷(选择题)和第II卷(非选择题)两部分,满分110分,考试时间100分钟。
第I卷(选择题 共54分)
一、选择题(本题包括18小题,每小题只有一个选项符合题意,每小题3分,共54分。)
 1.2006年诺贝尔化学奖授予美国科学家Roger.D.Kormberg,他揭示了真核生物体内的细胞如何利用基因内存储的信息生产蛋白质。下列关于蛋白质的说法中正确的是
1.2006年诺贝尔化学奖授予美国科学家Roger.D.Kormberg,他揭示了真核生物体内的细胞如何利用基因内存储的信息生产蛋白质。下列关于蛋白质的说法中正确的是
A.蛋白质均为天然有机高分子化合物,没有蛋白质就没有生命
B.蛋白质均易溶于水,均能跟浓硝酸作用变黄
C.HCHO溶液或(NH4)2SO4溶液均能使蛋白质变性
D.可以采用多次盐析或多次渗析的方法分离提纯蛋白质
2、下列物质属于天然高分子化合物的是
A、聚乙烯 B、尼龙 C、油脂 D、纤维素
3、下列事实与胶体知识有关的是
①若做化学实验时手指不慎被划破,可从急救箱中取FeCl3溶液应急止血 ②用氯化铁净水 ③在水泥厂、冶金工厂常用高压电对气溶胶作用除去大量烟尘 ④制肥皂时在高级脂肪酸钠、甘油和水形成的混合物中加入食盐析出肥皂 ⑤动植物尸体在土壤里的腐败 ⑥喝了含MgCl2的卤水,可以用牛奶或豆浆解毒
A、只有②③④ B、只有④⑤⑥ C、只有①②⑤ D、全部都是
4、下列各组分子中的各个原子,或处于同一平面,或在一条直线上的是
A、C6H6,C2H4,CO2 B、CS2,NH3,HC≡CCH3
C、H2O,HCl,CH4 D、C2H6,HCHO,C2H2
5、以下对生活事实的解释,不正确的是
A.厨房里洗涤油污,常用碱性洗涤剂,因为植物油会在碱性溶液中水解
B.食品添加剂虽然能改善食物的色、香、味,但由于他们对健康有害,均不宜食用
C.甲醛溶液虽能使细菌的蛋白质变性而死亡,但不宜浸泡海产食品
D.用加酶洗衣粉在温水中不能洗涤毛料服装
6、下列各化合物中,使发生酯化、还原、加成、消去四种反应的是
A.CH3-CH=CH-CHO
B.CH3-![]() -
-![]() -CH3
-CH3
 C.HOCH2-CH2-CH=CH-CHO D.HOCH2-
C.HOCH2-CH2-CH=CH-CHO D.HOCH2-![]() -CH2-CHO
-CH2-CHO
7、下列关于晶体的说法正确的是
A.离子晶体中一定不含共价键
B.金属晶体的熔点一定比原子晶体低、一定比分子晶体高
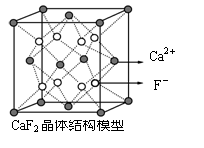
C.CaF2晶体中与一个Ca2+距离最近且距离相等F-的有4个
D.SiO2晶体中每个Si原子与四个O原子以单键相结合
8、2006年5月21日中央电视台“每周质量报告”报道:齐齐哈尔第二制药公司生产的亮菌甲素注射液,由于用二甘醇(HOCH2CH2OCH2CH2OH)冒充丙二醇(HOCH2—CH2—CH2OH)作为药用辅料,造成多人死伤事件。下列有关二甘醇和丙二醇的说法,不正确的是
A、二甘醇和丙二醇都是易溶于水的物质 B、丙二醇和丙三醇互为同系物
C、二甘醇和丙二醇都能和乙酸发生酯化反应
D、二甘醇和丙二醇都能发生催化氧化反应,最终生成二元羧酸
9、苯环上连接有一个烃基(—R)和3个—X基的有机物结构式共有
A.4种 B.5种 C.6种 D.7种
10、设NA为阿伏加德罗常数,下列有关说法正确的是
A.58.5g氯化钠中约含有6.02×1023个氯化钠分子
B.铜的电解精炼时,当阴极析出32gCu时,阳极产生的Cu2+离子数为0.5NA
C.将5.0mol·L-1的FeCl3溶液20mL滴加到沸水中形成的胶体中,分散质粒子数为0.1NA
D.常温常压下,14 g乙烯中含有的共用电子对数为3NA
11、下列说法中正确的是
A.用渗析法分离Fe(OH)3胶体和FeCl3溶液的混合物
B、分子式为CH3C(CH3)2CH2Br在NaOH的醇溶液中发生消去反应生成相应的烯烃
C、以Cu为阳极电解时Cu被除数氧化为Cu2+,以Fe为阳极电解时Fe 也被氧化为Fe3+
D、由于氢键的影响,甲酸蒸气的密度在373K时为1.335g•L-1,在293K时为2.5 g•L-1
12、仔细分析下列表格中烃的排列规律,判断排列在第15位的烃的分子式是
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | …… |
| C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | …… |
A.C6H12 B.C6H14 C.C7H12 D.C7H14
13、两种电解装置:①以铜为电极对Na2SO4溶液进行电解 ②以铂为电极对Na2SO4溶液进行电解当两装置中产生的氢气质量相同,两装置消耗的水的质量之比为
A.1:1 B.2:1 C.1:2 D.有一装置不消耗水,无法比较
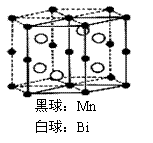 14、磁光盘机(Magnetic Optical Disk Drive,MO)是一种可重写的光盘驱动器,它使用磁光盘片作存储媒体。磁光存储的研究是Williams等在1957年使Mn和Bi形成的晶体薄膜磁化并用光读取之后开始的。下图是该物质的晶体结构,其化学式可表示为
14、磁光盘机(Magnetic Optical Disk Drive,MO)是一种可重写的光盘驱动器,它使用磁光盘片作存储媒体。磁光存储的研究是Williams等在1957年使Mn和Bi形成的晶体薄膜磁化并用光读取之后开始的。下图是该物质的晶体结构,其化学式可表示为
A.Mn2Bi B.MnBi C.MnBi3 D.Mn4Bi3
15、下列离子方程式书写不正确的是
A、AgNO3溶液中滴入过量氨水:Ag+ + 2NH3·H2O = Ag(NH3)2+ + H2O
|
C、电解饱和食盐水:2Cl- + 2H2O ==== H2↑+ Cl2↑+2OH-
|
16、下列有关化学实验的操作或说法中,不正确的是
A、医疗上判断糖尿病患者病情的方法可用新制的Cu(OH)2来测定患者尿液中葡萄糖的含量
B、在进行硫酸铜晶体里结晶水含量的测定实验中,称量操作至少要进行4次
C、检验溴乙烷中的溴元素时,将溴乙烷和氢氧化钠溶液混合加热后,加入稀H2SO4进行酸化
D、将铜丝在酒精灯外焰上加热变黑后,再移至内焰铜丝又恢复到原来的红色
17、人类已进入网络时代,长时间看显示屏幕的人,会感到眼睛疲劳,甚至会对眼睛有一定的伤害。人眼中的视色素中含有视黄醛(甲)作为辅导基的蛋白质,而与视黄醛相似结构的维生素A(乙)常作为保健药物。则下列有关叙述正确的是

A、视黄醛的分子式为C20H26O B、视黄醛和维生素A互为同分异构体
C、维生素A是视黄醛的还原产物 D、1mol视黄醛最多能与5molH2加成
18、实验室制取乙酸乙酯1mL 后,沿器壁加入紫色石蕊试液0.5 mL,这时石蕊试液将存在于饱和碳酸钠层与乙酸乙酯层之间(整个过程不振荡试管),对可能出现的现象,叙述正确的是
A、石蕊层仍显紫色,有机层无色 B、石蕊层有两层,上层紫色,下层蓝色
C、石蕊层为三层,由上而下是蓝、紫、红 D、石蕊层为三层、由上而下是红、紫、蓝
第II卷(非选择题共56分)
二、解答题(本题包括5小题,共56分)
19、(13分)按照下图所示装置进行有关实验,拔掉分液漏斗玻璃塞,将A逐滴加入B中。
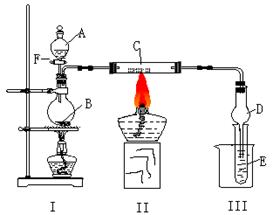
⑴ 若A是乙醇,B是生石灰,实验中观察到C中黑色固体逐渐变红。当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁出现了光亮的银镜。则C是 ,在反应作 剂(填“氧化”或“还原”),写出硬质玻璃管C中所发生的反应方程式 。试管E中所发生反应的离子方程式 。
⑵ 若A是能发生银镜反应且只含一个碳的一种液态有机物,B为浓硫酸,E为苯酚钠溶液,C不变。实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管E中溶液变浑浊,则A是(写名称) 。然后往烧杯中加入沸水,则试管E中的现象是 。此实验中浓硫酸的作用是 。写出硬质玻璃管C中所发生的反应方程式 。写出乙醇和⑵题中A这二种物质在浓硫酸存在时所发生的反应方程式 。
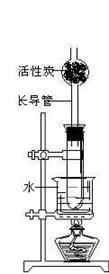 20、(16分)吉林市中石油吉化公司双苯厂苯胺车间发生爆炸事故,流入进松花江的硝基苯类污染物总量达100吨左右,对松花江水体造成严重污染,有一百多万人口都受到影响。实验室用浓硫酸、浓硝酸和苯(沸点80.1℃)在55~60℃时混合加热制得硝基苯,某学生设计了如图的试验装置制硝基苯(沸点210.9℃)。
20、(16分)吉林市中石油吉化公司双苯厂苯胺车间发生爆炸事故,流入进松花江的硝基苯类污染物总量达100吨左右,对松花江水体造成严重污染,有一百多万人口都受到影响。实验室用浓硫酸、浓硝酸和苯(沸点80.1℃)在55~60℃时混合加热制得硝基苯,某学生设计了如图的试验装置制硝基苯(沸点210.9℃)。
⑴ 混合浓硫酸和浓硝酸的操作是 ,反应方程式为 。
⑵ 已知苯在55~60℃发生硝化反应,在75~80℃发生磺化反应,95℃发生二硝基取代反应。为防止发生副反应,如何控制温度?采取的措施是 。
⑶ 装置中长导管的作用是 ,活性炭的作用 。
⑷ 反应后试管中有硝基苯、苯和残酸,为得到纯净的硝基苯,要用如下操作精制:① 用蒸馏水洗、分液;② 蒸馏;③ 用无水CaCl2干燥;④ 用W=5%的NaOH溶液洗涤、分液;⑤ 蒸馏水再洗涤、分液。正确的操作顺序为
A、①③④⑤② B、②③④①⑤ C、①④⑤③② D、①④②⑤③
⑸ 现有锥形瓶、铁架台、酒精灯、蒸馏烧瓶、活塞、铁圈,还需要的主要仪器有 。蒸馏得到的硝基苯聚集在 ,它是一种 色 味油状液体。
⑹ 硝基苯是剧毒物质,它及它在人体的中间转化物均能使蛋白质变性。下列物质中不能使蛋白质变性的是( )
A、高浓度的过氧化氢溶液 B、饱和硫酸铵溶液 C、醋酸铅溶液 D、甲醛
⑺ 使用活性炭能减轻松花江的水污染。活性炭是一种多孔径、状疏松的炭化物。生产活性炭分为两步。一是炭化(将原料在170~600℃的温度下干燥),二是活化(使炭化好的料与活化剂、水蒸气反应)。为降低活性炭的费用,科学家建议用稻草、秸秆来代替活性炭,也能起到减轻污染效果,这是因为稻草、秸秆中的有机碳可以吸附有机物。写出稻草、秸秆所含主要成分的通式 。
21、(14分)咖啡酸是某种抗氧化剂成分之一,其球棍模型如下图,请回答下列问题:
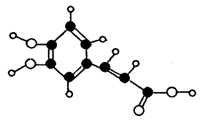 ⑴ 咖啡酸的分子式为______________,其含氧官能团的名称为_____________;
⑴ 咖啡酸的分子式为______________,其含氧官能团的名称为_____________;
⑵ 咖啡酸可以发生的反应类型是(填写选项序号)_____________________;
①氧化反应 ②加成反应 ③酯化反应 ④加聚反应 ⑤消去反应
⑶ 写出咖啡酸与足量氢氧化钠反应的化学方程式: ;
⑷ 咖啡酸有多种同分异构体,请写出三种只含一个苯环、一个一CH2一、一种含氧官能团的咖啡酸的同分异构体:_______________、_____________、________________;
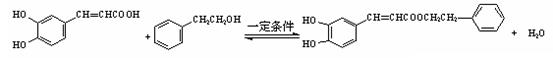
⑸ 蜂胶的主要活性成分为CPAE,分子式为C17H16O4,该物质在一定条件下可水解生成咖啡酸和一种醇,该醇为芳香醇,且分子结构中无甲基,则咖啡酸跟该芳香醇在一定条件下反应生成CPAE的化学方程式为: 。
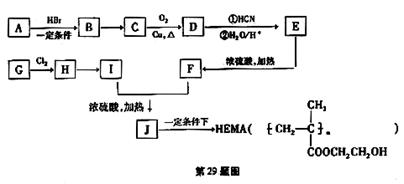
22、(17分)
|
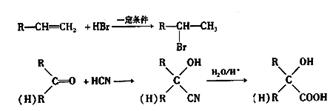
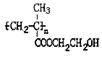
已知:①A、G为烃而且互为同系物,A的分子式为C3H6;CH3COOCH2CH2OH的名称为乙酸羟乙酯
|
②
③
请回答以下问题:
⑴ 试写出E、G的结构简式:E ,G 。
⑵ 反应B→C 及H→I的反应条件相同,其条件是 。
⑶ 写出下列反应的反应类型:E→F ,G→H ,J→HEMA 。
⑷ 化合物F具有的化学性质(填写字母代号)是 。
a.可以发生水解反应 b.可以发生还原反应
c.可以发生酯化反应 d.一定条件下可以发生加聚反应
⑸ 写出满足a.能发生银镜反应;b.能与碱发生中和反应;c.分子结构中无甲基;上述三个条件的J的同分异构体的结构简式____________________。
⑹ 写出下列转化的化学方程式:
H→I: ;
|
⑺ 隐形眼镜材料选用
的理由是 。
高二下学期期末考试
化学试题答案
一、选择题(本题包括18小题,每小题只有一个选项符合题意,每小题3分,共54分。)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | D | D | D | A | B | C | D | B | C |
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | D | D | B | A | B | A | C | C | D |
二、解答题(本题包括4小题,共56分。)
19、
|
CH3CHO + 2[Ag(NH3)2]+ + 2OH- → CH3COO- + NH4+ + 2Ag↓+ 3NH3 + H2O (2分)
⑵ 甲酸(1分) 变澄清 (1分) 脱水剂 (1分)
CO + CuO = Cu + CO2(2分)
HCOOH + C2H5OH![]() COOC2H5+H2O (2分)
COOC2H5+H2O (2分)
20、(16分)答案:
⑴ 将浓硫酸沿烧杯壁缓慢倒入装有浓硝酸的烧杯中,边加边搅拌。(2分)
(2分)
⑵ 使用温度计控制水浴温度在55~60℃ (1分)
⑶ 冷凝回流,使反应物苯、硝酸充分反应。(1分)
吸收苯和硝基苯,防止其污染大气。(1分)
⑷ C (2分)
⑸ 温度计、冷凝管、沸石(2分),蒸馏烧瓶(1分)、无色或浅黄色、苦杏仁味,(1分)
⑹ B (1分) ⑺ (C6H10O5)n (2分)
21、(12分)
⑴ C9H8O4 (1分) 羧基、羟基(各1分,共2分)
 ⑵ ①②③④(2分,错一扣1分,错二扣完)
⑵ ①②③④(2分,错一扣1分,错二扣完)
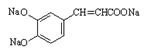
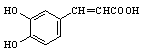 ⑶ +
3NaOH→
+3H2O(2分)
⑶ +
3NaOH→
+3H2O(2分)
⑷ (各1分,共3分)
![]() (邻、间、对三种) 或
(邻、间、对三种) 或 ![]() (邻、间、对三种)
(邻、间、对三种)
⑸ (2分)
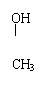 22、(15分)
22、(15分)
![]() ⑴ CH3—C—COOH CH2=CH2 (2分) ⑵ NaOH/H2O溶液(1分)
⑴ CH3—C—COOH CH2=CH2 (2分) ⑵ NaOH/H2O溶液(1分)
⑶ 消去反应 加成反应 加聚反应(3分) ⑷ bcd(2分)
⑸ OHCCH2CH2CH2CH2COOH;(1分)
⑹
H→I:CH2ClCH2Cl
+ 2H2O![]() HOCH2CH2OH + 2HCl
HOCH2CH2OH + 2HCl
I+F→J: HOCH2CH2OH
+ CH2=C(CH3)COOH![]() CH2=C(CH3)COOCH2CH2OH
+ H2O
CH2=C(CH3)COOCH2CH2OH
+ H2O
(其它合理答案均可,每个2分,共6分)
|
⑺ 因 的结构中含有—OH,具有亲水保湿作用(2分)