高二化学下学期第二次月考
高二化学试题
说明:
1. 本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟。
2. 答题前,考生务必将自己的班级、姓名、座号填写在试卷指定位置。
3. 答案写在各题指定的答题处。
4. 本卷可能用到的相对原子质量如下:H:1 Na:23 C:12 O:16
第Ⅰ卷 选择题(共42分)
一、选择题(本题包括18小题,1-12每小题3分,13-18每小题3分,共42分,每小题只有一个正确答案):
1.现代以石油化工为基础的三大合成材料是( )
①合成氨 ②塑料 ③医药 ④合成橡胶 ⑤合成尿素 ⑥合成纤维 ⑦合成洗涤剂
A.②④⑦ B.②④⑥ C.①③⑤ D.④⑤⑥
2、在有机溶剂中难溶解只能有所胀大的高聚物,它的结构通常是
A.线型结构 B.无定型结构 C.晶体型结构 D.体型结构
3、下列化学式能真实表示物质分子组成的是 ( )
A.NaOH B.SO3 C.CsCl D.NaCl
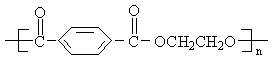 4.2008奥运吉祥物福娃,其外材为纯羊毛线,内充物为无毒的聚酯纤维(如图)。下列说法正确的是( )
4.2008奥运吉祥物福娃,其外材为纯羊毛线,内充物为无毒的聚酯纤维(如图)。下列说法正确的是( )
A.羊毛与聚酯纤维的化学成分相同
B.聚酯纤维和羊毛一定条件下均能水解
C.该聚酯纤维的单体为对苯二甲酸和乙醇
D.聚酯纤维属于纯净物
5.为保证加酶洗衣粉洗涤效果,应注意( )
A.使用沸水先冲泡洗衣粉 B.用含氯较高的自来水作水源
C.和其他洗涤剂混合使用 D.室温时用软水先溶解洗衣粉
6.1999年美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,下列推断中不正确的是( )。
A.原子晶体干冰有很高的熔点、沸点,有很大的硬度
B.原子晶体干冰易气化,可用作制冷材料
C.原子晶体干冰的硬度大,可用作耐磨材料 D.每摩尔原子晶体干冰中含4molC―O键
7.固体草酸晶体中不存在的作用力是( )
A.离子键 B.共价键 C.氢键 D.分子间作用力
8.下列现象不属于蛋白质变性的是( )
A.打针时用酒精消毒 B.用福尔马林浸制标本
C.用紫外线照射病房 D.蛋白质不溶于(NH4)2SO4溶液中
9、蔗糖3.42g与淀粉3.24g混合并完全水解,若生成mg葡萄糖和ng果糖,则m∶n为( )
A.1∶3 B.1∶5 C.5∶1 D.3∶1
10.食用花生油中含有油酸,油酸是一种不饱和脂肪酸,对人体健康有益。其结构如下:
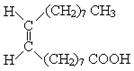
下列说法不正确的是
A.油酸的分子式为C18H34O2 B.油酸可与氢氧化钠溶液发生中和反应
C.1 mol油酸可与2 mol氢气发生加成反应 D.1 mol甘油可与3 mol油酸发生酯化反应
11.把①蔗糖②淀粉③油脂④蛋白质在稀酸存在的条件下分别充分水解,最后生成物只有1种的是( )
A.①② B.②③④ C.② D.③
12.在常温常压下呈气态的化合物、降温使其固化得到的晶体属于( )
A.分子晶体 B.原子晶体
C.离子晶体 D.何种晶体无法判断
13.关于氢键,下列说法正确的是( )
A.氢键比范德华力强,所以它属于化学键
B.分子间形成的氢键使物质的熔点和沸点升高
C.氨与水分子之间不能形成分子间氢键
D.H2O是一种非常稳定的化合物,这是由于氢键所致
14. 下列叙述正确的是( )
A 直径介于1nm~100nm之间的微粒称为胶体
B 电泳现象可证明胶体属电解质溶液
C 利用丁达尔效应可以区别溶液与胶体
D 欲将蛋白质从水中析出而又不改变它的性质,应加入CuSO4溶液
15、钡在氧气中燃烧时的得到一种钡的氧化物晶体,起结构如下图所示,有关说法正确的是( )
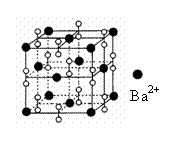 A、该晶体属于离子晶体
A、该晶体属于离子晶体
B、晶体的化学式为Ba2O2
C、该晶体晶胞结构与CsCl相似
D、与每个Ba2+距离相等且最近的Ba2+共有8个
16、下列四种晶体代表物的性质表述中,错误的是( )
A. 汞在固态和液态时都能导电
B. 硫酸在固态和熔融态时都不能导电
C. 二氧化硅在固态和熔融态时都不能导电
D. 氢氧化钠在固态和熔融态时都能导电
17、下列关于晶体的说法一定正确的是( )
A 分子晶体中都存在共价键
B 含有离子键的化合物形成的晶体一定是离子晶体
C SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D 金属晶体的熔点都比分子晶体的熔点高
18.下列说法错误的是( )
A. 血液中的血细胞直径在1~100nm之间,所以血液是胶体
B. 糖类是具有甜味的物质
C. 碘和干冰升华时,克服的粒子间作用属于同一类型
D. 葡萄糖能跟新制的氢氧化铜反应生成红色沉淀
第Ⅱ卷 非选择题(共58分)
二、填空题:
19.(9分)(1)将饱和氯化铁溶液滴入沸水时,液体变为 色,得到的是 ;反应的离子方程式是 ;用此分散系进行下列实验:将其装入U型管内,用石墨做电极,接通直流电,通电一段时间后发现阴极附近的颜色 ,这表明 ,这种现象称为 。
![]() (2)合成结构简式为
(2)合成结构简式为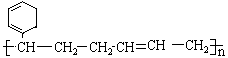 的高聚物,其单体的结构简式应是
和
。
的高聚物,其单体的结构简式应是
和
。
20.(13分)如图所示是某些晶体的结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一部分。
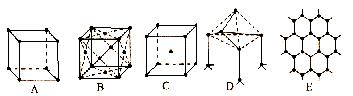
⑴ 其中代表金刚石的是(填编号字母,下同)______________,其中每个碳原子与______个碳原子最接近且距离相等。金刚石属于_________晶体。
⑵ 其中代表石墨的是____________,其中每个正六边形占有的碳原子数平均为______个。
⑶ 其中代表NaCl的是___________。
⑷ 代表CsCl的是_____________,它属于___________晶体,每个Cs+与______个Cl―紧邻。
⑸ 代表干冰的是________,它属于______晶体,每个CO2分子与______个CO2分子紧邻。
⑹ 上述五种物质熔点由高到低的顺序是_______________________________。
三、实验题(本题共2小题,共14分):
21、(4分)下列实验操作或叙述,正确的是_______(填写代号)
A、把饱和FeCl3滴入1mol/LNaOH溶液中制备Fe(OH)3胶体。
B、乙酸乙酯中少量乙酸可用饱和Na2CO3溶液除去
C、蔗糖水解时应用浓H2SO4作催化剂
D、在鸡蛋白溶液中滴入浓HNO3,加热会产生黄色物质
E、在植物油中滴入溴水,溴水褪色
F、用盐析法分离油脂皂化反应的产物
22、(10分)根据测定硫酸铜晶体中结晶水含量的实验,填写下列空白:
⑴ 加热前应将晶体放在 中研碎,加热时放在 中进行,加热失水后,应该在 中冷却。
⑵ 本实验至少需要加热_____________次,至少需要称量__________次;
⑶ 某学生实验得到以下数据:加热前容器的质量为m1,容器和晶体的总质量为m2,加热后容器和无水CuSO4的总质量为m3。请求出CuSO4・nH2O中n的值(用ml、m2、m3表示):n = _____________________
⑷ 若ml = 5.4g、m2 = 7.9g、m3 = 6.8g,该生结果偏高还是偏低? _______________
从下列分析中选出该生实验产生误差的原因可能是(填写字母) ___________________
A、加热前称量时容器未完全干燥 B、最后两次加热后的质量差大于0.1g
C、加热后容器未放在干燥容器中冷却 D、加热过程中有少量晶体溅出
E、加热后的粉末中有少量黑色固体
四、推断题(本题共2小题,共22分):
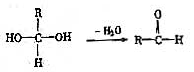 23.(16分)已知一个碳原子上连有两个羟基时,易发生下列转化:
23.(16分)已知一个碳原子上连有两个羟基时,易发生下列转化:
请根据下图回答。
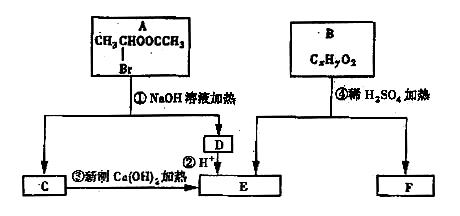
(1)E中含有的官能团的名称是 ;③的反应类型是 ;C跟新制的氢氧化铜反应的化学方程式为 。
(2)已知B的相对分子质量为162,其燃烧产物中n(CO2):n(H2O)=2:1。则B的分子式为 。
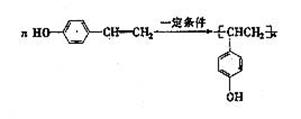
(3)在电脑芯片生产领域,高分子光阻剂是光刻蚀0.11![]() m线宽芯片的关键技术。F是这种高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为
m线宽芯片的关键技术。F是这种高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为
。
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应。G可能有 种
结构,写出其中任意一种同分异构体的结构简式 。
24.(6分)某天然油脂A的分子式为C57H106O6。1mol该油脂水解可得到1mol甘油、1mol不饱和脂肪酸B和2mol直链饱和脂肪酸C。经测定B的相对分子质量为280,原子个数比为C:H:O=9:16:1。
(1)写出B的分子式: 。(2)写出C的结构简式: 。
(3)写出C的甘油酯皂化反应的化学方程式: 。
|
|
|
|
题
|
| 名 姓
|
答 |
|
|
准
|
| 号 座
| 不
|
|
| 内
线
|
| 级 班
|
封
|
|
|
密
|
| 校 学 |
|
|
|
|
高 二 化 学 答 题 卷
一、选择题(本题包括18小题,1-12每小题2分,13-18每小题3分,共42分,每小题只有一个正确答案)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | |||||||||
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 |
二、填空题:
19.(9分)(1) , ; ;
, , 。
(2) 和 。
20.(13分)
⑴ , 。_________。
⑵____________, ______。 ⑶___________。
⑷_____________, ___________, ______。
⑸________, ______, ______。
⑹_______________________________。
三、实验题(本题共2小题,共14分):
21、(4分)正确的是 (填写代号)
22、(10分)⑴ , , 。
⑵_____________次, __________次;
⑶n = _____________________
⑷_______________ , __________________(填写字母)
23.(16分)
(1) ;
。
(2) 。
(3)
。
(4) 种 。
24.(6分)
(1) 。(2) 。
(3) 。
第二次月考参考答案
二、选择题(本题包括18小题,1-12每小题2分,13-18每小题3分,共42分,每小题只有一个正确答案)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | B | D | B | B | D | B | A | D | D |
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | C | C | A | B | C | A | D | B | B |
二、填空题:
![]() 19.(9分)(1) 红褐 , Fe(OH)3 胶体 ; Fe3++3H2O== Fe(OH)3 (胶体)+3H+ ;
19.(9分)(1) 红褐 , Fe(OH)3 胶体 ; Fe3++3H2O== Fe(OH)3 (胶体)+3H+ ;
变深 , Fe(OH)3 胶粒带正电荷 , 电泳 。
![]() (2) CH2=CH-CH=CH2 和
(2) CH2=CH-CH=CH2 和
20.(13分)⑴ D,4,原子 ⑵ E;2 ⑶ A ⑷ C;离子;8 ⑸ B;分子;12
⑹ 石墨>金刚石>NaCl>CsCl>干冰
三、实验题(本题共2小题,共14分):
21、(4分)正确的是 BDEF(填写代号)
22、(10分)⑴研钵,坩埚,干燥器。
⑵二,四。
![]() ⑶
⑶
⑷偏高; A、D、E
四、推断题(本题共2小题,共22分):
23.(16分) (1)羧基(2分);氧化反应(2分);CH3CHO+2Cu(OH)2![]() CH3COOH+Cu2O+2H2O(3分)
CH3COOH+Cu2O+2H2O(3分)
 (2)C10H10O2 (2分)
(2)C10H10O2 (2分)
(3) (3分)
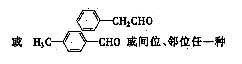
(4) 4 (2分); 任写一种(2分)
24.(6分)(1)C18H32O2(2分)(2)CH3(CH2(CH2)16COOH(2分)
![]() (3)C17H35COOCH2
CH2OH
(3)C17H35COOCH2
CH2OH
![]()
![]()
![]() C17H35COOCH +3NaOH→3C17H35COONa+ CHOH
C17H35COOCH +3NaOH→3C17H35COONa+ CHOH
![]()
![]() C17H35COOCH2
CH2OH
C17H35COOCH2
CH2OH