高二化学氮族元素测试题
高 二 年 级 化 学
请将正确答案填在答题卡上,填在试卷上的答案无效!
可能用到的原子量:
H—1 O—16 C—12 S—32 N—14 K—39 Cl—35.5 Ca—40 Mg—24 Zn—65 Na—23 Cu-64 Fe-56
一.选择题(本题包括个20小题,每小题只有一个正确答案,每小题分,共40分)
1、下列气体中,不会造成空气污染的是 ( )
A、N2 B、NO C、NO2 D、CO
2、通常情况下,既能用浓硫酸干燥,又能用碱石灰干燥的是 ( )
A、NH3 B、Cl2 C、NO D、HCl
3、下列气体的制取中,与氨气的实验室制取装置相同的是 ( )
A.CO2 B.H2 C.Cl2 D.O2
4.能将NH4Cl.(NH4)2SO4.NaCl.Na2SO4四种溶液一一区分开的试剂是 ( )
A.NaOH溶液 B.AgNO3溶液 C.BaCl2溶液 D.Ba(OH)2
5、下列关于氮族元素的说法中不正确的是 ( )
A、原子的最外层均有5个电子,最高价均为+5价
B、非金属性比同周期的氧族元素和卤族元素弱
C、原子半径比同周期的氧族元素、卤族元素小
D、稳定性:NH3 > PH3
6、下列离子方程式不正确的是 ( )
A、(NH4)2CO3溶液与足量的NaOH溶液混合加热:NH4+ + OH- ==NH3↑ + H2O
B、Cl2通入到FeCl2溶液中:Cl2 + Fe2+ == 2Cl- + Fe3+
C、将银片投入到浓硝酸溶液中:Ag + 2H+ + NO3 - == Ag+ + NO2↑ + H2O
D、过量Ba(OH)2和磷酸溶液反应:3Ba2+ + 6OH- + 2H3PO4==Ba3(PO4)2↓+6H2O
7、6.4g铜放入400ml浓度为0.5mol/L的硝酸中,充分反应后,被还原的HNO3的量为 ( )
A、0.03mo l B、0.05mol C、0.1mol D、0.2mol
8.生物固氮是指( )
A 生物从土壤中吸收含氮养料
B 豆科植物根瘤菌将含氮化合物转变为植物蛋白质
C 将氨转变成硝酸及其它氮的化合物
D 生物将空气中的氮气转变成含氮化合物
9、使用单质铜制硝酸铜,耗用原料最经济,而且对环境几乎没有污染的是
![]()
![]() A.Cu+HNO3(稀)
B.Cu CuO
Cu(NO3)2
A.Cu+HNO3(稀)
B.Cu CuO
Cu(NO3)2
![]()
![]() C.Cu+HNO3(浓)
D.Cu CuCl2 Cu(NO3)2
C.Cu+HNO3(浓)
D.Cu CuCl2 Cu(NO3)2
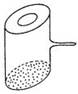
10、实验室里常见到如图所示的仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄。当玻璃管内装有碘片时,用此仪器进行碘的升华实验,具有装置简单、操作方便、现象明显、可反复使用等优点。用此仪器不能反复进行的实验是
A.NH4Cl受热分解的实验 B.KMnO4受热分解的实验
C.白磷和红磷在一定温度下相互转变的实验 D.无水CuSO4与胆矾的互变实验
[ 解析]要能反复进行,则 在不同条件下可以进行互为逆向的两个变化,由于KMnO4受热分解的产物不能化合生成KMnO4 ,故选B。
11、对于易燃、易爆的、有毒的化学物质,往往会在其包装上贴上危险警告标签,下面所列物质,贴错了包装标签的是
| A | B | C | D | |
| 物质的化学式 | 浓HNO3 | CCl4 | P4(白磷) | NH4NO3 |
| 危险警告标签 |
|
|
|
|
[解析]由于CCl4 中碳元素呈+4价,所以CCl4 不可燃,相反可以作灭火剂。[答案]B。
12.下列反应中,能说明NH3 既有碱性又有还原性的是( )
A 。2 NH3 +2Na==2NaNH2 +H2 B。8 NH3+3 Cl2==6NH4Cl+N2
C。2 NH3+3CuO==N2+3Cu+3H2O D. 4 NH3+6NO==5N2+6H2O
[解析]要能说明NH3 既有碱性又有还原性,则该反应中既要生成铵盐,又要产生高价态的含氮物质。[答案]B
13、 关于磷的下列叙述中,正确的是( )
A、红磷没有毒性而白磷剧毒
B、白磷在空气中加热到260℃可转变为红磷
C、白磷可用于制造安全火柴
D、少量白磷应该保存在煤油中
14、下列对硝酸的认识不正确的是
A.打开浓硝酸的瓶盖会产生棕色的烟
B.稀硝酸也是一种强氧化性的酸
C.硝酸是常用来作制炸药、化肥、染料的化工原料
D.不慎将浓硝酸滴在手上,若不及时擦去后会在皮肤上留下黄色斑痕
[解析]浓硝酸挥发出来的小液滴是白色的,故A错。皮肤的成分是蛋白质,遇浓硝酸发生颜色反应而发黄。
15.下列关于氨气的说法正确的是
A.氨气的检验方法为:将沾有浓盐酸的玻璃棒或者用沾有湿润的蓝色石蕊试纸玻璃棒靠近容器口
B.氨水能导电,所以NH3是电解质
C.制取氨气可以使用NH4Cl受热分解
D.用向下排空气法收集NH3
[解析]应用湿润的红色石蕊试纸玻璃棒靠近容器口检验 氨气,故A错;氨水能导电,不是氨气本身电离,所以NH3不是电解质,即B错;由于氨气分子间存在氢键,所以沸点:NH3 高于PH3,即C错。[答案]D
16、木炭屑与浓HNO3共热,产生的气体等分为①和②两份,将第一份气体先导入适量蒸馏水中再导入石灰水中,将第二份气体直接导入石灰水中,则石灰水的变化可能是
A.①不变浑浊②变乳白色 B.①变乳白色②不变浑浊
C.①变乳白色②变乳白色 D.①不变浑浊②变浅黄色
[解析]木炭屑与浓HNO3共热,产生气体为NO2和CO2 ,第一份气体先导入适量蒸馏水中再导入石灰水中,NO2和水 反应了,因此CO2 可和石灰水反应产生沉淀;第二份气体直接导入石灰水中,主要发生NO2和石灰水反应,故无沉淀。[答案]B。
17、下列说法中不正确的是 ( )
A、NO中有少量的NO2:用水洗涤后再干燥
B、白磷应保存在水中,切割白磷应在水下进行。
C、N2中有少量的O2:通过灼热的铜网
D、红磷中有少量的白磷:加热到40℃,使白磷自燃
[解析]加热到40℃, 白磷自燃放热也会使红磷燃烧,故D错。[答案]D
18、氨水中存在的粒子有( )
①NH3 ②NH3•H2O ③H2O ④OH- ⑤NH4+ ⑥H+
A.①②③④ B.②④⑤⑥ C.①②③④⑤ D.①②③④⑤⑥
19、取三张蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加65%的HNO3、98.3%的H2SO4和新制的氯水,三张试纸最后依次呈现的颜色是( )
A.白、红、白 B.红、黑、红 C.红、红、红 D.白、黑、白
20、如图所示,夹子开始处于关闭状态,将液体A滴人试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能是下列的
A.氢氧化钠溶液、二氧化碳
B.水、氨气
C.氢氧化钠溶液、一氧化氮
D.水、二氧化氮
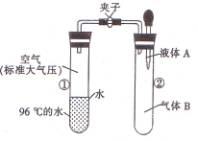
[解析]要使试管①内的水立刻沸腾,则中气体压强要显著下降,即气体B要被液体A大量消耗。[答案]C
二.填空题:(每空2分,共46分)
21.氨气电子式为 ,结构式为 ,实验室常用的制备方程式 。
答案: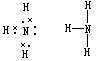
![]()
22.配平下列化学方程式并将其系数填在答题卡上:
(1): Fe + HNO3 = Fe(NO3)3 + NH4NO3 + H2O
8 30 8 3 9
(2): NO2 + NaOH = NaNO2 + NaNO3+ H2O
2 2 1 1 1
(3) SO32- + MnO4- + H+ — Mn2+ + SO42- + H2O
5 2 6 2 5 3
23.已知某非金属单质A,在常温下很稳定,一定条件下A与氢气能化合成B,能使湿润的红色石蕊试纸变蓝色,B与氧气在一定条件下能生成C,C在空气中能自然氧化生成红棕色气体D,D溶于水生成E和C,E与B化合又生成F,F既是化肥也能用作炸药,A,B,C,D均为气体。
(1)A,B,C,D,E,F的化学式分别为:
A B C D E F
(2)B→C的化学反应方程式为:
(3)D→C+E的化学反应方程式为:
(4)B+E→F的化学反应方程式为:
(1)N2 NH3 NO NO2 HNO3 NH4NO3
(2) ![]()
(3) 3NO2+H2O=2HNO3+NO
(4) NH3+HNO3=NH4NO3
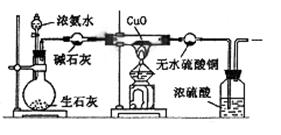
24.某课外活动小组在实验室用下图所示的装置进行实验,验证氨的某些性质并收集少量纯净氮气。试回答:
|
(1)实验前先将仪器按图连接好,然后 ,再开始实验。
(2)实验进行一段时间后,可以观察到硬质试管内黑色的CuO粉末变成 色,盛无水CuSO4的干燥管内出现 色,并在最后的出气导管处收集到纯净、干燥的N2。根据这些现象,硬质试管中的反应方程式为 ,这个反应说明氨气其有 性。
(3)烧瓶内盛有生石灰,随着浓氨水的滴入,产生氨气,氨气产生的原因是 。
(4)洗气瓶中浓硫酸的主要作用是 。
(5)在最后出气管口收集干燥、纯净的氮气,收集方法是 (填编号)
A.排气法
B.排水法
C.用塑料袋或球胆收集
(1)检查装置的气密性(2)光亮红,蓝,(3) 生石灰与水反应并放热促使氨气逸出(4)吸收尾气,保护环境(5)BC
三.计算题:(共14分,每小题7分)
25.1.某一种气态氮的氧化物250mL(标准状况),质量为0.33g,其组成里含氧53.3%,求它的化学式.NO
26.某混合物由NH4HCO3和NaCl组成,加热5.25g该混合物,经测定,产生标准状况下的NH31.12L.求该混合物中NaCl的质量分数。24.8%
高 二 年 级 化 学
一.选择题(本题包括个20小题,每小题只有一个正确答案,每小题分,共40分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
二.填空题:(每空2分,共46分)
21. , , 。
22. (共按3空计算)
(1): 、 、 、 、
(2): 、 、 、 、
(3): 、 、 、 、 、
23. (1)A B C D E F
(2)
(3)
(4)
24.(1) 。
(2) 色, 色, ,
性。
(3) 。
(4) 。
(5) (填编号)
三.计算题:(共14分,每小题7分)
25.
26.