高二化学上册月考测试题(二)
(考试时间:100分钟;满分:100分)
本试卷分第1卷和第Ⅱ卷两部分。第I卷为选择题,第Ⅱ卷为非选择题;
第Ⅰ卷 (选择题 共40分)
考生须知:
1.本卷答案必须做在答卷I、Ⅱ的相应位置上,做在试卷上无效。
2.请用钢笔或蓝、黑色圆珠笔将姓名、准考证号分别填写在答卷I、Ⅱ的相应位置上,并沿裁剪线将答卷Ⅱ裁下。
3.请用铅笔将答卷I上的准考证号和学科名称所对应的括号或方框涂黑,然后再开始答题。
4.本卷可能用到的相对原子质量数据:
H-1,C―12,N-14,O-16,Na-23,Mg-24,Al-27,S-32,C1-35.5,Fe-56,Ba-137。
一、选择题(本题有20小题,每小题2分,共40分。每小题只有1个选项符合题意,不选、多选、错选均不给分。)
1.人类未来理想的燃料是
A.煤 B.石油 C.天然气 D.氢气
2.下列物质中,属于纯净物的是
A.氨水 B.盐酸 C.液氯 D.漂粉精
3.下列物质在常温常压下为液体的是
A.甲烷 B.乙醇 C.乙烯 D.乙炔
4.常温下能用铁制容器盛放的是
A.稀硫酸 B.稀硝酸 C.浓硫酸 D.硫酸铜溶液
5.下列物质中,能发生银镜反应的是
A.乙醇 B.乙醛 C.乙酸 D.乙酸乙酯
6.下列物质的水溶液,其pH大于7的是
A.Na2CO3 B.(NH4)2SO4 C.KNO3 D.Na2SO4
7.下列物质可以由单质经化合反应直接得到的是
A.CuS B.Fe2S3 C.FeCl2 D.Al2S3
8.实验室制取下列气体时,只能用排水法收集的是
A.NH3 B.H2 C.SO2 D.NO
9.下列物质中,既有离子键又有共价键的是
A.H2O B.CaCl2 C.KOH D.C12
10.下列过程不可逆的是
A.蛋白质的盐析 B.蛋白质的变性 C.氯化铁的水解 D.醋酸的电离
11.气体甲能使湿润的红色石蕊试纸变蓝,气体乙可在空气中产生白雾,当甲与乙相遇时可能生成
A.NH4C1 B.NH4HCO3 C.(NH4)2CO3 D.(NH4)2SO4
12.下列各组性质的比较中,不正确的是
A.碱性:NaOH>Mg(OH)2 B.热稳定性:NH3>PH3
C.金属性:K>Na D.原子半径:Cl>S
13.有机物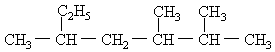 的名称正确的是
的名称正确的是
A.2,3-二甲基-5-己基己烷 B.2-乙基-4,5-二甲基己烷
C.2,3,5-三甲基庚烷 D.2,3-二甲基-5-乙基庚烷
14.往下列物质的水溶液中,分别滴加稀硫酸和氯化铝溶液,均有可能产生白色沉淀的是
A.BaCl2 B.Ba(OH)2 C.Na2CO3 D.KOH
15.进行如下实验时,所选用的试剂错误的是
A.用稀盐酸清洗做焰色反应的铂丝 B.用稀盐酸和二氧化锰制取氯气
C.用稀硝酸洗去残留在试管壁上的银镜 D.用浓硫酸吸收二氧化硫中水蒸气
16.在强酸性溶液中,可以大量共存的离子组是
A.Na+、K+、CH3COO―、Cl― B.Ba2+、Na+、CO32―、NO3―
C.Na+、Ag+、SO42―、Cl― D.Al3+ 、Fe3+、NO3―、SO42―
17.在一定条件下,发生反应:2NO2![]() N2O4,该反应达到化学平衡后,降低温度,混合物的颜色变浅,下列有关说法正确的是
N2O4,该反应达到化学平衡后,降低温度,混合物的颜色变浅,下列有关说法正确的是
A.正反应为放热反应 B.正反应为吸热反应
C.降温后NO2的浓度增大 D.降温后各物质的浓度不变
18.下列离子方程式书写正确的是
A.少量的金属钠投入水中:2Na+2H2O===2Na++2OH-+H2↑
B.铝片投入稀盐酸中:Al+6H+===Al3++3H2↑
C.氢氧化钡溶液与稀硫酸混合:Ba2++SO42-===BaSO4↓
D.氧化铝溶于烧碱溶液:Al2O3+2OH-===AlO2-+H2O
19.有关环境污染的下列说法中,不正确的是
A.环境污染主要指大气污染、水源污染、土壤污染、食品污染及噪声等
B.大气污染主要指CO、SO2、NmOn、CmHn及粉尘等
C.大气中CO2浓度增大,是造成酸雨的主要原因
D.从保护环境考虑,未来最理想的燃料是氢气
20.人造地球卫星用到一种高能电池――银锌蓄电池,其电极反应式为:
Zn+2OH―-2e―====ZnO+H2O,Ag2O+H2O+2e―====2Ag+2OH―。据此判断氧化银(Ag2O)是
A.负极,被氧化 B.正极,被还原 C.负极,被还原 D.正极,被氧化
第II卷(非选择题 共60分)
注意:1、第II卷页,请考生用蓝、黑钢笔或圆珠笔直接答在试卷上。
2、答卷前,请考生将密封线左边相应的项目填写清楚。
| 题号 | 二 | 三 | 四 | 总分 |
| 得分 |
|
|
|
|
| 得分 | 评卷人 |
|
|
|
二、填空题(本题有7小题,共38分。)
21.配平下列反应的化学方程式,并指出还原剂和氧化产物(8分)
□As2S3+□HNO3+□H2O==□H3AsO4+□H2SO4+□NO↑
还原剂________,氧化产物________、 ;
22. (4分)某有机物A,分子中含两个碳原子,现用A来制取有芳香气味的有机物F和加聚高分子化合物E,其变化如下图所示:
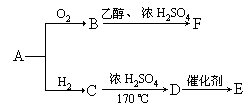
(1)写出结构简式:A________ E________,
(2)写出B→F的化学方程式________。
23.某混合物M,含有MgCl2、Al2O3,和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:(6分)
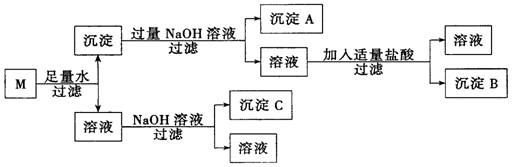
试写出沉淀A、B、C的化学式:A 、B 、C 。
24.(4分)有H、S、O、Na四种元素
(1)由两种元素组成的化合物水溶液呈酸性,它的电子式为________,它的稳定性比HCl________(强、弱)。</PGN0313.TXT/PGN>
(2)由两种元素组成一种盐,用电子式表示它的形成过程________________。
25、(6分)甲烷的分子式为 ,与氯气反应,生成物有 种,其中 是非极性分子,它的结构式是 ,常用作溶剂的是 和 。
26、(4分)原子序数为13的元素位于元素周期表中第 周期、 族,它的氧化物的化学式为 ,最高价氧化物对应的水化物的化学式为 。
27、(2分)一个5L的容器里,盛入8.0 mol某气态反应物,5min后,测得这种气态反应物还剩余6.0mol,这种反应物的化学反应速率为 mol/(L・min)
28、(4分)有机物A由碳、氢、氧三种元素组成,分子中不含碳碳不饱和键,它与烷烃B分子量相同。现将A、B在一定温度下以相同物质的量混合,取该混合物1mol,使其完全燃烧,需3.75mol氧气。则A、B可能是(写分子式)A________,B________。
| 得分 | 评卷人 |
|
|
|
三、实验题(本题有1小题,共10分)
29、为了验证木炭可以被浓硫酸氧化成二氧化碳,某学生设计了如图三个相同装置(分别加入不同试剂)进行实验,证明确有二氧化碳生成(气体发生装置省略)。试回答下列问题:
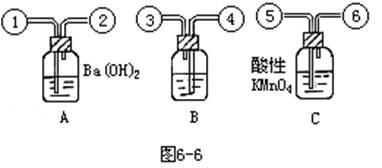
(1)装置B中应盛放的试剂是____ 溶液。(1分)
(2)三个装置之间的连接顺序是(填写导管序号):气体发生装置导管口接____,然后____接____,____接____。(5分)
(3)装置A、B、C中各有什么现象:
A中________,(2分)B中________,(2分)
| 得分 | 评卷人 |
|
|
|
四、计算题(本题有2小题,共12分。)
30.某有机物的蒸气密度是相同状况下氢气的30倍。将6.00g该有机物完全燃烧时,可生成6.72L CO2(标准状况)和7.20g H2O。该有机物能跟金属钠反应放出H2,且分子中只含有1个甲基。试通过计算,写出该有机物的结构简式。(5分)
31.用Cu与浓硫酸反应,得到SO2 的体积为 2.24L(标准状况)。试计算:
⑴被还原的H2SO4 的物质的量;(3分)
⑵把所得到的CuSO4 配制成 500 mL CuSO4 溶液,所得溶液中溶质的物质的量浓度。(4分)
参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | D | C | B | C | B | A | D | D | C | B |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | A | D | C | B | B | D | A | A | C | B |
21.3,28,4――6,9,28,As2S3,H3AsO4、H2SO4
22![]()
![]()
23. Fe2O3 AI (OH )3 Mg(OH)2
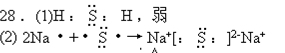
25. CH4 5 CCI4 CHCI3 CCI4
26.三 ⅢA AI2O3 AI(OH)3
27. 0.08
28 C2H4O,C3H8
29.(1)品红(2)5,6接4,3接1
(3)出现白色沉淀,不褪色,酸性KMnO4溶液褪色
30、(过程略)⑴0.1mol(3分)
⑵0.2mol/L(3分)