高二年级化学下学期第一次月考试题
2008.4.11
可能用到的相对原子质量:H 1; C 12; N 14; O 16; Na 23
说明:请将选择题答案填至答题卡中。
一、单项选择题(每题只有一个答案符合题意,共20×3=60分)
1.下列关于油脂的叙述不正确的是
A.油脂都不能使溴水褪色; B.油脂没有固定的熔沸点;
C.油脂属于酯类; D.油脂是高级脂肪酸的甘油酯。
2.下列有关葡萄糖的说法错误的是
A.葡萄糖的分子式是C6H12O6 B.葡萄糖能发生银镜反应
C.葡萄糖是人体重要的能量来源 D.葡萄糖属于高分子化合物
3.下列物质中属于醇类且能发生消去反应的是
A.CH3OH B.C6H5CH2OH
C.CH3CH(OH)CH3 D.HO―C6H4―OH
4.下列配制银氨溶液的操作中,正确的是
A.在洁净的试管中加入1~2mLAgNO3溶液,再加入过量浓氨水振荡混合
B.在洁净的试管中加入1~2mL浓氨水,再加入AgNO3溶液至过量
C.在洁净的试管中加入1~2mL稀氨水,再逐滴加入2% AgNO3溶液至过量
D.在洁净的试管中加入2% AgNO3溶液1~2mL,逐滴加入2%稀氨水至沉淀恰好溶解为止
5.下列物质中,在不同条件下可以发生氧化、消去、酯化反应的为
A.乙醇 B.乙醛 C.苯酚 D.乙酸
6.某有机物的结构简式如下图,则此有机物可发生的反应类型有
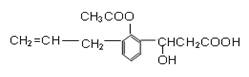 ①取代 ②加成 ③消去 ④酯化
①取代 ②加成 ③消去 ④酯化
⑤水解 ⑥氧化 ⑦中和 。
A.①②③⑤⑥ B.②③④⑤⑥
C.①②③④⑤⑥ D.①②③④⑤⑥⑦
7.某学生将一氯丙烷与NaOH溶液共热煮沸几分钟后,冷却,滴入AgNO3溶液,结果未见到白色沉淀生成,其主要原因是
A.加热时间太短 B.不应冷却后再滴入AgNO3溶液
C.加AgNO3溶液后未加稀HNO3 D.加AgNO3溶液前未加稀HNO3
8.下列有关蛋白质的叙述中,不正确的是
A. 人工合成的具有生命活性的结晶牛胰岛素,是1965年我国科学家合成的
B.蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解
C. 重金属盐能使蛋白质变性,所以误食重金属盐会中毒
D. 浓HNO3溅在皮肤上使其呈黄色,是由于浓HNO3和蛋白质发生了颜色反应
9.下列说法正确的是
A.乙烯的结构简式可以表示为CH2CH2
B.苯、乙醇和乙酸都能发生取代反应
C.苯酚具有弱酸性,属于一元弱酸
D.液化石油气和天然气的主要成分都是甲烷
10.用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是
A.18O只存在于乙酸乙酯中
B.18O存在于水、乙酸、乙醇以及乙酸乙酯中
C.18O存在于乙酸乙酯、乙醇中
D.若与丙酸反应生成的酯的相对分子质量为102
11.与 互为同分异构体且遇FeCl3溶液能呈现紫色的芳香族化合物有
A.2种 B.3种 C.4种 D.5种
12.完全燃烧相同质量的下列各烃,消耗氧气最少的是
A. CH4 B.C2H4 C.C2H2 D.C6H14
13.32克某饱和一元醇与足量的金属钠反应,得标准状况下氢气的体积为11.2L,则该醇是
A.CH3OH B.C2H5OH C.C3H7OH D.C4H9OH
14.在常压和100℃条件下,把乙醇气化为蒸气,然后和乙烯以任意比混合,其混合气体为V L,将其完全燃烧,需消耗相同条件下的氧气的体积为
A.2V L B.2.5VL C.3VL D.无法计算
15.有xL乙烯和乙炔的混合气体,完全燃烧需要相同状态下氧气yL,则混合气体中乙烯和乙炔的体积比为
A.![]() B.
B. ![]() C.
C.![]() D.
D.![]()
16.甲醛、乙酸和丙醛组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为
A.27% B.28% C.54% D.无法计算
17.某有机物的结构简式如下:若等物质的量的该有机物分别与Na、NaOH、NaHCO3恰好反应时,则消耗Na、NaOH、NaHCO3的物质的量之比是
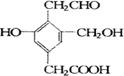 A.3:3:2
A.3:3:2
B.6:4:1
C.1:1:1
D.3:2:1
18.某种物质可能由甲酸、乙酸、甲醇和甲酸乙酯四种物质中的一种或几种组成,进行鉴定时实验记录如下:
①有银镜反应
②加入新制的Cu(OH)2悬浊液不溶解
③滴入几滴稀NaOH溶液和酚酞试液后加热,溶液呈红色,加热后溶液变无色.下列判断正确的是
A.一定有甲酸乙酯,可能有甲醇 B.四种物质都有
C.有甲酸乙酯和甲酸 D.有甲醇和甲酸
19.由乙醇制取乙二酸乙二酯时,最简便的流程需要下列哪些反应,其正确的顺序是:①取代;②加成;③氧化;④还原;⑤消去;⑥酯化;⑦中和
A.①②③⑤⑦ B.⑤②①③⑥
C.⑤②①④⑦ D.①②⑤③⑥
20.燃烧0.2mol某有机物,得标准状况下CO2的体积8.96L和10.8gH2O,由此可得出的正确结论是
A.该有机物分子式一定是C2H6或C2H6O
B.该有机物中碳与氢的原子个数比为3:1
C.该有机物中含有2个CO2和3个H2O
D.该有机物一个分子里含有2个碳原子和6个氢原子,还可能含有氧原子

![]()
化学试题答题卡 2008.4.11
一、单项选择题(共60分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
|
|
|
|
|
|
|
|
|
|
|
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
|
|
|
|
|
|
|
|
|
|
|
二、填空题(共40分)
21.(6分)填空(有机物用结构简式表示):
(1)写出乙醛与新制的氢氧化铜反应的化学方程式:
。
(2)写出C3H6O2属于酯的同分异构体的结构简式:
。
22.(12分)下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
【实验目的】制取乙酸乙酯
【实验原理】甲、乙、丙三位同学均用乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,其反应的反应方程式为:
。
【装置设计】甲、乙、丙三位同学分别设计了下列三套实验装置:
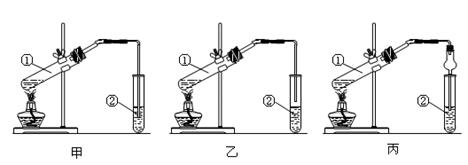
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,选择的装置是 (选填“甲”或“乙”)。
丙同学将甲装置中的玻璃管改成球形干燥管,球形干燥管起到的两个作用是:
。
【实验步骤】
(1)按你选择的装置组装仪器,在试管中先加入3 mL乙醇,并在摇动下缓缓加入2 mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸;(2)将试管固定在铁架台上;(3)在试管②中加入适量的饱和Na2CO3溶液;(4)用酒精灯对试管①加热;(5)当观察到试管②中有明显现象时停止实验。
【问题讨论】
a.步骤(1)装好实验装置,加入样品前还应检查: 。
b.从试管②中分离出乙酸乙酯的实验操作是 。
c.实验中加热试管的目的是:
①
②
23. (12分)化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下所示的反应。
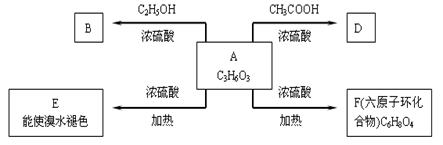
试写出:
⑴化合物的结构简式:B ,F 。
⑵化学方程式(有机物用结构简式表示):
A→E 。
⑶反应类型:A→D 。
A中含有官能团的名称为 。
⑷与A具有相同官能团的同分异构体的结构简式为: 。
![]() 24.(10分) 含C 40%、O 53.3%、H 6.7%对氢气相对密度30的有机物A,显酸性;另有相对分子质量与A相等的B,显中性。A与B在加热、浓硫酸作用下生成不溶于水且具香味的有机物C。
24.(10分) 含C 40%、O 53.3%、H 6.7%对氢气相对密度30的有机物A,显酸性;另有相对分子质量与A相等的B,显中性。A与B在加热、浓硫酸作用下生成不溶于水且具香味的有机物C。
请推断A、B、C可能的结构简式。
A的结构简式为 ;
B的结构简式为 ;
C的结构简式为 。
化学试题答案 2008.4.11
一、单项选择题(共60分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| A | D | C | D | A | D | D | B | B | C |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| B | C | A | C | C | C | D | A | B | D |
![]() 21.(6分)
21.(6分)
CH3CHO+2Cu(OH)2→CH3CO0H+2Cu2O+2H2O (2分)
HCOOC2H5;CH3COOCH3 (每个2分共4分)
![]() 22. (12分)
22. (12分)
【实验原理】CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O (2分)
【装置设计】乙 冷凝蒸汽及防倒吸 (4分)
【问题讨论】
a.装置的气密性 (2分) b.分液。 (2分)
c.①加快反应速率②及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动。 (2分)
 23. (12分)
23. (12分)
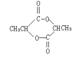
(1)(4分)B:CH3COOCH(CH3)COOH;F:
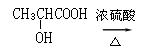 |
(2)(3分) CH2=CHCOOH+H2O
(3)(3分)酯化反应;羟基,羧基
(4)(2分)HOCH2CH2COOH
24. Mr(A)=Mr(B)=2×30=60 (每个2分,共10分)
A是CH3COOH
B是CH3CH2CH2OH或(CH3)2CHOH
C是CH3COOCH2CH2CH3 ;CH3COOCH(CH3)2