高二年级化学上册期末考试试题
化 学 试 题(模拟)
(总分:108分 考试时间:110分钟)
1.以下数据可供解题时参考
相对原子质量(原子量):H~1 C~12 N~14 O~16 Na~23 Al~27 S~32 K~39 Fe~56 Cu~64
2.把正确的答案填在答题卡上。
第一卷(选择题 共42分)
一、选择题(本题共21小题,每小题2分,共42分。每小题只有一个选项)
1.1965年在世界上第一次用人工方法合成了具有生命活力的蛋白质――结晶牛胰岛素,对蛋白质的研究作出了贡献。这个国家是
(A)中国 (B)日本 (C)美国 (D)前苏联
2.下列各项措施中无助于改善环境质量的是
(A)推行垃圾无害化与危险废弃物集中处理
(B)大力推行洁净煤技术,或改善能源结构
(C)研制与提倡使用化学农药,以减少病虫害
(D)积极推广使用无磷洗涤剂
3.下列说法正确的是
(A)淀粉和油脂是天然高分子化合物,通常都是纯净物
(B)人造丝、蚕丝都是蛋白质
(C)福尔马林主要成分是甲酸,由于可使蛋白质变性,可用于保存动物标本
(D)误食重金属盐类时,可以喝大量牛奶、蛋清或豆浆解毒
4.工业酒精中含有有毒物质,严禁用工业酒精勾兑食用酒。由于许多不法商贩利益熏心,用工业酒精制成散装白酒,使许多饮酒人中毒而双目失明甚至死亡。工业酒精中的有毒成份是
A. 甲醇 B. 乙醇 C. 乙酸 D. 乙酸乙酯
5.下列物质在一定条件下既能发生水解反应,又能发生酯化反应的是
(A)葡萄糖 (B)纤维素 (C)乙酸乙酯 (D)甲酸
6.下列说法错误的是
A.石油含有C5一C11的烷烃,可以通过石油的分馏得汽油
B.含C18以上烷烃的重油经过催化裂化可以得到汽油
C.煤是由有机物和无机物组成的复杂混合物
D.煤含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来
7.今年3月11日杭甬高速公路萧山路段一辆运送化学物品的槽罐车侧翻,罐内15t苯泄入路边300m长的水渠,造成严重危险,许多新闻媒体进行了连续报道,以下报道中有科学性错误的是
A.由于大量苯溶入水中渗入土壤,会对周边农田、水源造成严重污染
B.由于苯是一种易挥发、易燃的物质,周围地区如果有一个火星就可能引起爆炸
C.可以采取抽吸水渠中上层液体的办法,达到清除泄漏物的目的
D.处理事故时,由于事故发生地周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会产生大量的黑烟扩大污染,所以该办法未被采纳
8.下列物质不属于糖类化合物,但与葡萄糖最简式相同,且能发生银镜反应的是
(A)乙醛 (B)甲酸 (C)甲酸甲酯 (D)甲酸钠
9.下列物质是常见的食品添加剂,但使用时必须严格限制用量的是
(A)NaNO2 (B)食盐 (C)蔗糖 (D)味精
10.下列物质不能使溴水褪色的是
(A)NaOH溶液 (B)油酸甘油酯 (C)苯酚 (D)乙烷
11.下列各种物质的结构简式正确的是
A. 乙烷 CH3CH3 B. 乙烯CH2CH2 C. 乙醇C2H6O D. 甲醛 CHOH
12.下列化学式只能表示一种物质的是
A. C2H6O B. C3H6O C. C2H5Br D. C3H6NO2
13.扑热息痛是一种优良的解热镇痛药,其结构为: 它可能具有的化学性质是
A.不与氢氧化钠溶液反应 B.能与浓溴水发生取代反应
C.不能被氧化 D.遇三氯化铁溶液不呈现紫色
![]() 14.甲烷分子中的4个氢原子都可以被取代。若甲烷分子中的4个氢原子分别被苯基和氯原子取代,可得到右图所示结构,对该分子的描述正确的是
14.甲烷分子中的4个氢原子都可以被取代。若甲烷分子中的4个氢原子分别被苯基和氯原子取代,可得到右图所示结构,对该分子的描述正确的是
A.该分子的所有同分异构体中一定同时含有两个![]()
B.该分子中所有碳原子可能都在同一平面上
C.该分子属于非极性分子
D.该化合物属芳香烃类物质
15.燃烧0.2 mol某有机物,得到0.4mol CO2和0.6molH2O,由此可得出的结论是
A. 该有机物含有2个碳原子和6个氢原子
B. 该有机物中碳元素和氢元素的原子个数比为1:3
C. 该有机物中含有2个CO2和3个H2O
D. 该有机物的一个分子里含有2个碳原子和6个氢原子,还可能含有氧原子
16.对有机物: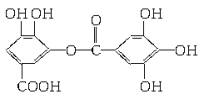 下列叙述不正确的是
下列叙述不正确的是
A.常温下,与Na2CO3溶液反应放出CO2
B.能发生碱性水解,1 mol该有机物完全水解应消耗8 mol NaOH
C.与稀H2SO4共热,生成两种有机物
D.该有机物的分子式为C14H10O9
17.下列石油和煤的炼制和加工过程中,不属于化学变化的是
A. 分馏 B. 干馏 C. 裂化 D. 裂解
18.ag甲醛、bg乙醛、cg丙醛组成的混合物中氢元素的质量分数为9%,则该混合物中氧元素的质量分数为
(A)37% (B)16% (C)6% (D)无法计算
19.下列实验中必须用到温度计,且温度计要插入液面以下的是
(A)实验室制乙烯 (B)蒸馏石油
(C)乙醛的银镜反应 (D)葡萄糖与新制Cu(OH)2反应
20.鉴别苯、苯酚溶液、己烯、KI淀粉溶液、AgNO3溶液等五种无色溶液的一种试剂
(A)KMnO4酸性溶液 (B)FeCl3溶液 (C)溴水 (D)金属钠
21. 由乙醇制取乙二酸乙二酯,最简便的流程途径,经下列哪些反应,其顺序正确的是
①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应 ⑦中和反应 ⑧缩聚反应
A. ⑤②①③⑥ B. ①②③⑤⑦ C. ⑤②①④⑧ D. ①②⑤③⑥
第二卷(非选择题 共66分)(选择题每空2分,计算8分)
22.烯烃的通式是_____________________,请写出乙烯的结构式__________________、乙炔的电子式_________________,请判断乙烯分子是(填极性或非极性)___________分子。
[解]22\CnH2n 非极性
23.完成下列化学方程式或离子方程式,并指明反应类型
(1)苯酚与NaOH溶液反应(写离子方程式)_______________________________ 反应类型______________
(2)硬脂酸甘油酯与NaOH溶液共热_____________________________________ 反应类型______________
(3)![]() 加入NaHCO3溶液中______________________________________ 反应类型______________
加入NaHCO3溶液中______________________________________ 反应类型______________
24.以前城市居民所使用的燃料主要是管道煤气,“西气东输”后,天然气开始作为民用燃料。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4。它们的燃烧反应如下:
2CO+O2![]() 2CO2 2H2+O2
2CO2 2H2+O2![]() 2H2O CH4+2O2
2H2O CH4+2O2![]() CO2+2H2O
CO2+2H2O
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是
。因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是 进风口(填增大或减小),如不作改进可能产生的不良结果是
管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:
| 乙烷 | 丙烷 | 丁烷 | |
| 熔点(℃) | -183.3 | -189.7 | -138.4 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 |
试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是 。
[解]24.(8分)天然气(2分); 增大(2分);不能充分燃烧,生成有毒的CO(2分);
丁烷遇冷凝结为液体使管道内气流不畅(2分)。
25.为测定某卤代烃分子中所含有的卤原子的数目和种类,可按下列步骤进行实验:① 量取该卤代烃液体11.4 mL;② 加入适量氢氧化钠溶液,煮沸至液体不分层;③ 冷却后加入稀硝酸酸化;④ 加入硝酸银溶液至沉淀完全;⑤ 过滤,洗涤沉淀并干燥;⑥ 称取干燥后的沉淀的质量。
回答下列问题:
(1)加入氢氧化钠溶液的目的是____________________________________
(2)加入过量硝酸银溶液的目的是___________________________________
(3)若加入硝酸银溶液时产生的沉淀为浅黄色,则此卤代烃中的卤原子是_____________
26.1,2―二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18g/cm3,沸点131.4℃,熔点9.79℃,易溶于醇、醚、丙酮等有机溶剂,在实验中可以用下图所示装置制备1,2―二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。
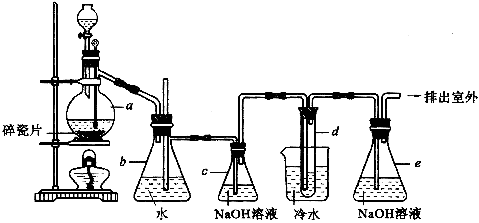
填写以下空白。
填写下列空白:
(1)写出本题中制备1,2―二溴乙烷的两个化学方程式
, 。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象________。
(3)容器c中NaOH溶液的作用是__________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓H2SO4混合液的量,比正常情况超过许多。如果装置的气密性没有问题,试分析其可能的原因。
[解]
(1)CH3CH2OH
![]() CH2=CH2↑+H2O、H2C=CH2+Br2→CH2Br―CH2Br
CH2=CH2↑+H2O、H2C=CH2+Br2→CH2Br―CH2Br
(2)b中水面会下降,玻璃管中的水面会上升,甚至溢出
(3)除去乙烯中带出的酸性气体(SO2、CO2等)
(4)①乙烯反应速度过快;②实验过程中乙烯和浓H2SO4的混合液没有迅速达到170℃(或写“控温不当”)。
27. 化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间产体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图示的反应。
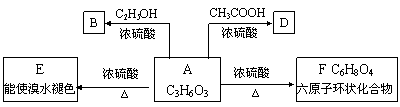 |
试写出:(1) 化合物的结构简式
A____________________ B____________________ D____________________
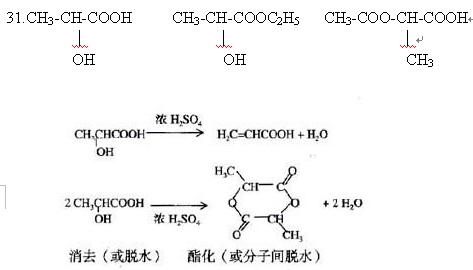
(2) 下列反应的化学方程式,并注明反应的基本类型
![]() A
E_____________________________反应基本类型________________
A
E_____________________________反应基本类型________________
![]() A
F________________________________反应基本类型________________
A
F________________________________反应基本类型________________
[解]
28.计算题:
A、B、C三种烃的衍所含元素的质量分数都为C:40%、H:6.7%、O:53.3%。又知在标准状况下,A蒸气的密度为1.34g/L;在同温同压下,B、C的蒸气密度都是A的2倍,且A能发生银镜反应;B显酸性;C显中性,C能与氢氧化钠溶液反应生成醇和盐。
(1)通过计算,求A、B、C的分子式
(2)根据A、B、C的性质,确定它们的结构,并写出它们的结构简式
[解]ACH2O;B和C:C2H4O2