�߶���ѧ��һѧ�ڻ�ѧ�����������Ծ�
һ������ѡ���⣺ÿ����ֻ��һ��ѡ���Ƿ���Ҫ������28С�⣬ÿС��2�֣���56�֣�
1��2006��4�£������ȱ����������������ǿ���ɳ����Ϯ�������±����ȡ����Ǿ����ƽ�ס���������ȾΪ�弶�ض���Ⱦ������Ϊ��س��п�����Ⱦ����Ҫ��Ⱦ���ǡ��� ��������
A������������B����������������C��������̼�������� D�������������
2�����и������ʻ������У�����û���������ϵ���ǡ������������������� ��������
A������β��--------�⻯ѧ��Ⱦ-------���Ժ�����������
B������ϴ�·�--------ˮ�帻Ӫ����--------ˮ�������������
C���˿�����--------������CO2Ũ������--------����ЧӦ
D��������--------�����ն�--------Ƥ������������
3��������Ŀ����ˮ�¡��ڵ����ʡ���PH���ܹ�����������ܽ�����DO������ѧ��������COD������������������BOD������һЩ�ж��к����ʵ�Ũ�ȵȣ�������������ˮ��������Ҫ������Ŀ�ǡ����������������������� ����������������������������������������
A.�ۢܢݢޢߢࡡ�� B.�ݢޢߢࡡ���� C.�ܢݢޢߢࡡ�� D.�٢ڢۢܢݢޢߢ�
4�����Ž���װ�β��Ͻ�����ռ�ͥ��ijЩװ�β��õľ�������װ�β����ͷų�������Ⱦ��Ũ�ȹ��ߣ�Ӱ�����彡������Щ��Ⱦ��������ǡ������������������������� ��������
A.һ����̼��������B.�������� C.������������D.��ȩ�����Ȼӷ����л���
5���������ʿ���������ˮ��ԭˮ�����������ֲ�����ɻ�����Ⱦ���ǡ��������� ��������
A��Һ�ȡ��������������� B�������������� C���ƾ������������� D������
6���й�Ӳˮ��˵��������ȷ���ǡ����������������������������������������� ��������
A�����н϶�������ӵ�ˮ����Ӳˮ
B�����н϶�ơ�þ���ӵ�ˮ����Ӳˮ
C��Ӳˮ����������������㣬����Ӳˮϴ�·�Ҫ����ϴ�·ۣ���Ӳˮ�Ĺ�¯Ҫ����ȼ���ҿ�����ɹ�¯��ը�ȵ�
D�������п��Բ��ò�ͬ�ķ�����Ӳˮ�����������ӽ�������
7�����м�ͥ�������ʺ����öѷʷ��������ǡ������������������������������� ��������
A �ƾɵ����������B�Ϲ��ǡ����� C �ɱ�ֽ�������� D������ƿ
8�������������������IJ�����ߣ��Էϵ�ر�����м��д��������ⱻ�ᵽ�����ճ̣�����Ҫԭ������������������������������������������������������ ��������
A���õ����ǵĽ������ϡ���
B ��ֹ����й����Ӻ�Ǧ���ؽ������Ӷ����غ�ˮԴ����Ⱦ��
C ��ʹ�������©�ĵ��Һ��ʴ������Ʒ
D �������е�ʯī���
9��Ϊ��֤��øϴ�·�ϴ��Ч����Ӧע�⡡������������������������ �������� ��������
A��ʹ�÷�ˮ�ȳ���ϴ�·ۡ������������� B���ú��Ƚϸߵ�����ˮ
C��������ϴ�Ӽ����ʹ�á������������� D������ʱ��ˮ���ܽ�ϴ�·�
10������������������������ˮ��ɱ���������ǡ��������������������������� ��������
A Ư�ۡ��������� B �������ȡ����� C�� ��ȩ��������D ����
11�����߲����������У���������ũҩ���β��溦�����й�ר�ҽ��ܣ��ü�����Һ����ˮ���ݣ���ʹ�������߲��ϵ�ũҩ�Ķ��Խ��͡���ˣ��������߲���ʳ��ǰ����ô���ϡ��Һ����ˮ����һ��ʱ�䡣���Ƕ��߲��ϲ���ũҩ���ʵ��Ʋ����������ǡ������� ��������
A������ũҩһ�㶼��һ����ˮ���ԡ���������
B��ũҩ����Һ��pHһ������7
C������ũҩ�ڼ�����Һ�и����ܻ�����������ʷ�Ӧ
D��ũҩ����Һ����ʹ��ɫʯ����Һ���ɫ
12��������������Ԫ����ָ�ܺ����������֮һ���������ܺͲ�����������ǧ��֮һ�Ķ�ʮ����Ԫ�أ���ЩԪ�ض�����������л�ͽ���������Ҫ���á�����Ԫ�ؿ϶���������������Ԫ�ص��ǡ������������������������������������������������������� ��������
�����ڣ�������� �£��ȡ����������������� �ã���e�������������� �ģ���u
13������˵���в���ȷ����
A������ȱ�⣬��ͨ��ʳ�üӵ��β���
B��ȱ����ƶѪ����ͨ��ʳ����ǿ������Ԥ��
C��Ϊ�˷�ֹȣ�ݣ����˶�Ҫʹ�ú�������
D����ͯȱп�ɵ������������������ֿ����ʳ������
14��������С����ҽԺ����Ѫ�����鱨�浥�IJ������ݣ�С��Ӧ��ע�ⲹ�����Ԫ���ǣ�������
| No | ��Ŀ | ��� | ������Χ�ο�ֵ | ��λ |
| 1 | ��ϸ������ | 2.3 | 3.5��5 | 1��1012/L |
| 2 | Ѫ�쵰�� | 75 | 110��150 | g/L |
| 3 | ѪС����� | 205.5 | 100��300 | 109/L |
A���������������������� B������������������� C�������������������� D����
15�����й������ࡢ�����ʡ���֬����ά�ص�˵���У���ȷ���ǡ������������������� �� ��������
A�����ǵ�����ж���C��H��O��N��Ԫ��
B����һ�������£����Ƕ��ܷ���ˮ�ⷴӦ
C��������Ҫ�Ķ�ʮ���ְ����ᶼ����ͨ�����������ϳ�
D����֬���Ǹ�֬����ĸ���������һ�ָ�����Ӫ����
16����ͼ��ʾ����һ��ƻ����Ƭ�Ϸֱ����1�ε�ˮ��������Һ����ɫ�仯��ͼ��ʾ��������Щʵ������������ƶ���ȷ���ǡ����� �������������������������������� ��������
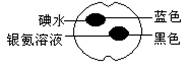 A������ƻ���к���֬��
A������ƻ���к���֬��
B������ƻ���в�������
C������ƻ���к��л�ԭ�Ե���
D������ƻ���в�����ԭ�Ե���
17����������������֬���ǡ��������������������������������������������� ��������
����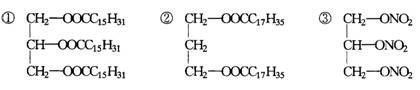
���������͡��ݻ����͡���ʯ��
����A���٢ڡ������� B���ܢݡ���������C���٢ݡ����� D���٢�
18�����в����ڵ����ʱ��Ե��ǡ����������������������������������������� ��������
�� A������������Һ�����ʳ��ʹ֮����ǡ��� B������ע��ǰ��ҽ�������ƾ���������
�� C������������Һ�м���Ũ�������ֳ����� D���ø������ֽ��ݶ���걾
19������ά����C������˵���в���ȷ���ǡ������������������������������� ��������
A��������ˮ,ˮ��Һ������ ����B��ά����CҲ��Ϊ����Ѫ��,������������Ҫ����
C����ˮ��Һ�����ױ���ԭ�� �� D�����ʵ�ˮ�����߲��к��д���ά����C
20������ʳƷ���Ӽ�������Ӧ������ǡ��������������������������������� ��������
A����ζ�������������ơ������������� ������ B�������������������ơ���
 C�����ɼ�����̼�����ơ�������������
������ D����ɫ������Ҷ����
C�����ɼ�����̼�����ơ�������������
������ D����ɫ������Ҷ����
21���ҹ��涨���������۵�ʳƷ��װ��ǩ���ϱ��ϣ�ʳƷ���Ӽ�Ӧʹ�ù涨�IJ�Ʒ���ƻ��������ƣ�������ζ��������������ɫ��Ӧע������ͼ��ǩע�������Ӽ���������ɫ�����ǡ����������� ��������
�������ᡡ��������������ɽ����ء��������� ����ζ��
�ܲ����㾫���������� �����ʻơ��������������������
A���٢ڢݡ��� ��������B���ڢݢޡ���������C���ݢޡ�����������������D���ۢ�
22�����������߷����Բ��ֻ�ѧ֪ʶ���й��ɵ������У������������ǡ������� ��������
A�����ʵ���������;������
�ǰ���ҩ��������ϸ���ϳɺ���D�D���Ʒ��ס���Ĥ�ס���·��Ⱦ����������Ⱦ
��������к�-----θ�����IJ��˷��ú�������þ��ҩ��
B������������
���ơ���ɫ��Ⱦ��������ֹʹ������������Ʒ ��
��ֹˮ����Ⱦ�����ᳫʹ������ϴ�·�
C��������ȫ��ʶ��
���üپ��ж��D�D�ɼ״����𡡡�����������
ʳ�ü����ж��D�D��������������
D�������е�һЩ������
��ȥ�·��ϵ����ۨD�D��������ϴ�ӡ���
ʹúȼ�ո����D�D������ú������Ӵ����
23�����й���ҩ���ʹ��˵����ȷ���ǡ����������������������������������� ��������
A������ҩ���ֶ��������밴ҽ����ҩ��˵����ʹ��ҩ�����ҩ�ﲻ����Ӧ
B��ʹ����ù��ʱ��ֱ�Ӿ���ע����Բ��ý���Ƥ����������
C�����ڴ���ʹ�ð�˾ƥ�ֿ�Ԥ��������û�и�����
D�����ڱ�ǡ�OTC����ҩ�������ҽ��ָ����ʹ��
24����ù����������λ��ѧ�ҷ��ֵġ������� ������������������������������ ��������
A.Ǯ�������������� B.��������������C.ŵ�������������� D.�¶���
25����˾ƥ����������ˮ���ᣬ�ƶ�����Ӧ���е����ʡ��������������������� ��������
A.��NaOH��Һ��Ӧ B.������Ʒ�Ӧ��C.�����ᷢ��������Ӧ��D.���Ҵ�����������Ӧ
26���������ֳ�������θ��ҩƷ�ı�ǩ��

������������
�١������������������������ڡ�����������������������
ҩƷ�����������ʾ����к�θ����������ᣬ���й�������ҩƬ�к�θ��������Ƚϣ���ȷ����(���ԭ��������H: 1;��C: 12 ;��O: 16 ;��Mg: 24 )�������������������� ��������
A���ڣ��ۣ��١����� B���٣��ڣ��ۡ�����C���ۣ��ڣ��١��� D���٣��ڣ���
![]() 27��������������������������Դ������������ʶ�������ķ����ռ���ʵ�������������Ҫ��ʩ��ij����������������ͼ��ʾ�ı�־������������ж����������ǣ�������
27��������������������������Դ������������ʶ�������ķ����ռ���ʵ�������������Ҫ��ʩ��ij����������������ͼ��ʾ�ı�־������������ж����������ǣ�������
A��Σ���������������������������������������� ������ B���ɻ�����
C�������������������������������������������������D����������
28���ҹ�Ӯ��2008���29���ļ����˻�ľٰ�Ȩ��Ϊ������չ��һ���µ�����ijУͬѧ������н��飺�ٿ�������Դ�����ٻ�ʯȼ�ϵ�ȼ�գ��ڿ�����������أ��۷���������������ᳫʹ��һ���Է������ϲ;ߺ����ϴ������ᳫʹ�����������ٲͽ�ֽ��ʹ�ã����ᳫ��ʹ�ú���ϴ�·ۡ�����Ϊ���Բ��ɵ��ǡ������������� ��������
A���٢ڢۢܢޡ�����������B���ڢۢܢݢޡ�����������C���٢ڢۢݢޡ�����������D��ȫ��
��ѧ�����������Ծ����
һ������ѡ���⣺ÿ����ֻ��һ��ѡ���Ƿ���Ҫ������28С�⣬ÿС��2�֣���56�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| �� | ||||||||||||||
| ��� | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 |
| �� |
��������⣬ÿ�ո�1�֣���39 �֡�
29��A��ά����C�Ľṹ��ʽ��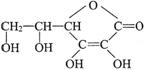 �����ķ���ʽ��______________���������ܷ��λ�Ѫ�����ֳ�Ϊ_________________����ά����C��Һ�е�����ɫʯ����Һ����Һ��ɫ��죬˵��ά����C��Һ����__________�ԣ���ά����C��Һ�е���������ɫ�ĺ��е��۵ĵ�ˮ���ɹ۲쵽��������______________��˵��ά����C����____________�ԡ�
�����ķ���ʽ��______________���������ܷ��λ�Ѫ�����ֳ�Ϊ_________________����ά����C��Һ�е�����ɫʯ����Һ����Һ��ɫ��죬˵��ά����C��Һ����__________�ԣ���ά����C��Һ�е���������ɫ�ĺ��е��۵ĵ�ˮ���ɹ۲쵽��������______________��˵��ά����C����____________�ԡ�
30����������ˮƽ����ߣ�����Խ��Խ��ע�����Ľ�����������̽�ֻ�ѧ���������彡�����й����⣺
��1�����������ϰ�����Ӫ��ȱ��֢������Ҫ��������ȡ_________��������ʡ�����֬������ά���ء�����������ġ�
��2����Ԫ�������彡��������أ�����ʳ�ṹ������������ij����Ԫ�ز��㣬�ͻ�����ijЩ�������������İ�С��������������������ȱ________��_________Ԫ���Ǻϳɼ�״�ټ��ص���Ҫԭ�ϣ�������Ԫ��������������ܻᵼ��_________��
��3������ҩ�������ܶ࣬����Ч�ɷ�һ�㶼��̼�����ơ�̼��ơ�̼��þ������������������þ�Ȼ�ѧ���ʡ�
�ٿ���ҩ����п������õ�ԭ������������������������������������ ��
��ijƷ�ƿ���ҩ����Ҫ�ɷ������¡�̼��þ���������������ۡ�
д���ÿ���ҩ���ӹ�Чʱ�Ļ�ѧ����ʽ����ʽ��
���������������������������������� ������������������������������������ ��
�۵����ڿ���ҩ����������ճ�ϼ���������������ø�Ĵ������·���ˮ�ⷴӦ������ת��Ϊ��д����ʽ�������������� ��
31����1����ʳƷ�м��뷢ɫ��������ʳƷ�е�ijЩ�ɷַ�����ѧ��Ӧ��ʹ��Ʒ�������õ�ɫ�������������Ƽӹ������У����������κ��������Σ�ʹ���ƺõ�������Ʒ�������ĺ�ɫ���йط�Ӧ������������ӽ������࣬���������ܲ��ȶ��������ᣬ������ֽ��������ᡢһ��������ˮ��һ�������뼡�쵰�ף�Mb����Ӧ��������ɫ�����������쵰�ף�MbNO������д����ط�Ӧ�Ļ�ѧ����ʽ�����ӷ���ʽ����д��һ�����֣�
������������������������������������������������������������������������������������������������������������������������������������������������������������������������������������ ����
��2������������һ�ֳ���������������2003�꿹�����ǵ䡱�Ĺ����У������˾�����á���������ķ��ӹ��ɱ������һ����ԭ�ӣ�����������Ĺ���������O��O���������ֳ�ǿ�������ԡ����ᣨ�����ᣩ�Ĵ������£�����ɱ�������������Ϊ�������ᣬ�˹����ǿ��淴Ӧ����д���÷�Ӧ�Ļ�ѧ����ʽ������������������������������������������������������������������������������������������
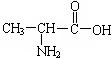
��3��һ�ֶ��ĵĽṹ��ʽΪ��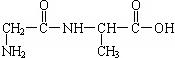 ���ϳ����ֶ��ĵİ�������
���ϳ����ֶ��ĵİ�������
���������������������� �������� �� ��������������������������������������
��4������ˮ���ᣨ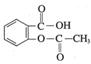 ��������Ϊ��˾ƥ�֣��dz��õĽ�����ʹҩ������ˮ�ܻ�����ˮ������ˮ���ᣬ������ˮ����ķ�Ӧ�ɱ�ʾΪ������������
���� ���������� ��
��������Ϊ��˾ƥ�֣��dz��õĽ�����ʹҩ������ˮ�ܻ�����ˮ������ˮ���ᣬ������ˮ����ķ�Ӧ�ɱ�ʾΪ������������
���� ���������� ��
32������Ⱦ���������ࣺ_________ ______�������������������� ������������������
33�����dz���__________ ___����ʾ����������������Ⱦָ���Ǹ��ݿ�����___������____���� _______����___����_____������������ __����Ⱦ���Ũ�ȼ����������ֵ��
34�����в�֢������ȱ����һ��ά��������ģ�
(1) ҹä֢��____________���������� __��(2) ���Ͳ���______�������� _________
(3) �������á������ɶ���_______________ (4) ��Ѫ����____________________________
35����1������β�����������ࡢCO��SO2��NO�����ʣ��dz��е���ȾԴ�������ķ���֮һ������������������װһ������ת���������ò����ٺϽ����������������ص���ʹCO��NO��Ӧ�����������壬����ʹ������ȼ�ռ�SO2��ת����
��д��CO��NO��Ӧ�Ļ�ѧ����ʽ������������������������������������ ��
�ڡ���ת��������ȱ������һ���̶�������˿�������ȣ���ԭ������������
�������� ������������������������������������������������������������������ ��
�ۿ��Ƴ��п�����ȾԴ�ķ����������������������� ����ѡ��
A�� ��������Դ��B�� ʹ�õ綯�� C�� ֲ�����֡��� D�������Ϻ������
��2�� ���о����⻯ѧ�������к������к��г��������γɹ�������������йأ��������ʵ���ϰ�����������Ӧ����NO2![]() NO+O����2NO+O2=2NO2����O2+O=O3�����ܷ�Ӧ�ɱ�ʾΪ����������������������
��NO2����������������������
���������á�
NO+O����2NO+O2=2NO2����O2+O=O3�����ܷ�Ӧ�ɱ�ʾΪ����������������������
��NO2����������������������
���������á�
36����������һ����Է�Ϊ������������ �������������� ������������������ ��
���������
37����5�֣�ú�к�������Բ���ʯ��ʯ�����д�����д���йط�Ӧ�ķ���ʽ����֪ij��ú�ĺ�����Ϊ1%���ڽ���������ʱ100t��ú����Ҫ������ٶֵ�ʯ��ʯ����Ӧ�ɵ�����ƶ��ٶ�? ���ԭ��������Ca-40��C-12��O-16��S-32
��
һ������ѡ���⣺ÿ����ֻ��һ��ѡ���Ƿ���Ҫ������28С�⣬ÿС��2�֣���56�֣�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| �� | D | C | D | D | B | A | B | B | D | C | B | B | C | C |
| ��� | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 |
| �� | D | C | C | A | C | A | C | B | A | B | C | C | B | C |
��������⣬ÿһ�ո�1�֣���39 �֡�
29. A��C6H8O6���� ����Ѫ�ᡡ�����ᡡ������Һ��ɫ��ȥ��������ԭ
30����1�������� ��2���ơ��⡢ȱ����ƶѪ��3��������Ч�ɷֶ����к�θ���������ᡡ
�Ƣ�MgCO3+2H+===Mg2++CO2��+H2O��Al(OH)3+3H+===Al3+ +3H2O����C6H12O6
31.��1��H+ + NO2-- = HNO2�� ��3HNO2 = HNO3 + 2NO�� + H2O ��Mb + NO = MbNO
(2) CH3COOH+H2O2��CH3COOOH+H2O��
(3) 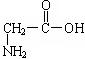 ��
��
��4��
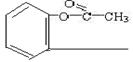 COOH +H2O��������
COOH +H2O�������� ![]() +
+![]() H
H
32. ֲ��Ⱦ�������ϳ�Ⱦ��������Ⱦ��������������
33. ������Ⱦָ����API������������(SO2) ������������NO2��������������PM10��
34. ����A������D������C�� ����C
35. ��1�� �� 2CO+2NO=CO2+N2���� �ڡ�SO2��SO3��H2SO4������AB
��2��3O2 =2O3 ��������
36. �л�������Σ�շ���ɻ���������
37. CaCO3==CaO+CO2 ��1�֣� CaO+SO2==CaSO3����1�֣� 2CaSO3+O2==2CaSO4��1�֣�
̼��ƣ� M=3.125t ��1�֣��� ����ơ�M =4.25t��1�֣�