�߶���ѧ�������������
��ѧ���ޣ�ѡ��5����
�����Ծ��֢�����������100�֡�����ʱ��90���ӣ�
���ԭ��������H:1��C:12��O:16�� Cu:64
�ڢ����ѡ����48�֣�
һ��ѡ����:�������16С�⣬ÿС��3�֣���48�֣�ÿС��ֻ��һ��ѡ��������⣩
1��
�ҹ��ġ�������š����˷ɴ��ѷ���ɹ������϶�̽�¹�������ʽ�������ݿ�ѧ��Ԥ�⣬�����������������������ֵ�![]() He��ÿ�ٶ�
He��ÿ�ٶ�![]() He�˾۱����ͷų��������൱��Ŀǰ����һ�����ĵ��������ڵ����ϣ���Ԫ����Ҫ��
He�˾۱����ͷų��������൱��Ŀǰ����һ�����ĵ��������ڵ����ϣ���Ԫ����Ҫ��![]() He����ʽ���ڡ�����˵������ȷ����
He����ʽ���ڡ�����˵������ȷ����
A��![]() Heԭ�Ӻ��ں���4�����ӡ��������������������������� B��
Heԭ�Ӻ��ں���4�����ӡ��������������������������� B��![]() He��
He��![]() He��Ϊͬλ��
He��Ϊͬλ��
C��![]() Heԭ�Ӻ��ں���3������
Heԭ�Ӻ��ں���3������
D��![]() He������������Ϊ2������
He������������Ϊ2������![]() He���н�ǿ�Ľ�����
He���н�ǿ�Ľ�����
2��������ʵ������У��д������
A����Һʱ����Һ©���²�Һ����¿ڷų����ϲ�Һ����Ͽڵ���
B������ʱ���¶ȼ�ˮ����Ӧ��û��Һ����
C������ʱ����ȴˮӦ�������ܵ��¿�ͨ�룬�Ͽ�����
D��������FeCl3������Һ����200ml ��ˮ�����һ�����ȡFe(OH)3����
3��
�����Լ�������������Fe2+��Fe3+����
A��KSCN�������������������������� B��FeCl3 ����������������������������C��H2SO4��������������������D��NH4Cl
4��
�������ʵ���Һ��ͨ����CO2���壬��������ɫ�������ǡ�
A��AlCl3����������������������B��C6H5O
Na�������������������������������������������� C��NaAlO2������������������ D��Na2SiO3
5��
���б仯�У�������ˮ�ⷴӦ����
A������ͷ����������������ζ
B��������Һ��ϡ���Ṳ��һ��ʱ��μӵ�ˮ������ɫ
C����Ϻ���ù��ò������ŵ��ȳ���ζ������������D����֬������������Һ�����Ƶ÷���
6��
����Ϊͬ���칹������ʲ�����
A��������ͬ����Է���������������������������������B��������ͬ���ۡ��е���ܶ�
C��������ͬ�ķ���ʽ������������������������������������D��������ͬ�����Ԫ��
7��
�������ʾ���Ư�����ã���Ư��ԭ����ͬ����
�ٴ����ᡡ�ڳ����� �۶������� �ܻ���̿
A���٢ڡ���������������������B���٢ۡ��������������������� C���ۢܡ���������������������D���٢ڢ�
8��
�����л�����������е�ԭ��һ������ͬһƽ�����
A��CH3CH��CH2������������������������������������������������������������������������������������������B��CH3CH2CH��CH2
C��CH2��CH��CH��CH2������������������������������������������������������������������ D��C6H5��C��CH
9��
������������������Ļ�����Ʒ���������ijЩ���ƻ�������ġ����ﰺ����Ʒ�������յ���������䶳����е�����������ж϶�������ĺ˴Ź��������ϵ�����������
A��4�������������� ����B��3��������������������C��2������������������D��1��
10����
�����л��������һ�ȴ�����3�ֵ���
A���� ![]() �� ����������������������������B��
�� ����������������������������B��![]()
C�� 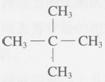 ������������������������������������D��
������������������������������������D��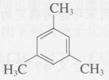
11����
2004��ŵ������ѧ��������λ��ɫ�к�һλ������ѧ�ң��Ա������Ƿ����ˡ����ص����µĵ����ʽ��⡱�����ر���Ϊ������֮�ǡ�������һ��76����������ɵĶ��ģ����õĵ����ʾͱ���������ճ���������͵�ϸ���ڵġ�����������������ø�����±��г�7~9��������Ķ��ġ��йط��ص�˵������ȷ����
A�����������µĵ����������������۷�Ӧ���� B�����ؼ������ᷴӦҲ����Ӧ
C�����ط����к���![]() �ṹ����������������D�����ز������л��߷��ӻ�������
�ṹ����������������D�����ز������л��߷��ӻ�������
12���� ijͬѧ������Ͳ��Һ��������Ϊm mL�������������Ӷ���Ϊn mL������Һ�����
A����(m��n) mL���������������������������������������� B������(m��n)mL
C������(m��n)mL������������������������������������������������ D�����ڻ����(m��n)mL
13����
2005��11��13�գ���ʯ�ͼ���ʯ����˾˫����������ը���ų���Լ100�ֱ���������C6H5NH2���������������ױ�����Ⱦ�����ˮ�������ɻ���������ɻ���ˮ�������Ⱦ��������ȫ��ͣˮ���졣����˵������ȷ����
A���������ױ����������������ӷ���������ɿ�����Ⱦ
B�������Ը��������Һ���Լ��𱽡����ױ���������
C���������ױ��������������ڷ��������������� D���������ױ���������������������
14����
1��5�����ȩ�����GA����һ����Ҫ�ı���ֱ����Ԫȩ��2%��GA��Һ���й��ס���Ч���̼�����ʴ���ص㣬�������С������ߡ������ȼ��������õķ������á�����������Ϣ���ж�����˵���в���ȷ����
A�����ȩ����ʽΪC5H8O2�����ϴ˷���ʽ�Ķ�Ԫȩ��4��
B�����ȩ���ڼ��������º����Ʊ���������ͭ��Һ��Ӧ
C�����ȩ����ʹKMnO4������Һ��ɫ
D��2%��GA��Һ��ʹ�����ʱ��ԣ���������ɱ������
15���� ����һƿA��B�Ļ��Һ����֪A��B��ijЩ�������£�
| ���� | ����ʽ | �۵�� | �е�� | �ܶ�g•���-3 | ˮ���� |
| A | ��3��6��2 | -98 | 57.5 | 0.93 | ���� |
| B | ��4��8��2 | -84 | 77 | 0.90 | ���� |
�ɴˣ�����A��B����ѷ�����
������ȡ�������� ���� �£��������������� �ã��������� �ģ���Һ
16����
����ʵ���ܻ�óɹ�����
A������ˮ���𱽡��Ҵ�������ϩ������������������ B����Ũ��ˮ��Ȼ����˳�ȥ����������ϩ
C��������ˮ�����ۻ���Ƴ��屽������������������ D�����÷�Һ©������������Ͷ��ױ�
17����
�����йؼױ���ʵ����ʵ�У���˵�������Ա���������Ӱ�����
A���ױ��ܷ�Ӧ�����������ױ����� ��������������B���ױ���ʹ���Ը��������Һ��ɫ
C���ױ�ȼ�ղ�����Ũ�̵Ļ��桡�� ��������������D��1 mol�ױ���3 molH2�����ӳɷ�Ӧ
18����
�������ӷ���ʽ��ȷ����
A��Al��H2SO4��Ӧ��������Al + 2 H+ ���� Al3+ + H2��
B��Al�� NaOH��Һ��Ӧ����2 Al + 2OH�� + 2 H2O��=
2 AlO2�� + 3 H2��
C��Na ��O2��Ӧ����������
4 Na + O2 ���� 4 Na+ + 2 O2��
D��AlCl3��ϡNH3.H2O��ϡ�Al3+ +
3OH�� �� Al(OH)3��
19����
ij�������������3��ȡ�����������ʽΪC8H10O��������������������Һ��Ӧ�Ľṹ��
A��1�֡��������������������� B��3�֡�����������������������C��6�֡��������������������� D��9��
20����
���и��������У���ȫȼ��ʱ���ɶ�����̼��ˮ�����ʵ���֮�ȴ���1�U1����
A����ϩ��ͬϵ����������������������������������������� B�����Ͷ�Ԫ��
C����ά�ء�����������������������������������������������������D������������ͬ���칹��
21����
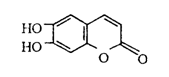 �в�ҩ��Ƥ�к��е���Ҷ���������ṹ����ͼ�������п������á���1mol��Ҷ�������ֱ��������������ˮ��NaOH��Һ��ȫ��Ӧ����������ĵ�H2��Br2��NaOH�����ʵ����ֱ�x��y��z ����x : y : z����
�в�ҩ��Ƥ�к��е���Ҷ���������ṹ����ͼ�������п������á���1mol��Ҷ�������ֱ��������������ˮ��NaOH��Һ��ȫ��Ӧ����������ĵ�H2��Br2��NaOH�����ʵ����ֱ�x��y��z ����x : y : z����
A��5: 3:
3��������������������B��2: 1:
2��������������������C��4: 3:
4��������������������D��4: 3:
2
22����
�����л�ѧ��Ӧ�IJ����У�������ͬ���칹�����
A��2���嶡���NaOH�Ĵ���Һ���ȡ����� �������� B��CH3��CH=CH2��HCl�����ӳɷ�Ӧ
C��CH3��CH2��CH2��Br��ǿ���ˮ��Һ��ˮ��
D���ױ���������м�������·���ȡ����Ӧ
23����
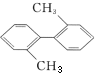 ��֪C��C�����Ƽ�����ת�����ڽṹ��ʽ����ͼ��ʾ����������˵����ȷ����
��֪C��C�����Ƽ�����ת�����ڽṹ��ʽ����ͼ��ʾ����������˵����ȷ����
A��������������10��̼ԭ�Ӵ���ͬһƽ����
B��������������9��̼ԭ�Ӵ���ͬһƽ����
C��������һ��ȡ���������4��
D�������DZ���ͬϵ��
24����
X��Y��Z���ǽ�������X�ֱ��A��Z��������Һ�У�X�ı�����Z������X��Y���ԭ���ʱ��YΪ������X��Y��Z���ֽ����Ļ��˳��Ϊ
A��X>Y>Z��������
B��X>Z>Y��������
C��Y>X>Z��������
D��Y>Z>X
�ڢ������ѡ����52�֣�
25����
��10�֣�A��B��C��D��E��FΪ������Է��������������������B���ܶȱȿ����Դ����̬����C��D��E��F��Ϊ�ܶȱ�ˮС��Һ̬��������A��C��E��F����ʹ���Ը��������Һ��ɫ��D��E��ͬϵ���Ȼ����������ˮ��Ӧ��ȴ���������嵥�����廯���������·���ȡ����Ӧ��A��D��F�����Ժ��ֱ�����ϣ���ȫȼ�����ɶ�����̼�����ʵ�������ˮ�����ʵ�����2����F�����е�̼ԭ����ǡ����A��D������̼ԭ�����ĺͣ���Ӿ۲�����ʹ�ý�Ϊ�㷺�����ϡ�A��C��ͨʽ��ͬ�IJ�ͬ������ʹC���嵥�ʰ����ʵ���1:1�����ӳɷ�Ӧ��ֻ�õ�3�ֲ��ʹC������������һ�������·����ӳɷ�Ӧ���ú�������Ƕ����üӳɲ������з���������������к���3������
��1����ȷ����A��B��C��D��E��F�Ľṹ��ʽ��
A��������
��B��������
��C��������
��D��������
��E��������
��F��������
��
��2����������A��B��C��D��E��F��ȫȼ�գ�������������������������
�������ƣ���ͬ�������ɶ�����̼���ٵ�������������������
��
��3�������ʵ�����A��B��C��D��E��F��ȫȼ�գ�������������������������
�������ƣ���ͬ��������ˮ����������������������
��
26���� ��2�֣�ij�����л���ʽ��Ϊ92��������������ȫ���������ò����ʽ����260����ó����л���������ǻ�����Ϊ________�������֣�����ˮ����Ϊ________����ܽ⡱���ܽ⡱����
27���� ��10�֣���ά������Ȼ����Ϊ�ḻ�Ŀ���������Ȼ�߷�����Դ��
��1����ά�ؿ��Ʊ����ڷ�֯����ֽ�ȵ�ճ����ά�۳ɷ���(C6H10O5)m�ݣ����������漰�����ѧ��Ӧ�����ռ�ͼ���£�
 |
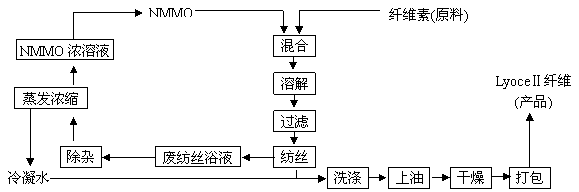 ��������������ѧ�ҿ�����һ��ʹ��NMMO�ӹ���ά�ص��·�������Ʒ��Lyoce����ά���ɷ�Ҳ��(C6H10O5)m����������ʾ��ͼ���£�
��������������ѧ�ҿ�����һ��ʹ��NMMO�ӹ���ά�ص��·�������Ʒ��Lyoce����ά���ɷ�Ҳ��(C6H10O5)m����������ʾ��ͼ���£�
�١�Lyoce����ά�����������У��ɳ��ѭ�����õ������������������������������� ��
���롰Lyoce����ά��������ȣ�ճ����ά�����л���������������� ��ֻ��ǽ���Ԫ�ط��ţ��ķ�����ɴ������������ɱ���
�ۡ�Lyoce����ά������Ϊ��21���͵���ɫ��ά����ԭ�������������������������������� ��
��2����Lyoce����ά�����������е�NMMO�ɰ�����·���Ʊ�(��Ӧ������ʡ��)��
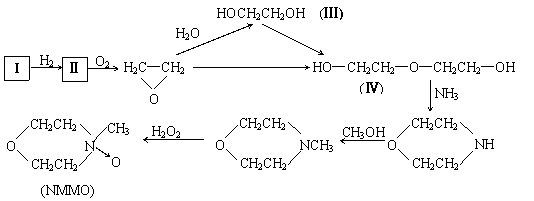 |
������ ���У�������I������Ϊ��ķ���������������ʹ��ˮ��ɫ��
�ٻ�����IҲ�ɾۺ�Ϊ��һ�������¾��е����Եĸ߷��ӻ�����ø߷��ӻ�����Ļ�ѧʽΪ������������ ��
�ڻ��������������Ӧ��ԭ�������ʴ�100%���仯ѧ����ʽΪ
��������������������������������������������������������������������������
��
�۹��ڻ��������˵����ȷ�������������������� (�����)��
A�����ɷ���������Ӧ������������������������������������B����ɱ������������ɱ�����
C��������ˮ��������������������������������������������������D��������Ʒ�Ӧ�����������Ʒ�Ӧ
E�������Ҵ���ͬϵ�����������������������������������F�������±������ȡ����Ӧ�Ʊ�
��д���ϳ����һ����Ӧ�Ļ�ѧ����ʽ�������������������������������������� ��
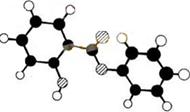
28���� ��14�֣����ޣ�Salol����һ�������������ķ���ʽΪC13H10O3,�����ģ������ͼ��ʾ��ͼ��������֮������ߴ�����ѧ�����絥����˫���ȣ���
��1��������ͼģ��д�����Ľṹ��ʽ������������ ��
��2������ˮ�⡢���롢�ᴿ�ɵõ������ı��Ӻ�ˮ���ᣨ���ǻ������ᣩ�������һ��������˵�����ӡ�̼�ᡢˮ���������������ǿ���û�ѧ����ʽ��ʾ�������������������������������� �� ������������������������������ ��
��3��ͬʱ��������Ҫ���ˮ�����ͬ���칹�干���������������� �֡�
�ٺ��б��������ܷ���������Ӧ������ϡNaOH��Һ��1mol��ͬ���칹������2molNaOH��Ӧ����ֻ����������һ�ȴ���
��4���ӣ�3��ȷ����ͬ���칹������ѡһ�֣�ָ��Ϊ���п�ͼ�е�A��
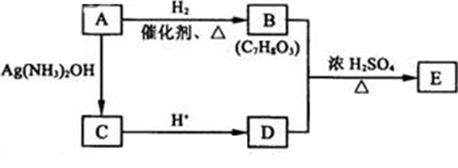
д������������Ӧ�Ļ�ѧ����ʽ���л����ýṹ��ʽ��ʾ������ָ����Ӧ�ķ�Ӧ���͡�
��A��B�������������������������������� ������������ ��Ӧ������ ����������
��B+D��E���������������������������� �������������� ��Ӧ����������������
��5������ˮ�����뱽�ӵĻ������ǵ����ʵ���֮��Ϊnmol���û������ȫȼ������O2 aL��������bg H2O��cL CO2�����������Ϊ��״���µ������
�ٷֱ�д��ˮ����ͱ�����ȫȼ�յĻ�ѧ����ʽ���л�����÷���ʽ��ʾ��
�������������������������������������������������������������������� ��
����������ˮ��������ʵ���Ϊxmol���г�x�ļ���ʽ��
29���� ��10�֣�ij��ѧС���������������������װ�ã���ͼ�����Ի������Ʊ�����ϩ
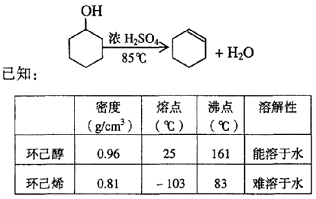
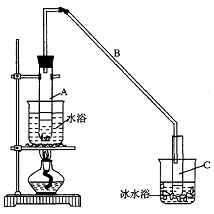
��1���Ʊ���Ʒ
��12.5mL�����������Թ�A�У��ټ���lmLŨ���ᣬҡ�Ⱥ�������Ƭ��������������Ӧ��ȫ�����Թ�C�ڵõ�����ϩ��Ʒ��
��A�����Ƭ��������____________������B���˵�������е�������____________��
 ���Թ�C���ڱ�ˮԡ�е�Ŀ����________________________________________________��
���Թ�C���ڱ�ˮԡ�е�Ŀ����________________________________________________��
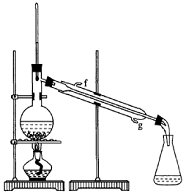
��2���Ʊ���Ʒ
�ٻ���ϩ��Ʒ�к��л������������������ʵȡ����뱥��ʳ��ˮ�������á��ֲ㣬����ϩ��_________��(���ϻ���)����Һ����_________ (������)ϴ�ӡ�
��a��KMnO4��Һ������b��ϡH2SO4 ���� c��Na2CO3��Һ
���ٽ�����ϩ����ͼװ��������ȴˮ��_________�ڽ��롣����ʱҪ������ʯ�ң�Ŀ����__________________��
���ռ���Ʒʱ�����Ƶ��¶�Ӧ��________���ң�ʵ���ƵõĻ���ϩ��Ʒ�����������۲��������ܵ�ԭ����_________��
��a������ʱ��70�濪ʼ�ռ���Ʒ������������ b���������������Ӽ���ˮ��Ӧ
��c���Ʊ���Ʒʱ���������Ʒһ������
��3���������ֻ���ϩ��Ʒ�ʹ�Ʒ�ķ�������������_________��
a�������Ը��������Һ��������b���ý����ơ��������� c���ⶨ�е�
�ġ������⡡
30����
��6�֣�0.2 mol�л����0.4 mol O2���ܱ�������ȼ�պ�IJ���ΪCO2��CO��H2O��g�������ᆳ��Ũ�����Ũ�������������10.8 g����ͨ�����ȵ�CuO��ַ�Ӧ������������3.2 g�����������ͨ����ʯ�ұ���ȫ���գ���ʯ����������17.6 g��
��1���жϸ��л���Ļ�ѧʽ��
��2����0.2 mol���л���ǡ����4.6 g��������ȫ��Ӧ����ȷ�����л���Ľṹ��ʽ��