高中二年级化学学业水平测试(必修科目)模拟考试
化学试题
|
本试卷可能用到的相对原子质量 H:1 C:12 O:16 S:32 Cl:35.5
Mg:24 Fe:56
一、单项选择题:在每题的四个选项中,只有一个选项是符合要求的(本大题17题,每题3分,共51分)。
1. 根据物质的组成对物质进行分类,Na2CO3属于
A.盐 B.有机物 C.碱 D.氧化物
2.下列说法正确的是
A.14C的中子数为14 B.14C的质子数为14
C.14C和12C互为同位素 D.14CO2的摩尔质量为46
3.下列叙述正确的是
![]() A.乙烯的结构简式为CH2CH2
B.氮分子的结构式为
A.乙烯的结构简式为CH2CH2
B.氮分子的结构式为
![]() C.氯化氢分子的电子式为 D.硫离子的结构示意图为
C.氯化氢分子的电子式为 D.硫离子的结构示意图为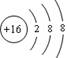
4.下列离子在溶液中可以大量共存的一组是
A.K+、Na+、SO42- B.K+、H+、HCO3-
C.Na+、H+、SiO32- D.Ca2+、OH-、CO32-
5.下列说法错误的是
A.CaO与H2O反应是放热反应
B.二氧化硅可用于制造光导纤维
C.浓硫酸和硝酸可以使所有金属钝化
D.NO2和H2O的反应不属于化合反应
6.全部由第二周期元素形成的化合物是
A.CO2 B.H2O C.Na2O D.MgCl2
7.下列离子方程式中正确的是
A. 铁与稀盐酸反应:Fe + 2H+ ══ Fe3+ + H2↑
B.氯气与H2O反应:Cl2+H2O══2H++Cl+ClO-
C.钠与水反应:2Na+2H2O══2Na++2OH-+H2↑
D.在硫酸铜溶液中加入过量的氢氧化钡溶液:Ba2++SO42-══BaSO4↓
8.某原子的最外电子层上只有1个电子,则它跟氯结合能形成的化学键是
A.一定是共价键 B.一定是离子键
C.可能是共价键,也可能是离子键 D.以上说法均不正确
9.下列说法正确的是
A.用澄清石灰水可区别Na2CO3和NaHCO3粉末
B.只能用加试剂的方法区别(NH4)2 SO4和Fe2(SO4)3溶液
C.用氯化钡溶液可区别SO42-和CO32-离子
D.用丁达尔效应可区别Fe(OH)3胶体和FeCl3溶液
10.设NA表示阿伏加德罗常数,下列叙述错误的是
A.2.4g金属镁变为镁离子时失去的电子数为0.2NA
B.在标准状况下,22.4 L H2O含有水分子的个数为NA
C.16 g臭氧(O3)中含有氧原子的个数为NA
D.1 L 1 mol/L NaCl溶液中含有钠离子的个数为NA
11.下列分离混合物的操作中,必须加热的是
A. 过滤 B.蒸馏 C.分液 D.萃取
12.下列说法正确的是
A.化学反应中化学能只可以转化为热能
B.可逆反应达到平衡后,正、逆反应速率均为0
C.N2和H2反应达到平衡后,无N2或H2剩余
D.化学反应中一定有化学键的断裂和形成
13.在下列所示的转化关系中,X不可能是
A.N2 B.H2 C.S D.C
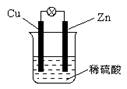
14.如右图所示的装置,下列说法正确的是
A.电子从铜片上流出 B.铜片上产生气泡
C.负极上发生了还原反应 D.锌片是原电池的正极
15.下列说法正确的是
A.乙醇催化氧化生成乙醛 B.常温下乙烯易发生取代反应
C.乙酸乙酯是高分子化合物 D.甲烷易发生加成反应
16.下列说法正确的是
A.苯分子中含有三个碳碳双键 B. 将乙酸和乙醇混合加热制取乙酸乙酯
![]() C.葡萄糖能够发生银镜反应
D. 糖类、油脂、蛋白质均能发生水解
C.葡萄糖能够发生银镜反应
D. 糖类、油脂、蛋白质均能发生水解
17.对于反应MnO2 + 4HCl(浓) MnCl2 + 2H2O + Cl 2↑,下列说法不正确的是
A.该反应是氧化还原反应
B.MnO2是氧化剂
C.HCl是还原剂
D.若生成7.1 g Cl 2,则转移0.1 mol电子
二、单项选择题:在每题的四个选项中,只有一个选项是符合要求的(本大题包括“A.化学与生活”和“B.有机化学基础”两个模块各6题,每题3分,每个模块18分。每位考生只可选择其中的一个模块作答)。
A.化学与生活
18.下列有关人体必需化学元素的说法错误的是
A.氟摄入过多可能导致氟斑牙
B.成人碘含量过高会引起甲状腺疾病
C.过量服用补铁剂可造成胃肠道出血
D.儿童缺锌会影响骨骼、牙齿的生长
19.下列说法正确的是
A.人体缺少维生素A易患夜盲症、干眼症
B.玻璃钢广泛用于制造汽车车身、船体和印刷电路板
C. 为使火腿肠颜色更鲜红,可多加一些亚硝酸钠
D.碳酸氢钠可作抗酸药,阿司匹林是重要的抗生素
20.下列物质中属于合成材料的是
A.羊毛 B.棉线 C.尼龙绳 D.蚕丝
21.下列有关环境保护的说法不正确的是
A.“白色污染”是废塑料制品造成的环境污染现象
B.生活废水中含氮、磷等元素,过多排放会引起水体污染
C.对煤等燃料进行脱硫处理后,可减少燃烧产物中SO2的含量
D.汽车使用乙醇汽油不会排放有害气体,故不必安装尾气净化装置
22.下列事实不能用电化学理论解释的是
A.镀锌铁比镀锡铁更耐用
B.铝制品不需要采用特殊方法保护
C.轮船吃水线以下的船壳上装有一定数量的锌块
D.钢铁在潮湿空气中比在干燥空气中腐蚀的快
23.某物质的结构简式为: 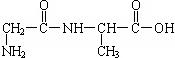 ,下列有关该物质的说法不正确的是
,下列有关该物质的说法不正确的是
A.分子式为C5H8O2N2
B.在一定条件下能发生脱水反应
C.是由一种氨基酸形成的二肽
D.既能和酸反应又能和碱反应
B.有机化学基础
18.下列物质中属于天然高分子化合物的是
A.酚醛树脂 B.氨基酸 C.油脂 D.纤维素
19.分子式为C4H8O2的有机物A,它能在酸性条件下水解生成B和C,在一定条件下B能氧化为C。下列说法不正确的是
A.B的红外光谱图出现C=O的特征吸收
B.A的结构只可能有1种
C.B的核磁共振氢谱图有三个特征峰
D.C可以发生取代反应
20.下列有机物的命名正确的是
A.3-甲基-2-戊烯 B.3-甲基-2-丁醇
C.3-乙基-1-丁炔 D.2,2-二甲基丁烷
21.高分子膜材料“ETFE”是四氟乙烯(CF2=CF2)与乙烯发生聚合反应得到的。下列说法正确的是
A.ETFE能使酸性高锰酸钾溶液褪色
B.合成ETFE的反应类型为取代反应
C.CF2=CF2可由CH3CH3与F2直接反应制得
D.CF2=CF2和CH2=CH2均是平面型分子
22.已知C4H9Cl的同分异构体共有四种,则分子式为C5H10O的醛应有
A.3种 B.4种 C.5种 D.6种
23.已知己烯雌酚是一种激素类药物,其结构简式如下图所示,则下列有关该物质的叙述不正确的是
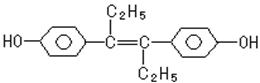
A.属于芳香族化合物 B.可以在空气中燃烧
C.能发生消去反应和加成反应 D.1 mol该物质可与5 mol Br2反应
三、本大题包括2题,共10 分。每题分为A题和B题,每位考生只可选做一题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题。
24.(5分)
A.人体所需要的营养素主要有糖、油脂、 、无机盐、维生素和水。根据维生素的溶解性,一般可把它们分为水溶性和 两大类。糖尿病患者的血液中葡萄糖的浓度很高,其中大部分的去向是 。将过量的维生素C溶液滴入碘水中,反应后单质碘转化为 ,为证明该反应的发生,常用试剂 检验。
B.苯酚的分子式是 ,它是一种无色晶体,但往往略带红色的原因是
。对甲基苯酚(CH3-![]() -OH)和苯甲醇(
-OH)和苯甲醇(![]() -CH2-OH)两种物质中,通常状况下能跟NaOH溶液反应的是 ,该反应能发生的原因是
(从分子中基团之间关系回答)。使用一种试剂,通过较简单的实验可鉴别稀醋酸和苯酚的溶液,这种试剂可以是 。
-CH2-OH)两种物质中,通常状况下能跟NaOH溶液反应的是 ,该反应能发生的原因是
(从分子中基团之间关系回答)。使用一种试剂,通过较简单的实验可鉴别稀醋酸和苯酚的溶液,这种试剂可以是 。
25.(5分)
A.化学兴趣小组查阅资料得知:甲醛是一种无色有刺激性气味的气体,沸点为-19.5oC,易溶于水,易被高锰酸钾氧化生成其他气体。大多数装修材料中含有甲醛。请回答下列问题:
(1)甲醛对人的皮肤和 有强烈的刺激作用。
(2)CO使人中毒是因为很容易和人体血液中的 结合。
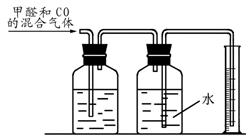
(3)该兴趣小组收集V1 L含有甲醛和CO的某居室空气,用下图装置测定其中甲醛和CO的含量。则装置A中盛放的试剂是 ,实验中还需要测定的数据是 。为了获得较准确的实验结论,他们需要采取的方法是 (填序号)。
a. 仔细做好每步操作,只做一次实验
b. 在A、B间加一个干燥装置
c. 重复做2~3次上述实验
A B C
B.已知:在碱性条件下,卤代烃可以跟某些阴离子发生取代反应。例如:
CH3CH2Br+CN-→CH3CH2CN+Br-。
请回答:
(1) 将溴乙烷和NaOH的醇溶液共热,发生的反应属于 (填反应类型)。
(2) 在碱性条件下,CH3Br与CH3COO-反应,所生成有机物的结构简式为 。
(3) A、B、C、D和醋酸五种有机物有如下图转化关系(其中部分产物没有列出):
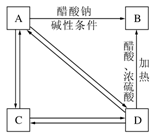
已知A是卤代烃,B的分子式为C5H10O2且无支链,C能使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色。则A的同分异构体的结构简式是 ,B的名称是 ,D的同类同分异构体 (填“能”或“不能”)直接氧化生成醛。
四、本大题3题,共21分。
26.(5分)在下图所示的实验装置中,A中盛有品红溶液,B 中盛有NaOH溶液。
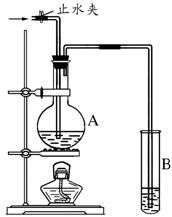
请回答下列问题:
(1) 若向A中通入足量的二氧化硫气体,A中的现象是 。
(2) 若向A中通入足量的氯气后,再加热A,A中的溶液 (填“能”或“不能”)恢复到原来的颜色。
(3) 如果A中盛的是氨水,B中盛的是无色酚酞溶液,微热,B中溶液会变为红色,则此时表现氨水的化学性质有碱性和 性。
(4) 如果A中盛的是浓硫酸,加入铜,加热反应,此反应中表现浓硫酸的酸性和 性。
(5) 如果A中盛的是盐酸,加入铜粉,为了让铜粉溶解,可以加入NaNO3,反应离子方
程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,请用单线桥标出其电子转移的方向和数目。
27.(6分)下图中A~H均为中学化学中常见的物质,它们之间有如下转化关系。其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应。(反应过程中生成的水及其他产物已略去)
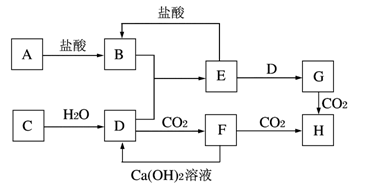
请回答以下问题:
(1)B是_________,H是_________。(填化学式)
(2)写出E转化为G的离子方程式____________。
(3)A在常温下也可与NaOH溶液反应生成G,写出此反应的化学方程式 _______。
28.(10分)化学学习小组为测定某补血剂中硫酸亚铁的含量进行了以下探究:
【查阅资料】本品为糖衣片,除去糖衣后显淡蓝绿色,主要成分硫酸亚铁(FeSO4·7H2O)。
【实验步骤】取本品10片,在适当的条件下配成100mL溶液,分别准确量取20mL溶液,用下列两种方法进行实验:
方法一、用一定物质的量浓度的酸性高锰酸钾溶液滴定。
方法二、加过量H2O2溶液,然后再加入过量NaOH溶液,得红褐色沉淀,将沉淀过滤并充分加热得红棕色固体,称量该固体的质量。
请回答下列问题:
(1)方法一中,配制一定物质的量浓度的酸性高锰酸钾溶液时,所需要的玻璃仪器除量筒、玻璃棒、胶头滴管、烧杯外还有 。
(2)方法二中,加过量H2O2溶液的目的是 。有的同学认为使用氯气也能达到此目的,和使用氯气相比,用H2O2溶液的好处是 。
(3)在方法一中,若每消耗1mL酸性高锰酸钾溶液相当于0.152 g FeSO4,则该溶液中高锰酸钾的物质的量浓度是 。在方法二中,若称得红棕色固体的质量为a g,则每片补血剂含FeSO4 g。
化学试题参考答案和评分标准
说明:学生解答主观性试题时,使用与本答案不同的其它合理答案的也给分。
一、共51分。每题3分。每题只有一个选项是符合要求的。
1.A 2.C 3.D 4.A 5.C 6.A 7.C 8.C 9.D 10.B 11.B 12.D 13.B 14.B 15.A 16.C 17.D
二、共18分。每题3分。每题只有一个选项是符合要求的。
18.D 19.A 20.C 21.D 22.B 23.C
三、共10 分。第24题5分,每空1分。第25题5分,每空1分。
24.A.蛋白质 脂溶性 通过尿液排出 I- 淀粉溶液
B.C6H6O 部分被氧化 对甲基苯酚 苯环对羟基的影响 碳酸氢钠溶液等
25.A.(1)呼吸器官 (2)血红蛋白
(3)水 C中水的体积 c
B.(1)消去反应 (2)CH3COOCH3
(3)CH3CH2BrCH3 乙酸丙酯 不能
四、共21分。第26题5分,每小题1分。第27题6分,每小题2分。第28题10分,每空2分。
26.(1)红色褪去 (2)不能 (3)略 (4)强氧化 (5)略
27.(1)AlCl3 NaHCO3
(2)Al(OH)3 + OH- == AlO2- + 2H2O
(3)2NaHCO3 ![]() Na2CO3 + CO2↑+ H2O
Na2CO3 + CO2↑+ H2O
28.(1)容量瓶 (2)使Fe2+完全氧化成Fe3+ 无污染
(2)0.2 mol·L-1 0.95a