�߶��꼶��ѧ�ڶ�ѧ�����п�����
������ ѧ �� ���������⣺�����ϡ� ��ˣ�ʯΰΰ��07/04/30
���Ծ���Ϊ�ڢ���͵ڢ�������֡�����120�֡�����ʱ��100���ӡ�
�����õ������ԭ��������H��1��C��12�� O��16��
�ڢ����ѡ��������64�֣�
һ���� ѡ���⣨���8С�⣬ÿ��3�֣���24�֡�ÿС��ֻ��һ��ѡ��������⣩
1��������������ϳɵĵ�һ���л�����
A����ʯ��������B�����顡����C�����ء�������D������
2����������������ȥ��һ����ԭ�Ӻ����õ�������ֹһ�ֵ��ǡ�����
�� ��A�����顡�� ������ B�����顡������������C�����顡���� ������D��������
3����֪һ��������8��ͬ���칹�壬����֪�촼�����ڴ��ࣩ��ͬ���칹�����Ŀ��
A��5�� ������ B��6�֡��������� C��7�֡��� ������D��8��
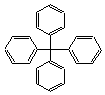 4����������е�4����ԭ��ȫ��������ȡ�����ɵ���ͼ��ʾ�ķ��ӣ��Ը÷��ӵ���������ȷ����
4����������е�4����ԭ��ȫ��������ȡ�����ɵ���ͼ��ʾ�ķ��ӣ��Ը÷��ӵ���������ȷ����
A������ʽΪC25H20����������
B������������ԭ���п��ܴ���ͬһƽ��
C���û��������������ԭ�Ӳ����ܴ���ͬһƽ��
D�����л������ڷ�������
5�������л���������϶��������
A. 3-��-2-��ϩ��B.2-��-2-��ϩ�� C. 2��2-�������� �� D. 2-��-3-��Ȳ
6����25��ʱ�����ʵ���Ũ�Ⱦ�Ϊ1mol/L ��(NH4)2SO4��(NH4)2CO3��(NH4)2Fe(SO4)2��������Һ�У������c��NH4+���ֱ�Ϊa��b��c����λ��mol/L���������ж���ȷ����
A��a=b=c��������������B��a>b>c������������ C��a> c > b����������D��c > a > b
7�������£�ij��ɫ����Һ����ˮ���������H+��OH��Ũ�ȵij˻�Ϊ1��10��24�������Һ�п��ܴ��������������Ϊ
A��SiO32����SO32����MnO4����Cl����������B��I����NO3����K+��NH4+
C�� Na+��Cl����SO42����K+�� ����������D��HCO3����Al3+��Na+��SO42��
8������ʵ�������ʵ�����ݼ�¼����ȷ����
A����100mL��Ͳ������ȡNaCl��Һ�����Ϊ93.2mL
B���ü�ʽ�ζ���ȷ��ȡKMnO4��Һ�����Ϊ21.50mL
C����ʪ���pH��ֽ��ϡ������Һ��pHֵ��pH=3.5
D���õ�����ֽ������ֱ�ӳ�ȡNaOH���壬����Ϊ10.2g
����������ѡ����(�������10С�⣬ÿС��4�֣���40�֡�ÿС����һ��������ѡ��������⡣����ȷ��ֻ����һ��ѡ���ѡʱ������Ϊ0�֣�����ȷ�𰸰�������ѡ�ֻѡһ������ȷ�ĵ�2�֣�ѡ�����Ҷ���ȷ�ĵ����֣���ֻҪѡ��һ����С���Ϊ0��)
9������ȡ���������У�̼ԭ�Ӷ����������Ϊ8���ӽṹ����
A���һ�����CH2CH3�������������� ������B��̼������[(CH3)3C��]
C����ȩ (CH3CHO)����������������������D��̼ϩ��(:CH2)
10���л��������е� ![]() ���еġ�OH��±ԭ��ȡ�����õĻ�����Ϊ��±�����л������п��Կ�����±���ǡ���������������������������
���еġ�OH��±ԭ��ȡ�����õĻ�����Ϊ��±�����л������п��Կ�����±���ǡ���������������������������
������ A. HCOF������ B. CCl4��������C. COCl2������ D.��CH2ClCOOH
11��ij������6.4 g����������ȫȼ�գ�ֻ����8.8 g CO2��7.2 g H2O������˵����ȷ����
A�����û��������̼��������Ԫ�ء�������B���û�������̼����ԭ�Ӹ�����Ϊ1��4
C����ȷ���û������Ƿ�����Ԫ�ء��� D���û�������һ��������Ԫ��
![]()
|
![]()
![]()
![]()
![]() A��
����������������
B������������������
C�� ��������������
D��
A��
����������������
B������������������
C�� ��������������
D��
13��ij�л���ķ���ʽΪC3H6O��ͨ���˴Ź�����������3���壬���������Ϊ
1 ��2 ��3��������ʿ�����
A.CH3COCH3 �� B.CH3CH2CHO��C.CH2=CH��CH2OH��D.CH2=CH��O��CH3
14��0.1mol/L�Ĵ�����Һ��ˮϡ��10������������Ũ�ȼ���������
A��CH3COO-�������� B��H+�������� C��OH-�������� D��CH3COOH
15��25��ʱ����pH��x��H2SO4��Һ��pH��y��NaOH��Һ�������1:100��ϣ���Ӧ��������ҺpH��7����x��![]() y����xֵΪ
y����xֵΪ
A��2���������������� B��3������������������ C��4��������������������D��5
16����һ�ܱ������У���ӦaA(g)![]() bB(g)��ƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��B��Ũ����ԭ����60%����
bB(g)��ƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��B��Ũ����ԭ����60%����
A��ƽ��������Ӧ�����ƶ������� B������A��ת���ʼ�С������
 C������B�������������������� D��a��b
C������B�������������������� D��a��b
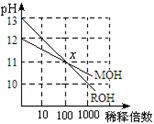
17��MOH��ROH����һԪ�����Һ�ֱ��ˮϡ��ʱ��pH��
�仯����ͼ��ʾ����������������ȷ������������������������������������������������
A��MOH��һ����������������
B����x�㣬c(M��) �� c(R��)
C����x�㣬ROH��ȫ��������
D��ϡ��ǰ��c(ROH) ��10 c(MOH)
18����ͼ�����Ǻ�ѹ�ܱ����������Ǻ����ܱ�������

����������ͬʱ�������зֱ����2mol X��2mol Y����ʼʱ���������ΪV L���������·�Ӧ���ﵽƽ��(X��Y״̬δ֪)��2X(?)��Y(?)![]() aZ(g)����ʱ����X��Y��Z�����ʵ���֮��Ϊ1:3:2��������˵��һ����ȷ����
aZ(g)����ʱ����X��Y��Z�����ʵ���֮��Ϊ1:3:2��������˵��һ����ȷ����
A����X��Y��Ϊ��̬����ƽ��ʱ����ƽ��Ħ����������
B����X��Y����Ϊ��̬����ƽ��ʱ����ƽ��Ħ����������
C����XΪ��̬��YΪ��̬�������д���ʼ��ƽ������ʱ����ͬ
D��ƽ��ʱ�����������С��V L
�� ѧ �� ���� ���⣺�����ϡ� ��ˣ�ʯΰΰ�� 07/04/30
�뽫�ڢ���е�ѡ����Ĵ������±�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| �� |
|
|
|
|
|
|
|
|
|
| ��� | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| �� |
|
|
|
|
|
|
|
|
|
�ڢ�� ����ѡ��������56�֣�
��������⣨�������4С�⣬��35�֣�
19����10�֣�(1) ��ϵͳ����������
�١��л���CH3CH(C2H5)CH(CH3)2��������________________________.
�ڡ����л�����������ijһ��̼ԭ������4����ͬ��ԭ�ӻ���ţ�������̼ԭ�ӳ�Ϊ������̼ԭ�ӡ���C7H16��ͬ���칹���о��С�����̼ԭ�ӡ�����_______��, д������һ�ֵ������������������������� _________������
(2) д�����и����л���Ľṹ��ʽ
������ 2��3��������4���һ����� _____________________________________
�ڡ�֧��ֻ��һ���һ���ʽ����С������_____________________________________��
![]() 20����6�֣��л���Ľṹ���á�����ʽ����ʾ��CH3��CH��CH��CH3�ɼ�дΪ ���� ��
20����6�֣��л���Ľṹ���á�����ʽ����ʾ��CH3��CH��CH��CH3�ɼ�дΪ ���� ��
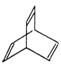 |
�л���X�ļ���ʽΪ��
��1������ �л���Y��X��ͬ���칹�壬�����ڷ�������д��Y�Ľṹ��ʽ����������������������������������������������������������
��2��Y����ϩ��һ�������·��������ʵ����ۺϷ�Ӧ��д���䷴Ӧ�Ļ�ѧ����ʽ��
������������������������������������������������������������������������
��3��X��������H2��һ�������·�Ӧ�����ɻ�״�ı�����Z��Z��һ�ȴ������������� �֡�
21����6�֣����л���ѧ������,���ݷ�Ӧ�����ʺͷ�Ӧ����,����ȷ��ϩ������ɺͽṹ(˫����֧����λ��),����:
��������������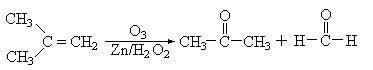
������ ���������������з�Ӧ��ʵ,ȷ��C7H14�Ľṹ������:
��������������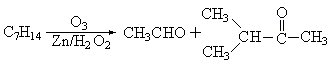
�����Ľṹ��ʽ��________________________,������____________________���� ___
����̼ԭ�ӵ��ӻ���ʽΪ�������������������� �����ţ�
�� sp �ӻ���������sp2 �ӻ����� ��sp3 �ӻ����� ��̼ԭ��û���ӻ�
22����13�֣���1�������£�ij���Na2CO3����Һ�е����̪����Һ�ʺ�ɫ�������Һ��
�������� �ԡ��ڷ�������Һ����̪�ʺ�ɫԭ��ʱ����ͬѧ��Ϊ��������Һ���õĴ�����Ʒ�л���NaOH��������ͬѧ��Ϊ����Һ��Na2CO3�������CO32��ˮ���������������һ����ʵ�鷽����������λͬѧ��˵�������У���������������ͽ��ۣ������������� ����������������������������
 ��������������������������������������������
����������������������
��������������������������������������������
����������������������
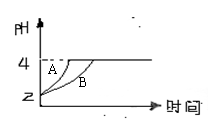
��2�������£�ȡpH=2������ʹ�����Һ��100mL����
���зֱ����������Zn������Ӧ����������Һ��pH�仯
����ͼ��ʾ����ͼ�б�ʾ������Һ��pH�仯���ߵ���
�������� ������A������B����������������Zn����
Ϊm1�� ������Һ�м����Zn����Ϊm2����m1������m2
��ѡ���������=������������
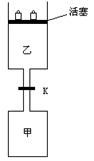 ��3����ͼ��ʾ�����رշ���Kʱ������г���1.5 mol A��3.5 mol B�������г��� 3
mol A��7 mol B����ʼʱ���ס��������ΪV L������ͬ�¶Ⱥ��д������ڵ������£��������и��Է������з�Ӧ��
��3����ͼ��ʾ�����رշ���Kʱ������г���1.5 mol A��3.5 mol B�������г��� 3
mol A��7 mol B����ʼʱ���ס��������ΪV L������ͬ�¶Ⱥ��д������ڵ������£��������и��Է������з�Ӧ��
3A(g)��2B(g)![]() C(g)
C(g)![]() ��2D(g)����H<0
��2D(g)����H<0
�ﵽƽ�⣨��ʱ��V(��)=0.86V��L����ش�
��1������B��ת����Ϊ ���������� ��
��2������D������C�����ʵ����Ƚϣ��������� �����ȡ�����ǰ�ߴ������ߴ���
��3����K����һ��ʱ�����´�ƽ�⣨��ʱ���ҵ����Ϊ�������� ���ú�V�Ĵ���ʽ��ʾ����ͨ��������������Բ��ơ���
�ġ�ʵ���⣨�������1С�⣬��13�֣�
23����13�֣�ͨ����ȼ�յķ����ⶨ�л���ķ���ʽ������ȼ�����ڽ��л�����Ʒ�봿���ڵ�¯�����³��ȼ�գ����ݲ�Ʒ�ĵ�����ȷ���л������ɡ���ͼ��ʾ������ȼ�շ�ȷ���л��������ʽ�ij���װ�á�
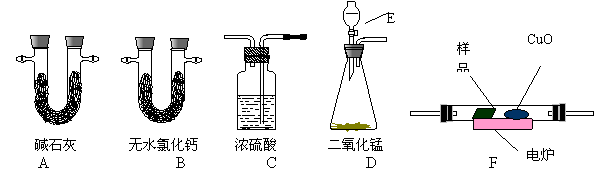
��1����ȷ��ȡ0.44 g��Ʒ��ֻ��C��H��O����Ԫ���е����ֻ����֣�����ȼ�պ�A������0.88 g��B������0.36g����ش𣺣�1�������������IJ�����Ϣ��װ�õ�����˳��Ӧ��
![]()
![]()
![]()
![]() D���� ���������� F���� ������������������ ��
D���� ���������� F���� ������������������ ��
��2��A��B���ھ�ʢ���й�̬�Լ���A�ܵ�������______________________��
��3��E��Ӧʢװʲô�Լ���_______________��
��4�������CuO��ȥ����A��������_______�������������С�������䡱��
��5�����л����ʵ��ʽΪ__________________��
��6��Ҫȷ�����л���ķ���ʽ��������֪����������___________��
�� ����Һ��E������������ ����Ʒ��Ħ������������������ �� CuO������ٵ���������
�� Cװ�����ӵ����������� �� ȼ������O2�����ʵ���
�塢�����⣨�������2С�⣬24��Ϊ3�֣�25��5�֣���8�֣�
24����֪Ag2CrO4��AgCl��AgI���ܶȻ������ֱ�ΪKsӨ(Ag2CrO4)=1.12��10-12��KsӨ(AgCl)=1.77��10-10���� KӨs(AgI)=8.51��10-17���ں���CrO42-��Cl����I-���ӵģ�����Ũ�Ⱦ�Ϊ0.1mol��L-1������Һ�У���μ���AgNO3��Һ�������������������������� ������
��������������������� ����������������������������� ����
25��5.8g�л�����ȫȼ�գ�ֻ����CO2��H2O���������Ϊ1:1(ͬѹͬ��)����������ͨ����ʯ�ң���ʯ��������18.6g����֪���л���Կ���������ܶ�Ϊ2��
��(1)�л������Է�����������(2)�л���ķ���ʽ��
��
�� ѧ �� �� �� �� �� ���������⣺�����ϡ� ��ˣ�ʯΰΰ
�뽫�ڢ���е�ѡ����Ĵ������±������������������������������� 07/04/30
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| �� | C | C | D | B | D | D | C | A | C |
| ��� | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| �� | AC | BD | B | BD | D | B | AC | D | AC |
19���š��� 2,3-�������顡���ڡ�2�֡� 3-�������2,3-��������
��2�� �� ![]() �����ڡ�
�����ڡ� ![]() ��������
��������
20��(1) ![]() ��2��
��2��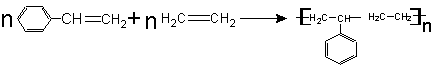
(3)2�֡� (ÿС��2�֣���6��)
21�������Ľṹ��ʽ��: (CH3)2CHC(CH3)=CHCH3 ,������:3,4-����-2-��ϩ�����ڢ�
22����1����������ɫ��Һ�м�������BaCl2��Һ�������Һ���Ժ�ɫ˵������ȷ����ɫ��ȥ˵������ȷ���������Լ�����Ҳ���֣�
��2��B����
��3��20% ��2�����ߴ�3��0.29V
23����1��C��B��A�� ��ÿ��1�֣�������2��������Ʒ��Ӧ���ɵ�CO2�� ��3��˫��ˮ����4����С�� ��5��C2H4O����6�� �ڡ���ÿ��2�֣�
24��AgI��AgCl��Ag2CrO4����ÿ��1�֣�
��:����Ag2CrO4�����������Ag+Ũ��Ϊ��(1.12��10-12/0.1)0.5 =3.35��10-6������ ����������������������������
���� ����AgCl�����������Ag+Ũ��Ϊ��
�������������� ���������������� 1.77��10-10/0.1 = 1.77��10-9 mol��kg-1
���� ����AgI�����������Ag+Ũ��Ϊ:
������������������������������
8.51��10-17/0.1
= 8.51��10-16
mol��kg-1
25����1������л���ΪA��������֪Mr��A����2��29��58����������2�֣�
��2����Aȼ��ֻ����CO2��H2O���������Ϊ1:1�����������ʽΪCxH2xOz�� ��������n(CxH2xOz)=m(CxH2xOz)/M(CxH2xOz)��5.8g/58g��mol��1��0.1mol������ ��1�֣�
������ CxH2xOz������ xCO2�� ���� xH2O
������ 1���������� x���������� x
0.1mol���� 0.1x mol����0.1x mol���� ��44��0.1x ��18��0.1x��18.6����x��3����1�֣�
����A����Է�����Ϊ58����z��1���������ʽΪ��C3H6O������ ��������1�֣�
������������������������������������������������������