高二化学学业水平调研测试
化 学 试 题
注意事项:
1. 本试题包括四大题,28小题(共8页),满分100分。考试时间75分钟
2. 答题前,考生务必将卷密封线内各项填写清楚。
3. 选择题答案填在Ⅱ卷选择题答题栏内,其它试题答案直接写在试卷规定位置。考试结束考生只交第Ⅱ卷。
第Ⅰ卷(选择题 共69分)
可能用到的相对原子质量 H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Ba-137
一、单项选择题:在每题的四个选项中,只有一个选项是符合要求的(本大题包括17小题,每题3分,共51分)
1.中共十七大报告提出:“建设生态文明,基本形成节约能源资源和保护生态环境的产业结构,增长方式、消费模式”。下列行为不利于“生态文明”建设的是
A.在化学反应中要考虑“原子经济性”以提高效率
B.资源的开发和利用,要考虑可持续发展的原则
C.要加强对工业“三废”的治理,以保护环境
D.将废弃的塑料袋回收进行焚烧,以解决“白色污染”问题
2.2007年,我国成功发射了“嫦娥一号”月球探测卫星。人类探测月球发现,其土壤中存在较丰富的质量数为3的氦元素,它可以作为核聚变的重要原料之一。而在地球上,氦元素主要以24He的形式存在。以下关于24He的说法正确的是
A. 是 4He的同分异构体 B.与4He是同一种核素
C.是4He的同位素 D.比4He少一个质子
3.下列叙述正确的是
A.摩尔是物质的质量单位 B.碳的摩尔质量为12g
C.阿伏加德罗常数约为6.02×1023mol-1 D.一个碳原子的质量为12g
4.以下对Cl-离子的说法的叙述正确的是
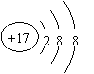
![]() A.结构示意图为:
B.电子式为: Cl
A.结构示意图为:
B.电子式为: Cl
C.比F-离子半径小 D.具有漂白性
5.用左图表示的一些物质或概念间的从属关系中不正确的是
|
| X | Y | Z |
| A | 极性键 | 共价键 | 化学键 |
| B | 胶体 | 分散系 | 混合物 |
| C | 电解质 | 离子化合物 | 化合物 |
| D | 氧化物 | 化合物 | 纯净物 |
6.以下对乙烯 的描述不正确的是
A.其产量可以用来衡量一个国家的石油化工发展水平
B.能使溴的四氯化碳溶液褪色
C.可作为水果的催熟剂
D.与乙炔互为同分异构体
7.下列反应属于氧化还原反应的是
A.Ca(OH)2+2HCl==CaCl2+2H2O B.CaO+H2O==Ca(OH)2
C.2Cl2+2Ca(OH)2==Ca(ClO)2+CaCl2+2H2O D.CaCO3==CaO+CO2↑
8.以下对元素周期表中第三周期元素原子结构与性质的说法不正确的是
A.钠元素形成的最高价氧化物对应的水化物碱性最强
B.从左到右元素的原子半径依次增大
C.铝元素形成的氧化物为两性氧化物
D.气态氢化物的稳定性:HCl>H2S
9.通过复习总结,你认为下列对化学知识的理解不合理的是
A.盛放氢氧化钠溶液的试剂瓶用橡皮塞,不用玻璃塞
B.常温下可用铁、铝制容器盛放浓硫酸或浓硝酸,因为它们不反应
C.N2和H2合成NH3,属于氮的固定
D.丁达尔效应是检验胶体和溶液的一种物理方法
10.对反应:C+2H2SO4==2SO2↑+CO2↑+2H2O,下列说法不正确的是
A.浓H2SO4作氧化剂 B.C元素被氧化 C.S元素的化合价降低 D.转移的电子数为2e-
11.由下列化学方程式改写的离子方程式正确的是
A.AlCl3+3NH3・H2O==Al(OH)3↓+3NH4Cl Al3++3OH-==Al(OH)3↓
B.BaCO3+2HCl==BaCl2+CO2↑+H2O CO32-+2H+==CO2↑+H2O
C.2NaOH+H2SO4==Na2SO4+2H2O H++OH-==H2O
D.(NH4)2SO4+Ba(OH)2==BaSO4↓+2NH3・H2O NH4++OH-==NH3・H2O
12.下列有关化学能与热能的说法正确的是
A.酸与碱发生中和反应所放出的热量称为中和热
B.若某反应的反应物的总能量大于生成物的总能量,则该反应为吸热反应
C.H2→H+H的变化需要吸收能量
D.凡经加热而发生的化学反应都是吸热反应
13.在无色溶液中,下列离子组能大量共存的是
A.Na+、K+、OH-、Cl- B.Na+、Cu2+、SO42-、NO3-
C.Fe3+、Na+、SO42-、SCN- D.Ba2+、SO42-、NO3-、K+
14.下列实验操作正确的是
①用湿润的红色石蕊试纸置于氨气集气瓶口,检验氨气是否集满
②过滤时,玻璃棒的末端应轻轻靠在三层滤纸上
③配制0.1mol/LNaOH溶液过程中,将NaOH固体放在滤纸上称量
④可用FeCl3溶液除去试管内难以刷去的铜迹
⑤用分液漏斗分液时,要控制好活塞,先让下层液体流出,再让上层液体慢慢流下
A.①②④ B.②④⑤ C.①③④ D.③④⑤
15.用Zn与稀硫酸反应制取氢气,以下条件不能加快反应速率的是
A.加热 B.将锌粒制成锌粉 C.降温 D.适当增大稀硫酸的浓度
16.某同学配制一定物质的量浓度的氢氧化钠溶液时,造成所配溶液浓度偏高的是
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量的NaOH溶液残留在烧杯中
D.用带游码的托盘天平称2.4gNaOH时,误用了“左码右物”方法
17.铅蓄电池是广泛应用于汽车、柴油机、等的启动电源。电池总反应式为:Pb+PbO2+2H2SO4==2PbSO4+2H2O.下列说法正确的是
A.该电池的正极为铅 B.该电池反应中PbO2起催化剂作用
C.该电池的正极为PbSO4 D.该电池的负极为铅
二、单项选择题:在每题的四个选项中,只有一个选项是符合要求的(本大题包括“A.化学与生活”和“B.有机化学基础”两个模块各6小题,每小题3分,每个模块18分。每位考生只可选择其中的一个模块作答)。
A.化学与生活
18.下列同学饮食习惯科学的是
A.多吃肉,少吃蔬菜水果 B.合理摄入糖类、油脂等,注意膳食平衡
C.调味品和营养剂加的越多越好 D.饮用水越纯净越好
19.以下对生活事实的解释,不正确的是
A.厨房里洗涤油污,常用碱性洗涤剂,因为油脂会在碱性溶液中水解
B.食用加碘盐,铁强化酱油可补充人体的微量元素
C.甲醛溶液虽能使细菌的蛋白质变性死亡,但不宜浸泡海产食品
D.食品添加剂虽然能改善食物的色、香、味,但由于它们对身体健康有害,均不宜食用
20.装饰不久的居室,由于装饰材料释放出的污染物浓度过高,影响人体健康,这些污染物最常见的是
A.二氧化硫 B.甲醛、苯等挥发性有机物
C.一氧化碳 D.一氧化氮、二氧化氮
21.运用化学知识可以解决日常生活中遇到的许多问题,下列说法不正确的是
A.液氯罐泄漏时,可将其移入水塘中,并向水塘中加入生石灰
B.胃酸过多的病人,可以服用氢氧化铝来中和胃酸,缓解胃部不适
C.用淀粉溶液检验食盐是否为加碘盐
D.用稀硝酸回收利用破碎热水瓶胆内的银
22.以下鉴别食盐水和蔗糖水的方法,其中适合在实验室进行鉴别且方法正确的是
①在两种溶液中分别加入少量稀硫酸,加热,再加入碱中和硫酸,再加入银氨溶液,微热
②测量溶液的导电性 ③在两种溶液中加入新制的氢氧化铜,加热 ④用舌头尝味道
A.①② B.①③ C.②③ D.③④
23.你认为以下叙述无科学性错误的是
A.铅笔芯的原料是金属铅,儿童在使用时不可以用嘴允咬铅笔,以免引起铅中毒
B.一氧化碳有毒,生有煤炉的居室可放置数盆清水吸收一氧化碳,以防煤气中毒
C.可用灼烧的方法区别羊毛织物和尼龙等化纤织物
D.在食品包装袋内放入生石灰可以防止食品因氧化而变质
B.有机化学基础
18.糖类、脂肪和蛋白质是维持人体生命活动所必须的三大营养物质。下列说法不正确的是
A.淀粉和纤维素均可用(C6H10O5)n表示
B.淀粉水解的最终产物能发生银镜反应
C.向蛋白质溶液中加入饱和硫酸铵溶液后产生的沉淀能重新溶于水
D.脂肪能发生皂化反应,生成甘油和硬脂酸钠两种物质
19.(CH3CH2)2CHCH3的正确命名是
A.3―甲基戊烷 B.2―甲基戊烷 C.2―乙基丁烷 D.3―乙基丁烷
20.丙烯酸的结构简式为CH2=CH-COOH,对其性质描述不正确的是
A.能与金属钠反应放出氢气
B.能与新制的氢氧化铜反应
C.能发生加聚反应生成高分子化合物
D.能与溴的四氯化碳溶液发生取代反应而使其褪色
21.分子式为C6H12O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化为C。则有机物A的可能结构简式有
A.1种 B.2种 C.3种 D.4种
22.下列除去括号内杂质的有关操作正确的是
A.苯(苯酚):加饱和溴水振荡,过滤 B.乙酸(乙醇):分液
C.乙醇(水):蒸馏 D.乙酸乙酯(乙酸):加氢氧化钠溶液,蒸馏
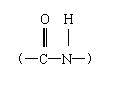 |
23.两个α-氨基酸分子脱水形成的含有肽键 的化合物称为二肽,二肽还可以继续与其它的α-氨基酸分子脱水形成三肽、四肽以致生成长链的多肽。若丙氨酸[CH3CH(NH2)COOH]与甘氨酸[H2N-CH2-COOH]的混合物在一定条件下反应,可形成二肽的种类有
A.1种 B.2种 C.3种 D.4种
第Ⅱ卷(选择题 共31分)
选择题答题栏:(18~23题只可选择其中的一个模块作答)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | D | C | C | A | C | D | C | B | B |
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 |
|
| 答案 | D | C | C | A | A | C | B | D |
|
| 题号 | 18 | 19 | 20 | 21 | 22 | 23 | |||
| A.(化学与生活)答案 | B | D | B | C | A | C | |||
| B.(有机化学基础)答案 | D | A | D | A | C | D | |||
三、本大题包括2小题,共10 分。每题分为A题和B题,每位考只可选做一题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题。
24.(5分)
A.(1)维生素是参与生物生长发育和新陈代谢所必需的一类小分子有机化合物;我们 所熟悉的维生素有A、B、C、D、E等。其中维生素C又称 ;人体自身 (填能或不能)合成维生素C;上述五种维生素中,属于水溶性维生素的是 。
(2)某同学一天的食谱为:米饭、烙饼、豆腐、鸡蛋、糖醋排骨、酱牛肉。你认为这位同学还应该吃一些 食物,营养才算平衡。
![]() (3)人们熟知的一种感冒药阿司匹林的结构式为:
OCOCH3
(3)人们熟知的一种感冒药阿司匹林的结构式为:
OCOCH3
COOH
请你写出其中含有的一种官能团的名称
B.在下列物质中选择相应的序号填空:
①甲烷 ②乙烯 ③乙炔 ④甲苯 ⑤乙醇 ⑥乙酸乙酯
(1) 分子结构为正四面体的是
(2) 分子中含有碳碳三键的是
(3) 能发生水解反应 的是
(4) 在核磁共振氢谱中有三个吸收峰,且峰面积之比为1:2:3的是
(5) 能使酸性高锰酸钾溶液褪色,但不能使溴的四氯化碳溶液褪色的是
25.(5分)
A.影响金属腐蚀的因素包括 和 两个方面,因此常用的防止金属腐蚀的方法包括改变金属内部组织结构、在金属表面 和电化学保护法等。每年因酸雨对金属的腐蚀也很严重,我国主要以硫酸型酸雨为主,形成这种酸雨的主要原因
我国目前防治这种酸雨所采取的措施有多种,请指出其中的一种措施
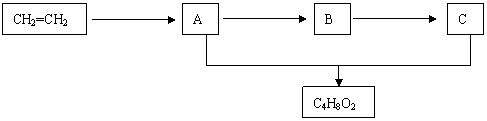
B.A、B、C在一定条件下,有如下转化关系:
 ①
②
③
①
②
③
④
请根据上图回答:
(1) 写出①的反应类型
(2) 分别写出②、④反应的化学方程式(有机物用结构简式表示):
 四、本大题包括3题,共21分。
四、本大题包括3题,共21分。
26.(5分)以下是实验室常用的部分仪器,请回答下列问题:
① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(1)编号为⑧、⑩仪器的名称分别为 、
(2)在分液操作中,必须用到上述仪器中的 (填编号)
(3)能做反应容器且可直接加热的仪器是上述中的 (填名称)
27.(6分)以下框图中各物质均为中学化学中常见的物质,且构成这些物质的元素均为短周期元素。
已知:①A、D、G为单质,其中只有D为非金属单质,且常温为气态;其余为化合物或化合物的水溶液,②G的焰色呈黄色,③F是无色、有特殊香味的液体,其相对分子质量为46.
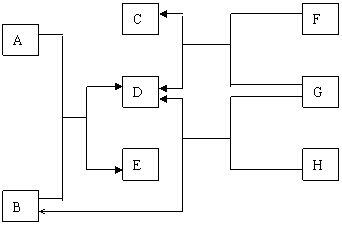 |
回答下列问题:
(1) 写出F的分子式
(2) 写出B的电子式
(3) 写出反应①的离子方程式
(4) 写出G在空气中燃烧产物与H反应的化学方程式,并标出电子转移方向和数目
28.(10分)今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生
第二份加足量NaOH溶液加热后,收集到0.04mol气体
第三份加足量BaCl2溶液后,得到干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
根据上述实验,回答以下问题:
(1) 由第一份进行的实验推断该混合物中可能存在的离子有
(2) 由第二份进行的实验得知混合物中应含有 离子,其物质的量浓度为
(3) 由第三份进行的实验可知6.27g沉淀的成分为
请计算形成这些沉淀的原混合物中各离子的物质的量。
(4) 综合上述实验,你认为以下结论正确的是
A.该混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl-
B. 该混合液中一定含有:NH4+、CO32-、SO42-,可能含K+、Cl-
C. 该混合液中一定含有:NH4+、CO32-、SO42-,可能含Mg2+、K+、Cl-
D. 该混合液中一定含有:NH4+、SO42-,可能含Mg2+、K+、Cl-
高中学业水平调研测试(必修科目)
化学试题参考答案
三、
24.A.抗坏血酸 不能 维生素B、C
蔬菜、水果等
羧基(或酯基)
B.(1)① (2)③ (3)⑥ (4)⑤ (5)④
25.
A.金属本性 介质或环境 覆盖保护层
我国能源结构以煤炭为主,改善燃煤质量、钙基固硫、开发新能源等其中一条。
B.(1)加成反应 (2)2CH3CH2OH+O2 →2CH3CHO+2H2O
CH3COOH+CH3CH2OH==CH3COOCH2CH3+H2O
四、
26.(1)容量瓶 冷凝管 (2)⑥② (3)试管
27.(1)C2H5OH
![]() (2)Na+[
O H]-
(2)Na+[
O H]-
(3)2Al+2OH-+2H2O==2AlO2-+ 3H2↑
![]()
![]()
![]() 2e-
2e-
(4)2Na2O2+2H2O ==4NaOH + O2 ↑
28.(1)Cl-、CO32-、SO42-,(2分)
(2)NH4+ 0.4mol/L (2分)
(3)BaCO3 BaSO4 (2分)CO32- 0.01mol、SO42- 0.02mol (2分)
(4)A(2分)